Содержание
- 3. Длина связи- расстояние между химически связанными атомами называют длиной связи. Как правило, длина химической связи меньше,
- 4. При образовании химической связи всегда происходит сближение атомов - расстояние между ними меньше, чем сумма радиусов
- 5. 1. Длина химической связи элемент–водород в ряду соединений СН4 – BH3 – BeH2 – LiH: 1)
- 6. 3. Длина связи уменьшается в ряду 1) HF, H2, HCl; 2) CO2, SO2, J2O5; 3) H2O,
- 7. 5. Длина связи увеличивается в ряду : 1)CCl4-CBr4-CF4; 2)SO2-SeO2-TeO2; 3)H2S-H2O-H2Se; 4)P2O5-P2S5-PCl5. 6. Длина связи увеличивается в
- 8. 7. Длина связи в ряду H2Te → H2Se → H2S 1) не изменяется; 2) увеличивается; 3)
- 9. 9. Длина связи Э-Сl увеличивается в ряду 1) хлорид углерода (IV), хлорид сурьмы (III); 2) хлорид
- 10. 10. Длина связи Э-О увеличивается в ряду 1) оксид кремния (IV), оксид углерода (IV); 2) оксид
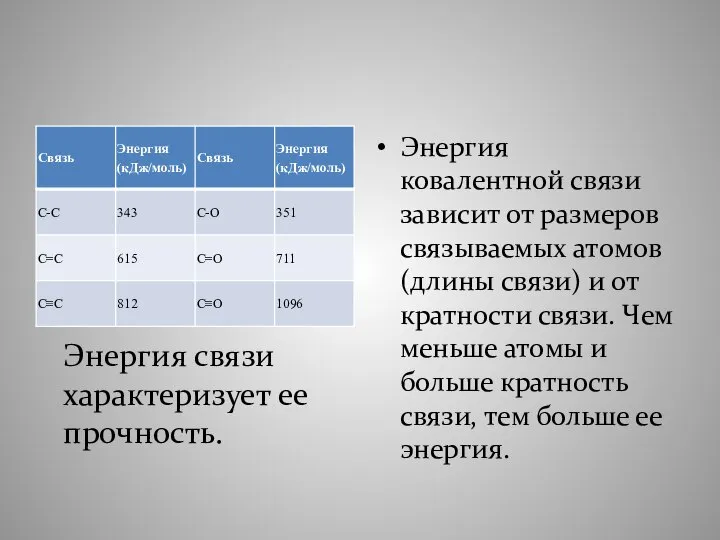
- 11. Энергия связи. Существенной характеристикой химической связи является ее прочность. Для оценки прочности связей обычно пользуются понятием
- 12. Энергия связи – энергия, выделяющаяся при ее образовании, или необходимая для разъединения двух связанных атомов.
- 13. Химическое соединение образуется из отдельных атомов только в том случае, если это энергетически выгодно. Чем выше
- 14. Энергия ковалентной связи зависит от размеров связываемых атомов (длины связи) и от кратности связи. Чем меньше
- 16. Энергия связи увеличивается в ряду:
- 17. Как изменяется энергия связи и межъядерное расстояние в рядах: А) HF, HCl, HBr, HI Увеличивается размер
- 18. Наименее прочная химическая связь в молекуле 1) О2 2) N2 3) Cl2 4) F2 Ответ: 4
- 19. 1. Молекула, в которой наиболее прочная химическая связь: 1) HF; 2) F2; 3) H2S; 4) O2.
- 20. 3. Прочность углеродной-углеродной связи в ряду этан– бензол–этилен–ацетилен 1) увеличивается 2) уменьшается 3) сначала увеличивается, затем
- 21. 4. Установите соответствие между химической связью и ее энергией
- 22. 5.Прочность связи увеличивается в ряду: а) H2O, H2S б) NH3, PH3 в) CS2, CO2 г) N2,
- 23. 7. Прочность связи увеличивается в ряду 1) NH3, PH3; 2) H2, Br2; 3) CS2, CO2; 4)
- 24. Кратность связи- число общих электронных пар, образующих связь. Расстояние между атомами существенно уменьшается при образовании кратных
- 25. 1.Число химических связей в молекулах увеличивается в ряду 1) H2O, CO2, H2S; 2) N2, CH4, O2;
- 26. 3. Число химических связей в молекулах увеличивается в ряду 1) HClO2, CO, HCl; 2) O2, CF4,
- 27. 5.Число химических связей в молекулах уменьшается в ряду 1) HCl, CS2, HClO2; 2) CF4, Cl2, Ar;
- 28. 7. Число химических связей в молекулах увеличивается в ряду 1) NСl3, C2H6, PCl5; 2) CCl4, Cl2,
- 29. 9.Число двойных связей увеличивается в ряду 1) SO3, H2SO4, H3PO4; 2) C2H4, C2H2, NO; 3) NO,
- 30. 11. Число σ-связей уменьшается в ряду 1) SF6, SO2, SO3; 2) H3PO4, WF6, SiCl4; 3) NH3,
- 31. 13. Число двойных связей увеличивается в ряду 1) SO2, H2SO3, H3PO4; 2) C2H6, C2H4, NO; 3)
- 32. 15.Число двойных связей уменьшается в ряду 1) NO, CS2, SO3; 2) C2H4, C2H2, NO; 3) SO3,
- 33. Полярность связи. Полярность химической связи зависит от разности электроотрицательностей связываемых атомов. Полярность связи обусловлена неравномерным распределением
- 35. 1.Полярность связи С-Э уменьшается в ряду 1) CO2, CS2, CCl4; 2) CF4, C2H6, CO2; 3) Al4C3,
- 36. 3.Полярность химической связи O-Н увеличивается в ряду 1) H2SO4, H3PO4; 2) HClO4, HClO3; 3) HNO3, Al(OH)3;
- 37. Насыщаемость ковалентной связи обусловлена ограниченными валентными возможностями атомов, т.е. их способностью к образованию строго определенного числа
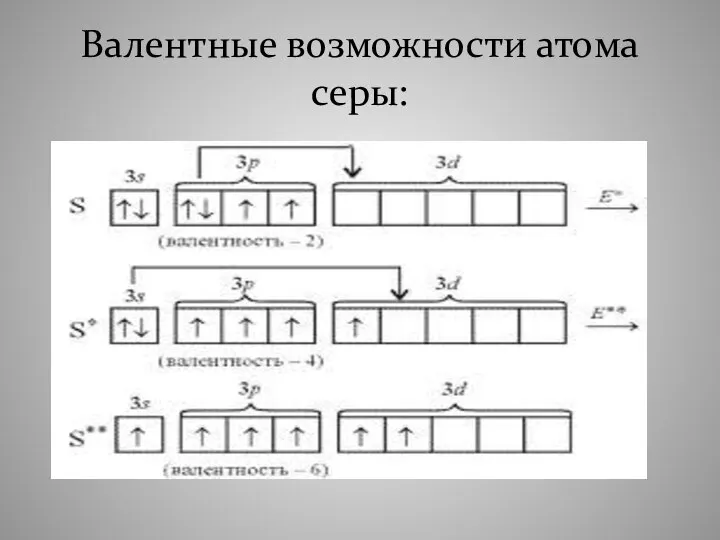
- 38. Валентные возможности атома серы:
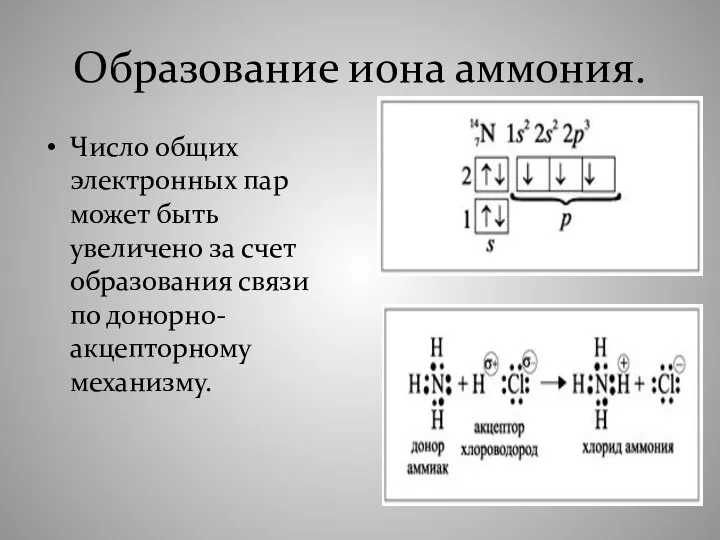
- 39. Образование иона аммония. Число общих электронных пар может быть увеличено за счет образования связи по донорно-
- 40. Направленность- – определенное направление химической связи, которое возникает в результате перекрывания электронных облаков. Направленность определяется строением
- 42. СТРОЕНИЕ МОЛЕКУЛ. РХТУ.
- 47. Скачать презентацию









































 Биоорганическая химия
Биоорганическая химия Подготовка газа к транспорту с применением процесса низкотемпературной сепарации
Подготовка газа к транспорту с применением процесса низкотемпературной сепарации Предельные углеводороды
Предельные углеводороды Производство стекла
Производство стекла Химические свойства строительных материалов. Урок №5
Химические свойства строительных материалов. Урок №5 Основные виды и понятия курса органической химии в старшей школе
Основные виды и понятия курса органической химии в старшей школе Изотопы. (8 класс)
Изотопы. (8 класс) Ароматические и гетероциклические соединения. Электронная спектроскопия
Ароматические и гетероциклические соединения. Электронная спектроскопия Смесители. Пропеллерная мешалка
Смесители. Пропеллерная мешалка Водород. Химический элемент
Водород. Химический элемент Алюминий и его соединения
Алюминий и его соединения Карбоновые кислоты
Карбоновые кислоты Дисперсті жүйелердің оптикалық әдістері
Дисперсті жүйелердің оптикалық әдістері Презентация по Химии "Кинетика химических реакций.Химическое равновесие" - скачать смотреть
Презентация по Химии "Кинетика химических реакций.Химическое равновесие" - скачать смотреть  Основные классы неорганических веществ
Основные классы неорганических веществ Химический элемент, минерал, горная порода. (Лекция 6)
Химический элемент, минерал, горная порода. (Лекция 6) Вещественный состав магматических горных пород
Вещественный состав магматических горных пород Протравка стекла с помощью ионного обмена
Протравка стекла с помощью ионного обмена Фосфор Соединения фосфора химия 9 класс
Фосфор Соединения фосфора химия 9 класс  Карбоновые кислоты. Лекция 7
Карбоновые кислоты. Лекция 7 Природные и попутные нефтяные газы
Природные и попутные нефтяные газы Рецепторы анионов
Рецепторы анионов Альтернативная бытовая химия
Альтернативная бытовая химия Расстворение. Расстворы
Расстворение. Расстворы Химия и повседневная жизнь человека
Химия и повседневная жизнь человека Рідкі кристали
Рідкі кристали  Химия вокруг нас Презентация к внеклассному мероприятию Альбина Фанузовна Хамидуллина учитель химии первой квалификационно
Химия вокруг нас Презентация к внеклассному мероприятию Альбина Фанузовна Хамидуллина учитель химии первой квалификационно Элементы V А группы. Азот и его соединения
Элементы V А группы. Азот и его соединения