Содержание
- 2. Кислоты Кислоты – это электролиты, которые при диссоциации образуют катионы водорода и анионы кислотного остатка. Диссоциация:
- 3. Классификация кислот По растворимости Растворимые Нерастворимые азотная кислота осадок кремниевой кислоты
- 4. Классификация кислот По наличию кислорода Кислородсодержащие Бескислородные уксусная кислота соляная кислота
- 5. Классификация кислот По основности ОДНООСНОВНЫЕ НСl, HNO3 ДВУХОСНОВНЫЕ H2SO4, H2CO3 ТРЕХОСНОВНЫЕ H3PO4
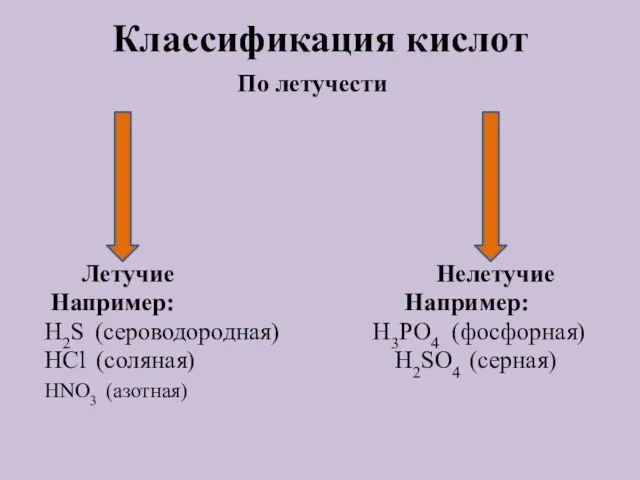
- 6. Классификация кислот По летучести Летучие Нелетучие Например: Например: H2S (сероводородная) H3PO4 (фосфорная) HCl (соляная) H2SO4 (серная)
- 7. Типичные реакции кислот Кислота + основание = соль + вода 2) Кислота + оксид металла =
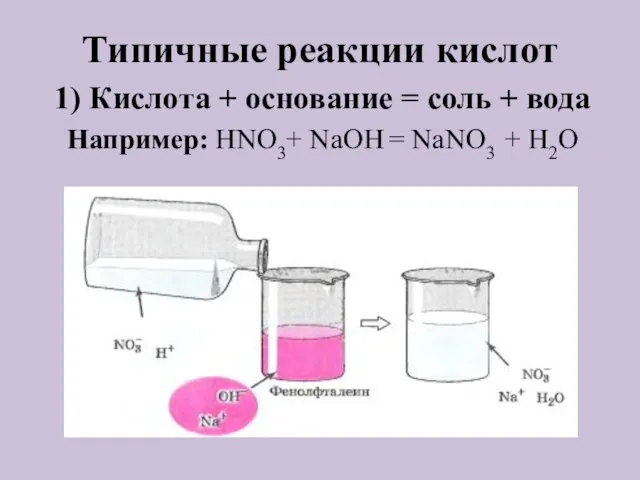
- 8. Типичные реакции кислот 1) Кислота + основание = соль + вода Например: HNO3+ NaOH = NaNO3
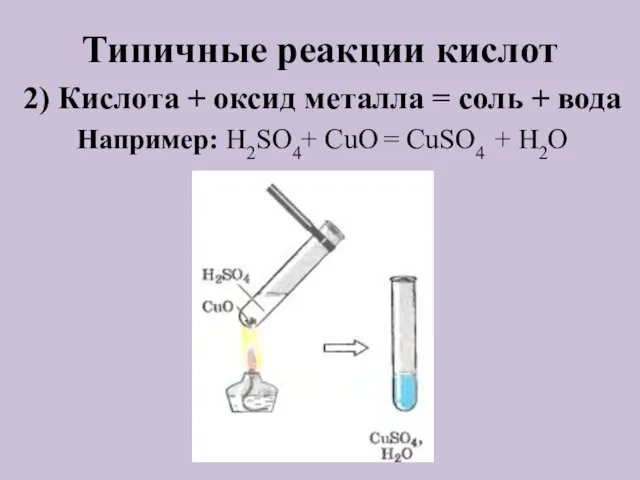
- 9. Типичные реакции кислот 2) Кислота + оксид металла = соль + вода Например: H2SO4+ CuO =
- 10. Типичные реакции кислот 2) Кислота + металл = соль + водород Например: HCl + Zn =
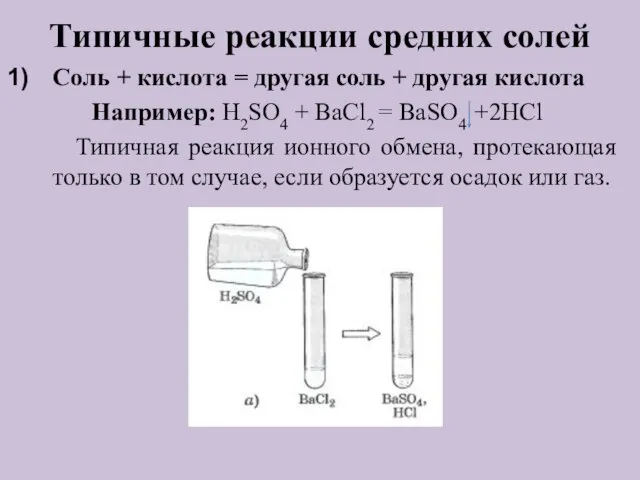
- 11. Типичные реакции средних солей Соль + кислота = другая соль + другая кислота Например: H2SO4 +
- 12. Практическое применение кислот Производство лекарств; химических продуктов и товаров; минеральных удобрений; красок; пластмасс и т.д.;
- 14. Скачать презентацию







 Хімічні зв’язки
Хімічні зв’язки Минерал клинохлор. Месторождения
Минерал клинохлор. Месторождения Ковалентная неполярная химическая связь
Ковалентная неполярная химическая связь Нітрати в продуктах харчування
Нітрати в продуктах харчування  Метаморфические горные породы
Метаморфические горные породы Sample Kit Kemira 3f. External
Sample Kit Kemira 3f. External Биологическое значение элементов неорганоненов и их применение в медицине
Биологическое значение элементов неорганоненов и их применение в медицине Формирование навыков научно-исследовательской деятельности школьников 5-7 классов
Формирование навыков научно-исследовательской деятельности школьников 5-7 классов Физические и химические явления
Физические и химические явления Синтетические лекарственные средства
Синтетические лекарственные средства Школьное мероприятие Д. И. Менделеев в высказываниях Автор: Ким Наталья Викторовна учитель химии
Школьное мероприятие Д. И. Менделеев в высказываниях Автор: Ким Наталья Викторовна учитель химии  Алканы. Строение алканов
Алканы. Строение алканов Разработка технологии получения раствора коагулянта в условиях филиала «Азот» АО «ОХК «УРАЛХИМ»
Разработка технологии получения раствора коагулянта в условиях филиала «Азот» АО «ОХК «УРАЛХИМ» Радиоуглеродный анализ
Радиоуглеродный анализ БИОЛОГИЧЕСКИ АКТИВНЫЕ НИЗКОМОЛЕКУЛЯРНЫЕ ВЕЩЕСТВА
БИОЛОГИЧЕСКИ АКТИВНЫЕ НИЗКОМОЛЕКУЛЯРНЫЕ ВЕЩЕСТВА  Презентация Вещества и их свойства
Презентация Вещества и их свойства Химические свойства хрома и его соединений
Химические свойства хрома и его соединений Свинец. Строение атома свинца
Свинец. Строение атома свинца Лекция 10. Химия s-элементов
Лекция 10. Химия s-элементов Аттестационная работа. Влияние электромагнитного излучения смартфонов на жизнедеятельность микроорганизмов
Аттестационная работа. Влияние электромагнитного излучения смартфонов на жизнедеятельность микроорганизмов Медициналық тәжірибедегі потенциометриялар
Медициналық тәжірибедегі потенциометриялар Презентация по Химии "Презентация Войди в природу другом" - скачать смотреть
Презентация по Химии "Презентация Войди в природу другом" - скачать смотреть  Наноструктурированные тонкие пленки суперсплавов Mo, W и Re с 3d6-8 металлами
Наноструктурированные тонкие пленки суперсплавов Mo, W и Re с 3d6-8 металлами Гидрокаталитические процессы
Гидрокаталитические процессы Гидролиз. Фармацевтический филиал ГБОУ СПО Сомк
Гидролиз. Фармацевтический филиал ГБОУ СПО Сомк Алканы. Задания
Алканы. Задания Применение закона действующих масс к окислительно-восстановительным равновесиям. (Лекция 6)
Применение закона действующих масс к окислительно-восстановительным равновесиям. (Лекция 6) Колообіг води Виконав Проданчук Олег Учень 10-А класу
Колообіг води Виконав Проданчук Олег Учень 10-А класу