Содержание
- 2. Электрохимическая цепь (гальванический элемент) является комбинацией электродов. Из обратимых электродов составляют обратимые элементы. Учитывая природу электродной
- 3. Электрохимические цепи, в которых электроды отличаются лишь физическими свойствами, называются физическими цепями. Источником электрической энергии в
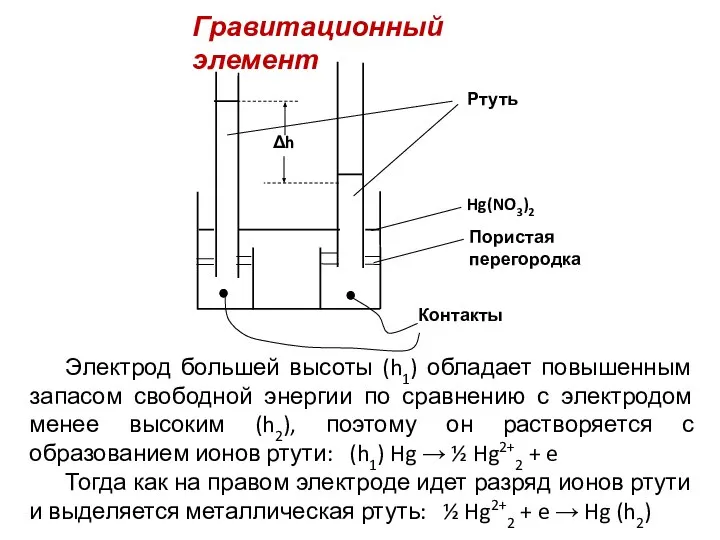
- 4. Гравитационный элемент Электрод большей высоты (h1) обладает повышенным запасом свободной энергии по сравнению с электродом менее
- 5. Суммарный процесс в гравитационной цепи состоит в переносе ртути от высокого электрода к низкому. Этот самопроизвольный
- 6. Электрод, изготовленный из металла в метастабильном состоянии (Мβ), обладает повышенным запасом свободной энергии, играет роль отрицательного
- 7. Различной энергией обладают: разные грани монокристалла; кристаллы различных размеров, которые образуются за счет нарушения режима охлаждения
- 8. II тип. Химические цепи (элементы) Элемент составлен из электродов, отличающихся друг от друга по физическим и
- 9. Простая химическая цепь – водородно-кислородный элемент: Реакция на водородном электроде: H2 ⇔ 2H+ + 2e. Реакция
- 10. ЭДС водородно-кислородного элемента зависит от парциального давления водорода и кислорода и не зависит от рН среды.
- 11. Простая химическая цепь - стандартный элемент Вестона: Cd (Hg) │ CdSO4│Hg2SO4│Hg. ЭДС этого элемента отличается постоянством
- 12. Токообразующие процессы, лежащие в основе уравнения ЭДС, отвечают теории двойной сульфатации Гладстона и Трайба. Оба электрода
- 13. Сложная химическая цепь – элемент Даниэля-Якоби: Zn│ZnSO4║CuSO4│Cu, в котором протекает реакция: Zn + Cu2+ ⇔ Cu
- 14. Определение стандартного электродного потенциала и коэффициентов активности Стандартные потенциалы металлических электродов, термодинамически устойчивых в водных растворах,
- 15. Средняя ионная активность а± соли выражается уравнением: где: ν+, ν- - числа положительных и отрицательных ионов,
- 16. средний коэффициент активности соли; фактор валентности; Если исследуемый электрод положительнее электрода сравнения, например, в элементе: Ag
- 17. Е' = E0 , Уравнение преобразуем, перенося в левую часть все известные члены, а в правой
- 18. При известных Е, Е0 и концентрации электролита, средний коэффициент активности может быть рассчитан по уравнениям: если
- 19. Определение константы устойчивости комплекса Ион металла Мz+ с лигандами L- образует комплекс [MLn]z-n : Mz+ +
- 21. Скачать презентацию

















 Химия вокруг нас
Химия вокруг нас Обмен белков. Источники и пути обезвреживания аммиака. (Лекция 15)
Обмен белков. Источники и пути обезвреживания аммиака. (Лекция 15) Производство шампуня. Технология
Производство шампуня. Технология Физико-химические основы патологии клетки. Митохондрии и апоптоз
Физико-химические основы патологии клетки. Митохондрии и апоптоз Виды присадок к моторным топливам
Виды присадок к моторным топливам Идеи и прогнозы Д. И. Менделеева в области улучшения плодородия почв.
Идеи и прогнозы Д. И. Менделеева в области улучшения плодородия почв. Мыло и мыловарение
Мыло и мыловарение Химический состав молока
Химический состав молока Презентация по Химии "Природные соединения кремния" - скачать смотреть
Презентация по Химии "Природные соединения кремния" - скачать смотреть  Метаморфогенная серия. Группа регионального метаморфизма
Метаморфогенная серия. Группа регионального метаморфизма Свойства неорганических веществ. (Задание 37. ЕГЭ по химии)
Свойства неорганических веществ. (Задание 37. ЕГЭ по химии) Алкины. Ацетилен
Алкины. Ацетилен Современные конструкционные материалы
Современные конструкционные материалы Прикладная геохимия. Вторичные ореолы
Прикладная геохимия. Вторичные ореолы Производные фенилуксусной и фенилпропионовой кислот
Производные фенилуксусной и фенилпропионовой кислот «Надпровідний розчин» Опишіть, яким чином на електропровідність розчинів впливають температура, природа розчинника, природа
«Надпровідний розчин» Опишіть, яким чином на електропровідність розчинів впливають температура, природа розчинника, природа  Биологически важные реакции монофункциональных соединений. Реакционная способность альдегидов, кетонов, карбоновых кислот
Биологически важные реакции монофункциональных соединений. Реакционная способность альдегидов, кетонов, карбоновых кислот Жидкость-жидкость. Эмульсии - грубодисперные системы из несмешивающихся жидкостей с размером капель от 100 до 5000 нм. Свойства эмульсии: 1. Эмульсии имеют поверхность раздела. 2. Эмульсии неустойчивы. 3. Эмульсии нуждаются в стабилиза
Жидкость-жидкость. Эмульсии - грубодисперные системы из несмешивающихся жидкостей с размером капель от 100 до 5000 нм. Свойства эмульсии: 1. Эмульсии имеют поверхность раздела. 2. Эмульсии неустойчивы. 3. Эмульсии нуждаются в стабилиза Химические реакции. Скорость химической реакции
Химические реакции. Скорость химической реакции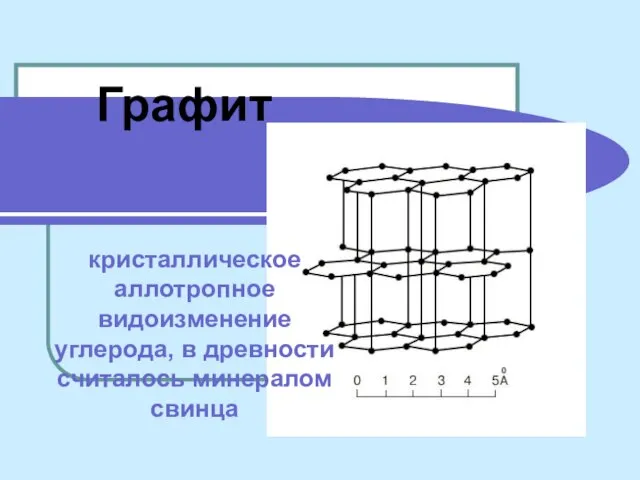 Графит кристаллическое аллотропное видоизменение углерода, в древности считалось минералом свинца
Графит кристаллическое аллотропное видоизменение углерода, в древности считалось минералом свинца Композиционные материалы
Композиционные материалы Кислородные соединения азота
Кислородные соединения азота Водород. Получение водорода
Водород. Получение водорода Гидролиз солей
Гидролиз солей Исследовательская работа по химии Количественное содержание витамина С в ягодах клюквы и проблема сохранности в зимний период вр
Исследовательская работа по химии Количественное содержание витамина С в ягодах клюквы и проблема сохранности в зимний период вр Фосфор. История открытия
Фосфор. История открытия Бензол молекуласында байланыстардың түзілу сызбанұсқасы
Бензол молекуласында байланыстардың түзілу сызбанұсқасы Основания. Классификация оснований
Основания. Классификация оснований