Если растворитель – вода:
O2 + 4H+ + 4e = 2H2O (в
кислой среде)
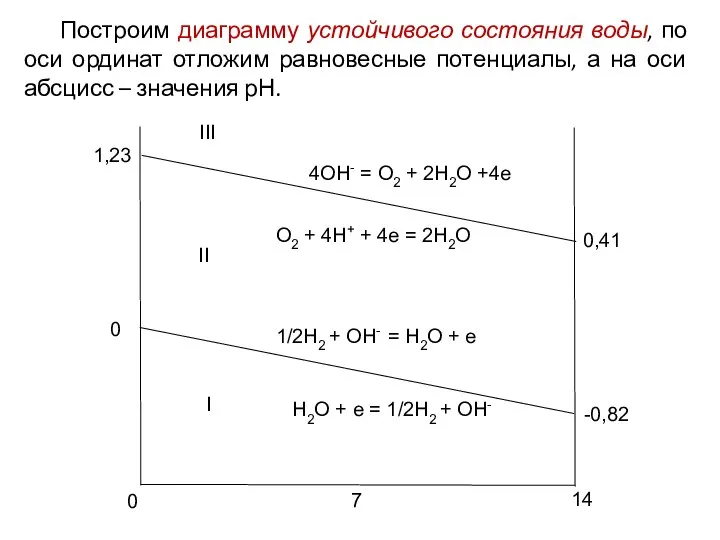
O2 + 2H2O + 4e = 4OH- (в щелочной среде) Eр =1,23 – 0,059 рН
Н+ + e = 1/2Н2 (в кислой среде)
Н2О + е = 1/2Н2 + ОН- (в щелочной среде) Ер = - 0,059рН
Термодинамическая устойчивость электродов
в водных растворах
Большинство электрохимических процессов протекает в контакте с водой и воздухом. Для того, чтобы на электроде установился равновесный потенциал, необходимо отсутствие всех видов побочных реакций.
Возможность получения равновесного потенциала какого-либо электрода определяется соотношением равновесных потенциалов этого электрода и электрохимической реакции с участием растворителя.







 ХИМИЯ - это наука о веществах и их превращениях. все вещества состоят из мельчайших, далее неделимых частиц - атомов (греч. атомос означает «неделимый») – (, Эпикур, Демокрит, V - III вв. до н. э.). -1911г. Планетарная модель Э. Резерфорда 19
ХИМИЯ - это наука о веществах и их превращениях. все вещества состоят из мельчайших, далее неделимых частиц - атомов (греч. атомос означает «неделимый») – (, Эпикур, Демокрит, V - III вв. до н. э.). -1911г. Планетарная модель Э. Резерфорда 19 Химические формулы. Относительная молекулярная масса. 8 класс
Химические формулы. Относительная молекулярная масса. 8 класс Предмет органической химии. Тест 18
Предмет органической химии. Тест 18 Химический состав водоотталкивающих средств
Химический состав водоотталкивающих средств Презентація на тему: “Мінеральні добрива” Підготував: Учень 10-А класу Матвійчук Роман
Презентація на тему: “Мінеральні добрива” Підготував: Учень 10-А класу Матвійчук Роман  Сложные эфиры
Сложные эфиры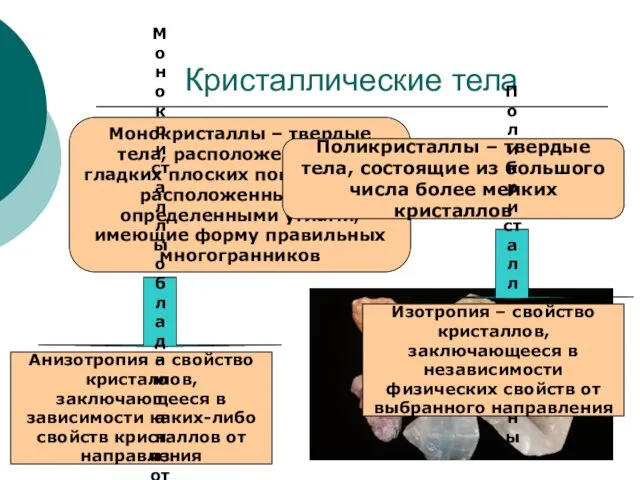 Кристаллические тела
Кристаллические тела Физический этап развития периодического закона
Физический этап развития периодического закона Химический эквивалент. Современные представления
Химический эквивалент. Современные представления Минеральные удобрения: польза и вред
Минеральные удобрения: польза и вред Классификация гомеопатических лекарственных средств
Классификация гомеопатических лекарственных средств Аттестационная работа. Образовательная программа кружка «Химия и жизнь»
Аттестационная работа. Образовательная программа кружка «Химия и жизнь» Образование почвообразующих пород под действием эоловых процессов. (Лекция 5)
Образование почвообразующих пород под действием эоловых процессов. (Лекция 5) Вольфрам. Знаходження в періодичній системі
Вольфрам. Знаходження в періодичній системі Натрий
Натрий Окислительно-восстановительные процессы
Окислительно-восстановительные процессы Electron configuration and periodicity
Electron configuration and periodicity Характеристика неметаллов. Галогены
Характеристика неметаллов. Галогены Физико-химические процессы переработки нефти. Термические процессы
Физико-химические процессы переработки нефти. Термические процессы Периодическая система элементов Д. И. Менделеева. IA группа
Периодическая система элементов Д. И. Менделеева. IA группа Чистые вещества и смеси Способы разделения смесей Цели: 1. Выяснить какое вещество считают чистым. 2. Что такое смесь? Какие бы
Чистые вещества и смеси Способы разделения смесей Цели: 1. Выяснить какое вещество считают чистым. 2. Что такое смесь? Какие бы Иммунохимические методы. Иммуноферментный анализ (ИФА )
Иммунохимические методы. Иммуноферментный анализ (ИФА ) КУБАНСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ КАФЕДРА ФУНДАМЕНТАЛЬНОЙ И КЛИНИЧЕСКОЙ БИОХИМИИ Лекция по теме: «Обмен белко
КУБАНСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ КАФЕДРА ФУНДАМЕНТАЛЬНОЙ И КЛИНИЧЕСКОЙ БИОХИМИИ Лекция по теме: «Обмен белко Презентация Химический алфавит
Презентация Химический алфавит  Синтез и изучение свойств фоточувствительного холестерического жидкого кристалла
Синтез и изучение свойств фоточувствительного холестерического жидкого кристалла Формы природных выделений минералов. Занятие 2
Формы природных выделений минералов. Занятие 2 Коррозия, как источник загрязнения окружающей среды
Коррозия, как источник загрязнения окружающей среды Химическая посуда и ее назначения (5)
Химическая посуда и ее назначения (5)