Содержание
- 2. III тип. Концентрационные элементы Элемент составлен из электродов, совпадающих по физическим свойствам и природе электродной реакции.
- 3. Концентрационные элементы бывают двух типов: с переносом и без переноса. В концентрационных элементах с переносом в
- 4. Изменение количества вещества около правого электрода (в молях): -1Zn2+ + t+ Zn2+ -2t- Cl- = -t-
- 5. С учетом того, что , можно записать: где: Е+ – ЭДС элемента с переносом, составленного из
- 6. Чтобы приготовить концентрационную цепь без переноса, необходимо соединить навстречу друг другу два простых химических элемента типа:
- 7. На электродах левого элемента пойдут обратные процессы: на левом: 2Hg + 2Cl- - 2e → Hg2Cl2
- 8. Измерением ЭДС цепей с переносом и без переноса можно найти числа переноса: Полученные значения чисел переноса
- 9. Диффузионный потенциал Скачок потенциала на границе двух растворов называется диффузионным потенциалом, возникает в том случае, если
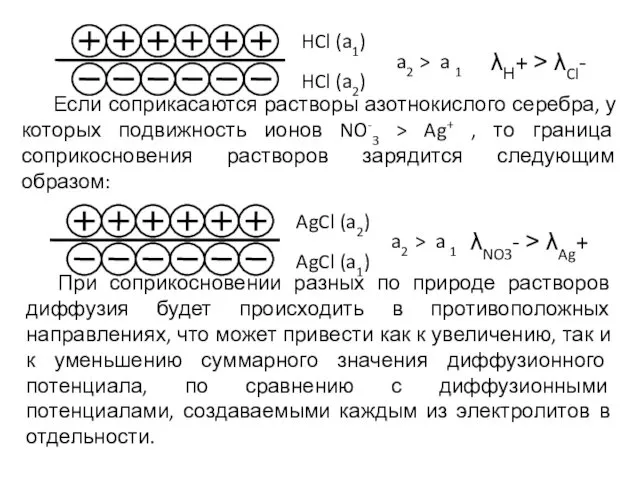
- 10. Если соприкасаются растворы азотнокислого серебра, у которых подвижность ионов NO-3 > Ag+ , то граница соприкосновения
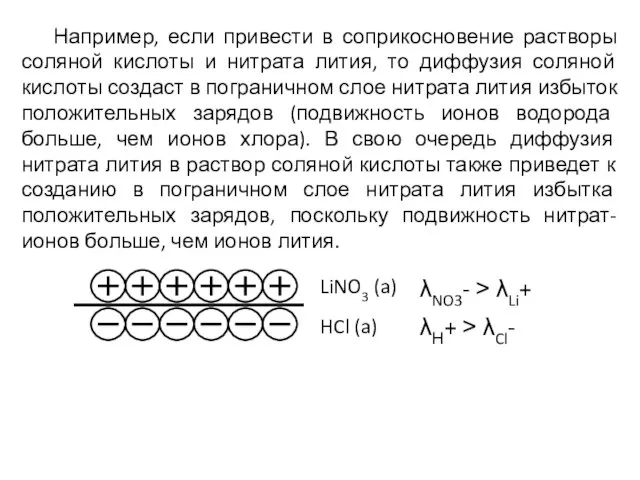
- 11. Например, если привести в соприкосновение растворы соляной кислоты и нитрата лития, то диффузия соляной кислоты создаст
- 12. Взаимная диффузия на границе соприкосновения растворов нитрата лития и гидроксида натрия, наоборот, будет приводить к уменьшению
- 13. Если доля тока, переносимая данным сортом ионов, равна ti, то отношение , где zi – заряд
- 14. Метод расчета разработан в 1907 году Гендерсоном. Он принял, что в переходном слое состав изменяется плавно
- 15. λi – подвижность ионов; zi – заряды ионов; сiI, ciII – концентрации растворов I и II.
- 16. Уравнение Гендерсона ввиду его сложности в общем виде обычно не используется. Практически более важны простые частные
- 18. Скачать презентацию













 Введение. Основные понятия химии
Введение. Основные понятия химии I закон термодинамики, его применение для расчёта тепловых эффектов
I закон термодинамики, его применение для расчёта тепловых эффектов Дозиметрия ионизирующих излучений. Влияние радиации на организм человека
Дозиметрия ионизирующих излучений. Влияние радиации на организм человека Камни и Рак
Камни и Рак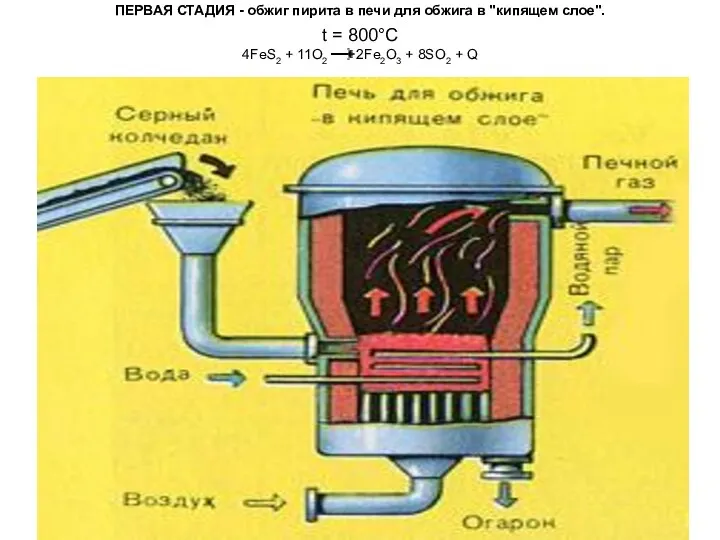 Получение серной кислоты
Получение серной кислоты Презентация Спирты
Презентация Спирты Глицерин Свойства - применение Выполнила учитель химии МОУ «Средняя школа №7» г. Балаково Саратовской области Трибунская Е
Глицерин Свойства - применение Выполнила учитель химии МОУ «Средняя школа №7» г. Балаково Саратовской области Трибунская Е Получение водорода в промышленности и его применение Химия 8 класс
Получение водорода в промышленности и его применение Химия 8 класс  Исследование влияния концентрации наночастиц никеля в водных растворах на генерацию активных форм кислорода при лазерном пробое
Исследование влияния концентрации наночастиц никеля в водных растворах на генерацию активных форм кислорода при лазерном пробое Классификация химических элементтов
Классификация химических элементтов Презентация по Химии "Нитраты - минеральные удобрения" - скачать смотреть
Презентация по Химии "Нитраты - минеральные удобрения" - скачать смотреть  Фізичні та хімічні явища. (7 клас)
Фізичні та хімічні явища. (7 клас) Каучук. История открытия
Каучук. История открытия Материаловедение. Теория термической обработки стали. (Тема 8)
Материаловедение. Теория термической обработки стали. (Тема 8) Органические вещества. Валентность. Теория химического строения
Органические вещества. Валентность. Теория химического строения Основы общей химии
Основы общей химии Важнейшие химические понятия и законы
Важнейшие химические понятия и законы Презентация по химии Неорганические и органические основания.
Презентация по химии Неорганические и органические основания.  Особенности строения, реакционной способности и методы синтеза алкенов
Особенности строения, реакционной способности и методы синтеза алкенов Водород, нахождение в природе. Получение водорода и его физические свойства
Водород, нахождение в природе. Получение водорода и его физические свойства Классификация оснований
Классификация оснований PSKhE
PSKhE Электрофизические свойства GaAs, зонная структура, полупроводящий и полуизолирующий GaAs, способы создания p-n перехода
Электрофизические свойства GaAs, зонная структура, полупроводящий и полуизолирующий GaAs, способы создания p-n перехода Деструкция углеводородов
Деструкция углеводородов Физические, химические свойства предельных и непредельных карбоновых кислот, получение
Физические, химические свойства предельных и непредельных карбоновых кислот, получение Классификация силикатов
Классификация силикатов - Это оружие массового поражения, действие которого основано на токсических свойствах химических веществ. - Это оружие массового
- Это оружие массового поражения, действие которого основано на токсических свойствах химических веществ. - Это оружие массового  Алюминий и его органические производные
Алюминий и его органические производные