Содержание
- 2. Коррозия углеродистых и низколегированных сталей в различных средах
- 3. рH 3 6 9 12 Влияние рН на скорость коррозии Fe Vкор mFe(OH)2ּ nFe(OH)3ּkH2O Fe(OH)2 НFeO2-
- 4. Кислотная коррозия 1. Растворение барьерной пленки оксидов и облегчения диффузии кислорода; 2. Повышение концентрации ионов Н+
- 5. Кислотная коррозия Пример: коррозия в НСl – 0,04% В присутствии О2 – 9,9мм/год; В отсутствии О2
- 6. Кислотная коррозия В слабых кислотах (борная, щавелевая, лимонная) переход в область кислотной коррозии при рН 5-6;
- 7. Кислотная коррозия Fe – 2e → Fe2+ НО анодный процесс идёт стадийно в отдельных стадиях участвуют
- 8. Влияние вида кислоты на коррозию железа
- 9. Коррозия железа в HNO3 самая высокая скорость коррозии в HNO3 за счет наличия трех окислителей Н+,
- 10. Коррозия железа в HNO3 Концентрированная азотная кислота > 58% может перевозиться в стальных цистернах. Дымящая HNO3
- 11. Влияние вида кислоты на коррозию железа
- 12. Коррозия железа в H2SO4 Максимальная скорость коррозии при концентрации 50-60%, далее начинает падать. Пассивация в серной
- 13. Коррозия железа в HСl В средних концентраций скорость коррозии существенно ниже, чем в HNO3 и H2SO4.
- 14. Коррозия железа в H3РO4 Влияние концентрации кислоты сходно с влиянием ее в H2SO4 Максимальная скорость коррозии
- 15. Коррозия железа в HF До 50% углеродистые и низколегированные стали растворяются очень активно; При более высоких
- 16. Влияние температуры Чем выше температура, тем выше скорость коррозии. Особенно сильно это влияние проявляется в НCl,
- 17. Влияние на коррозию сталей примесей 0,1N HCl
- 18. Влияние на коррозию стали вида обработки % HCl 0,02 0,08 Кm г/м2сутки 50 100 150 Прокат
- 19. рH 3 6 9 12 Влияние рН на скорость коррозии Fe в нейтральных средах Vкор mFe(OH)2ּ
- 20. Коррозия в нейтральных средах Катодный процесс: O2 + 2H2O + 4e → 4OH– Анодный процесс: Fe
- 22. Коррозия в нейтральных средах В атмосфере могут присутствовать: CO2, H2S, SO2. FeSO4 ухудшает упорядоченность плёнки, FeCO3
- 23. Коррозия в нейтральных средах Небольшое количество меди (0,2 - 0,3 %) на 20% уменьшает скорость коррозии
- 24. Коррозия в нейтральных средах Влияние хрома при концентрации его в стали от 1 до 2 %
- 25. Коррозия в нейтральных средах Влияние температуры на скорость коррозии в нейтральных средах
- 26. Коррозия в нейтральных средах Влияние анионного состава коррозионной среды
- 27. Коррозия в нейтральных средах Влияние анионного состава коррозионной среды NaCl Na2SO4 NaNO3 скорость коррозии повышается NH4NO3
- 28. Коррозия в нейтральных средах Влияние концентрации коррозионной среды Кривые с максимумом для хорошо растворимых солей: рост:
- 29. рH 3 6 9 12 Влияние рН на скорость коррозии Fe в щелочах Vкор Fe(OH)2 НFeO2-
- 30. Влияние рН на скорость коррозии Fe в щелочах Скорость коррозии в растворах щелочей сильно зависит от:
- 31. Влияние рН на скорость коррозии Fe в щелочах
- 32. Влияние рН на скорость коррозии Fe в щелочах
- 34. Скачать презентацию































 Волокно капрон
Волокно капрон Полимеры, пластмассы и изделия из них
Полимеры, пластмассы и изделия из них Моделирование, как метод научного исследования. Ограниченный метод Хартри-Фока
Моделирование, как метод научного исследования. Ограниченный метод Хартри-Фока Электролиз: опыты к заданиям ЕГЭ
Электролиз: опыты к заданиям ЕГЭ Битумы и материалы на основе битумов
Битумы и материалы на основе битумов Камни мира. Минералы
Камни мира. Минералы Молярный объём газов
Молярный объём газов Катаболизм фенилаланина, тирозина
Катаболизм фенилаланина, тирозина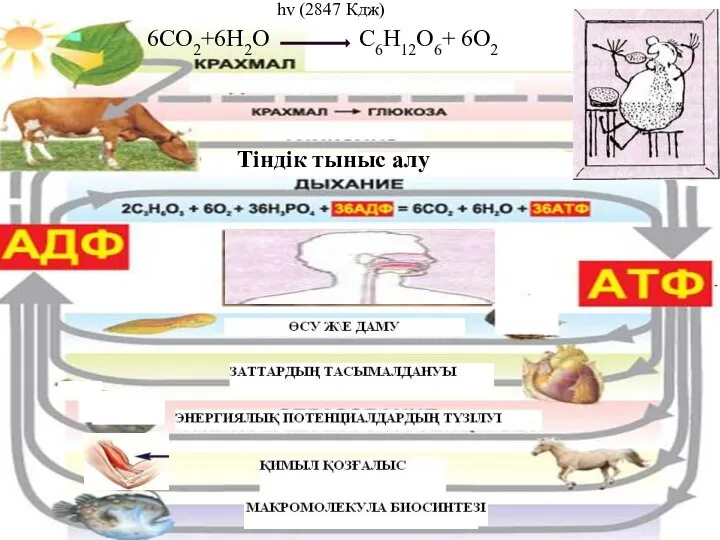 Биологиялық тотығу электрондардың тасымалдану тізбегі тотығудан фосфорлану
Биологиялық тотығу электрондардың тасымалдану тізбегі тотығудан фосфорлану Установка гидрокрекинга в составе завода глубокой переработки нефти ООО Кинеф
Установка гидрокрекинга в составе завода глубокой переработки нефти ООО Кинеф Зависимость свойств химических элементов от положения в ПСХЭ
Зависимость свойств химических элементов от положения в ПСХЭ Презентация по Химии "Химическая природа белка" - скачать смотреть
Презентация по Химии "Химическая природа белка" - скачать смотреть  АТФ (Аденозинтрифосфат)
АТФ (Аденозинтрифосфат) Азот. Физические и химические свойства азота
Азот. Физические и химические свойства азота Классификация и краткие характеристики основных групп токсикантов
Классификация и краткие характеристики основных групп токсикантов Хлороводород. Соляная кислота.
Хлороводород. Соляная кислота.  Уксусная кислота
Уксусная кислота Основания. Физические свойства оснований
Основания. Физические свойства оснований Плавиковая кислота или фтористоводородная кислота
Плавиковая кислота или фтористоводородная кислота Едкость Coca-Cola
Едкость Coca-Cola Химический элемент платина
Химический элемент платина Липидтер
Липидтер Подготовил учитель химии МОУ СОШ № 16 С. Александровского Александровского района Кононенко Светлана Юрьевна
Подготовил учитель химии МОУ СОШ № 16 С. Александровского Александровского района Кононенко Светлана Юрьевна Исследование содержания аскорбиновой кислоты в зимних сортах яблок, районированных в Петровском районе Ставропольского края
Исследование содержания аскорбиновой кислоты в зимних сортах яблок, районированных в Петровском районе Ставропольского края  Гравиметрические методы анализа
Гравиметрические методы анализа Дәрілік препараттардың синтезі мен олардың классификациясы
Дәрілік препараттардың синтезі мен олардың классификациясы Необратимый (совместный) гидролиз
Необратимый (совместный) гидролиз Хроматофокусирование: новые подходы в концентрировании и разделении
Хроматофокусирование: новые подходы в концентрировании и разделении