Слайд 6

Электронные соединения (фазы Юм-Розери)
Электронные соединения (ЭС) образуются в металлических сплавах
между одновалентными металлами: Cu, Ag, Li, металлами переходных групп Fe, Mn, Co с одной стороны и металлами с валентностью от 2 до 5: Be, Zn, Cd, Sn, Si c другой. Эти соединения характеризуются определенным отношением числа валентных электронов к числу атомов в соединении: 3/2, 21/13, 7/4. Каждому отношению соответствует определенный тип кристаллической решетки. При отношении 3/2 образуется решетка ОЦК. Такое ЭС называют β-фаза (например CuZn). ЭС, у которых отношение числа свободных электронов к числу атомов составляет 21/13, имеют кубическую решетку, называют γ-фазой (например Cu5Zn8). При отношении 7/4 соединение имеет решетку ГП и называется ε-фаза (например CuZn3). У электронных соединений определенное соотношение атомов и новая, отличная от решетки компонентов, кристаллическая решетка является признаком химического соединения. Однако в ЭС нет строгого упорядочения атомов, по крайней мере при повышенных температурах, расположения атомов. При понижении температуры в ЭС происходит упорядочение. Поэтому, ЭС следует отнести к промежуточным фазам.


![Взаимодействие дислокации с растворенными атомами ∆τ = α G b∑[δК (с/сmax)К]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1396519/slide-3.jpg)















 Стискання газів. Рівняння Менделєєва-Клапейрона
Стискання газів. Рівняння Менделєєва-Клапейрона Спиртзавод ОАО «Петровский»
Спиртзавод ОАО «Петровский» Проект: жило-было мыло
Проект: жило-было мыло Искусственные или технические битумы
Искусственные или технические битумы Минералдар және олардың агрегаттарының морфологиясы. Минералдарды жүйелеуінің негізі
Минералдар және олардың агрегаттарының морфологиясы. Минералдарды жүйелеуінің негізі Презентация по Химии "Теория химического строения органических веществ" - скачать смотреть
Презентация по Химии "Теория химического строения органических веществ" - скачать смотреть  Оборотні і необоротні реакції. Хімічна рівновага
Оборотні і необоротні реакції. Хімічна рівновага Синтез ультрадисперсного мела для различных эффективных использований
Синтез ультрадисперсного мела для различных эффективных использований Реакционная способность углеводородов
Реакционная способность углеводородов Тіршілік гетерофункционалды қосылыстар
Тіршілік гетерофункционалды қосылыстар Химические свойства оксидов. Тренажер
Химические свойства оксидов. Тренажер Галогены: Хлор, бром, иод
Галогены: Хлор, бром, иод p-элементы 17 группы периодической системы: галогены
p-элементы 17 группы периодической системы: галогены Что объединяет вещества. Классификация твёрдых веществ
Что объединяет вещества. Классификация твёрдых веществ Рідкі кристали
Рідкі кристали Неорганические соединения серы
Неорганические соединения серы Процессы минералообразования
Процессы минералообразования Топливо. Виды топлива
Топливо. Виды топлива Защита от коррозии двигателя, кузова, шасси. Фосфотирование
Защита от коррозии двигателя, кузова, шасси. Фосфотирование Презентация по химии на тему: Бром
Презентация по химии на тему: Бром Количество вещества
Количество вещества Благородные металлы
Благородные металлы Алкены. Олефины, этиленовые углеводороды. (Лекция 5)
Алкены. Олефины, этиленовые углеводороды. (Лекция 5) Презентация по Химии "Окислительно - восстановительные свойства серной кислоты" - скачать смотреть
Презентация по Химии "Окислительно - восстановительные свойства серной кислоты" - скачать смотреть  Водород.Кислоты.Соли
Водород.Кислоты.Соли Заттардың агрегаттық күйлері
Заттардың агрегаттық күйлері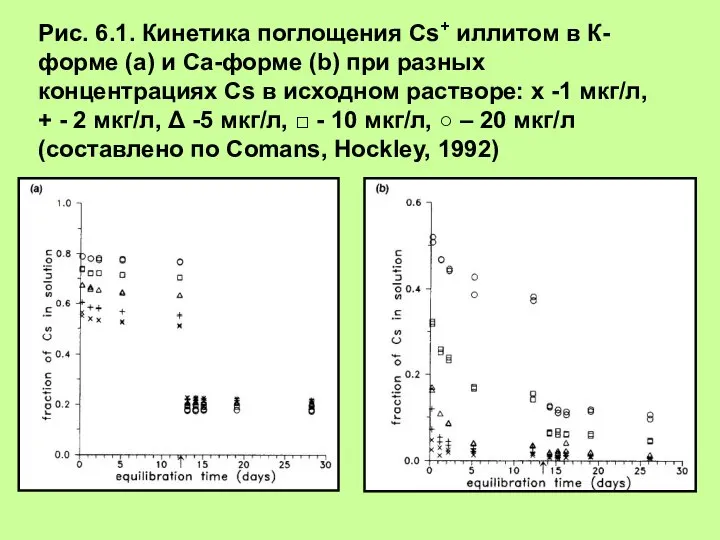 Определение коэффициента селективности при бинарном обмене
Определение коэффициента селективности при бинарном обмене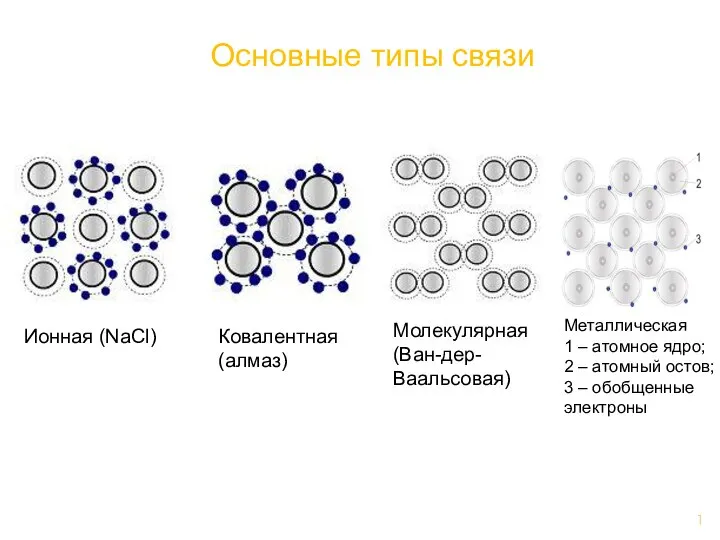 Основные типы связи
Основные типы связи