Содержание
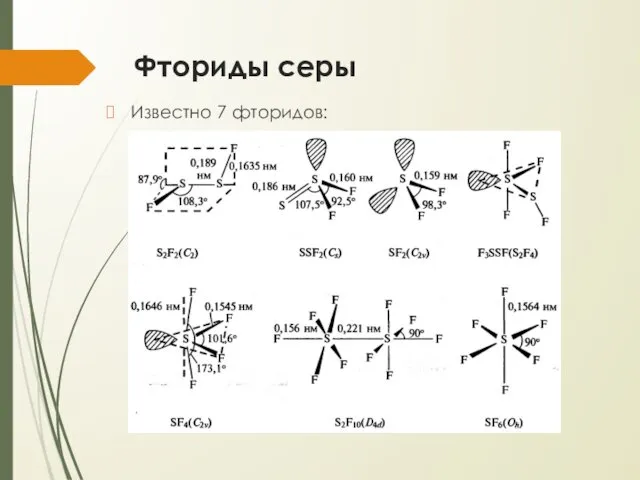
- 2. Фториды серы Известно 7 фторидов:
- 3. Фториды серы. Получение Фторирование хлоридов Из дигалогенидов Фторирование серы Из простых веществ
- 4. Фториды серы. Физические свойства
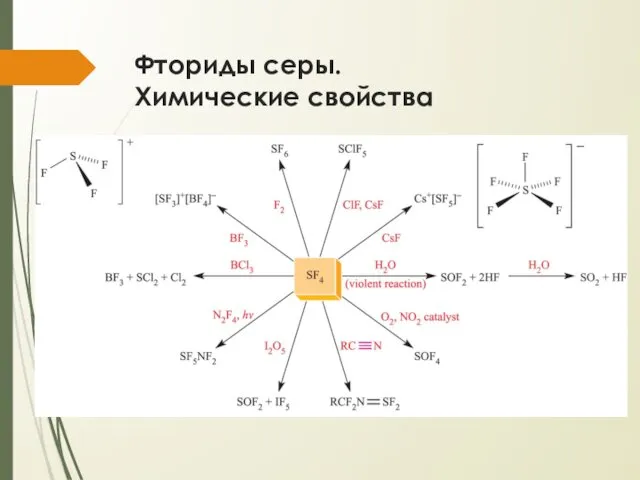
- 5. Фториды серы. Химические свойства
- 6. Фториды серы. Химические свойства Гидролиз Горение в кислороде Диспропорционирование Взаимодействие с металлами Фторирующие агенты
- 8. Хлориды серы. Физические свойства S2Cl2 – золотисто-желтая ядовитая легкокипящая дурно-пахнущая жидкость, т. пл. = -76°С, т.
- 9. Хлориды серы. Химические свойства Гидролиз с образованием H2S, SO2, H2SO3, H2SO4, H2SxO6 Окисляется кислородом
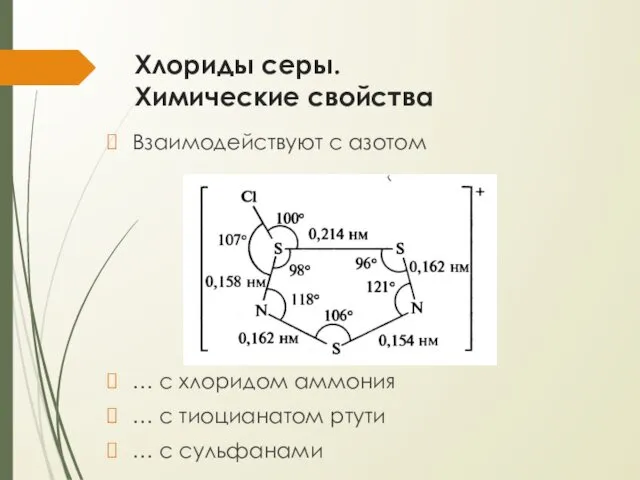
- 10. Хлориды серы. Химические свойства Взаимодействуют с азотом … с хлоридом аммония … с тиоцианатом ртути …
- 11. Бромиды серы. Получение Прямой синтез SBr2 был обнаружен как продукт, изолированный в матрице, когда через смесь
- 12. Бромиды серы. Свойства Очень нестабильны. Разлагаются при комнатной температуре S2Br2 – гранатово-красная жидкость с т. пл.
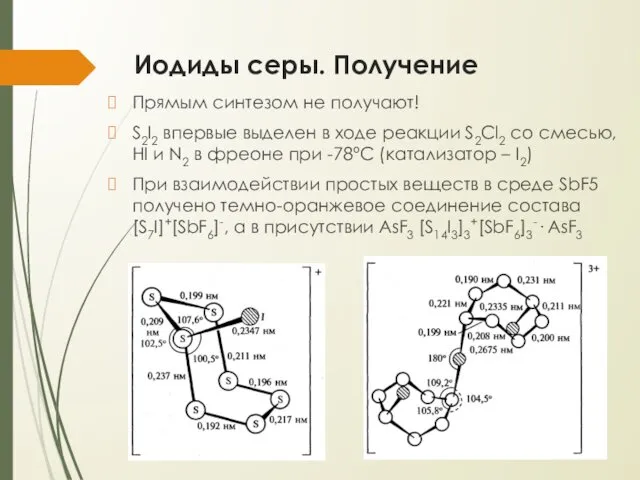
- 13. Иодиды серы. Получение Прямым синтезом не получают! S2I2 впервые выделен в ходе реакции S2Cl2 со смесью,
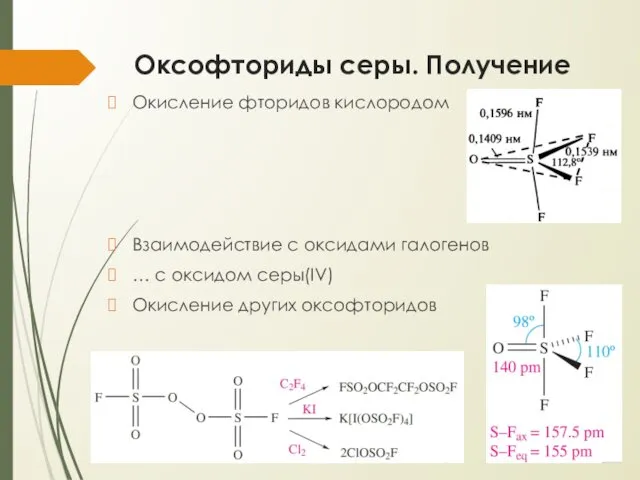
- 14. Оксофториды серы. Получение Окисление фторидов кислородом Взаимодействие с оксидами галогенов … с оксидом серы(IV) Окисление других
- 15. Оксохлориды серы. Получение Окисление хлоридов Хлорирование оксидов
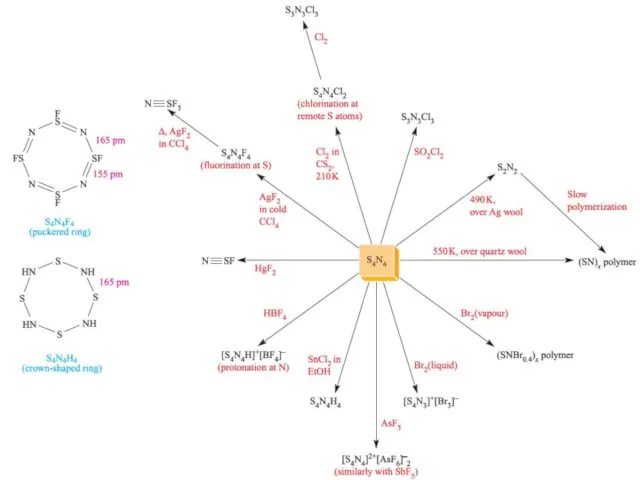
- 16. Нитрид серы. Получение Взаимодействие хлоридов с аммиаком и хлоридом аммония Растворение серы в жидком аммиаке
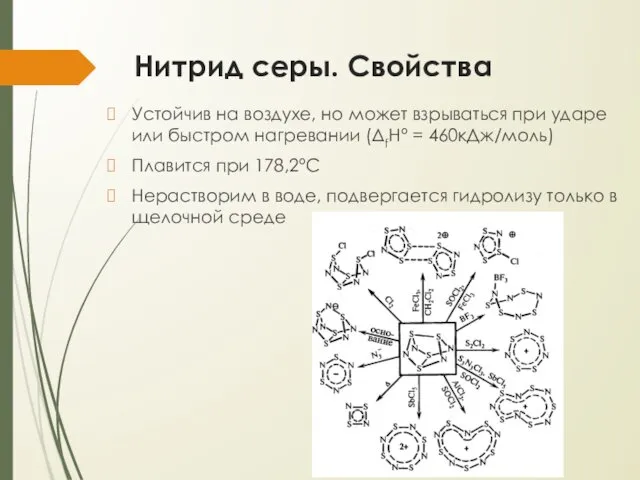
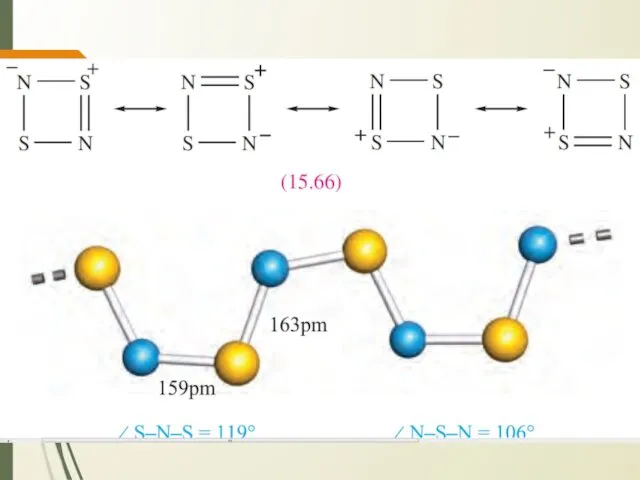
- 17. Нитрид серы. Свойства Устойчив на воздухе, но может взрываться при ударе или быстром нагревании (ΔfH° =
- 20. Катионы серы
- 21. Пероксосерные кислоты Получаются при взаимодействии хлорсульфоновой кислоты с пероксидом водорода … при электролизе раствора серной кислоты
- 22. Тиосерная кислота В водной среде быстро разлагается до серы, SO2, H2S, H2Sn, H2SO4 и т. д.
- 24. Скачать презентацию













 Этанол (этиловый спирт)
Этанол (этиловый спирт) Кометика Liv Delano - презентация_
Кометика Liv Delano - презентация_ Хемосинтез. Автотрофное питание
Хемосинтез. Автотрофное питание Сложные эфиры в жизни человека
Сложные эфиры в жизни человека Вода. Физические и химические свойства воды
Вода. Физические и химические свойства воды Углеводы. 10 класс
Углеводы. 10 класс Презентация Свойства черных и цветных металлов
Презентация Свойства черных и цветных металлов  Количество вещества. Молярная масса. Задачи
Количество вещества. Молярная масса. Задачи Растворы. Гетерогенные равновесия растворов с осадком
Растворы. Гетерогенные равновесия растворов с осадком Тема урока "Основания" - презентация_
Тема урока "Основания" - презентация_ “ КОРОЗІЯ МЕТАЛІВ. ЗАХИСТ ВІД КОРОЗІЇ ” Підготував: Учень 10-А класу ЗОШ №25 м. Луцька Матвійчук Роман
“ КОРОЗІЯ МЕТАЛІВ. ЗАХИСТ ВІД КОРОЗІЇ ” Підготував: Учень 10-А класу ЗОШ №25 м. Луцька Матвійчук Роман  Хімічні добавки. Е-числа
Хімічні добавки. Е-числа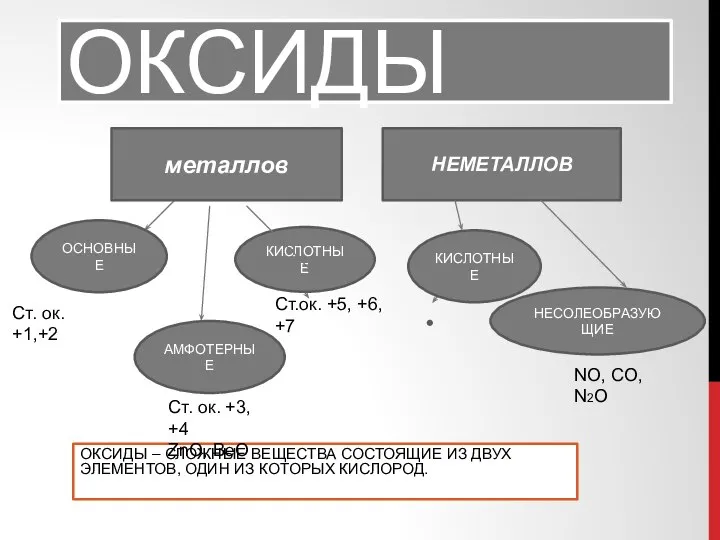 Оксиды
Оксиды Вуглеводи, як компонент їжі. Їхня роль в організмі людини
Вуглеводи, як компонент їжі. Їхня роль в організмі людини Тема: Липиды. Лекция № 2 для студентов 2 курса
Тема: Липиды. Лекция № 2 для студентов 2 курса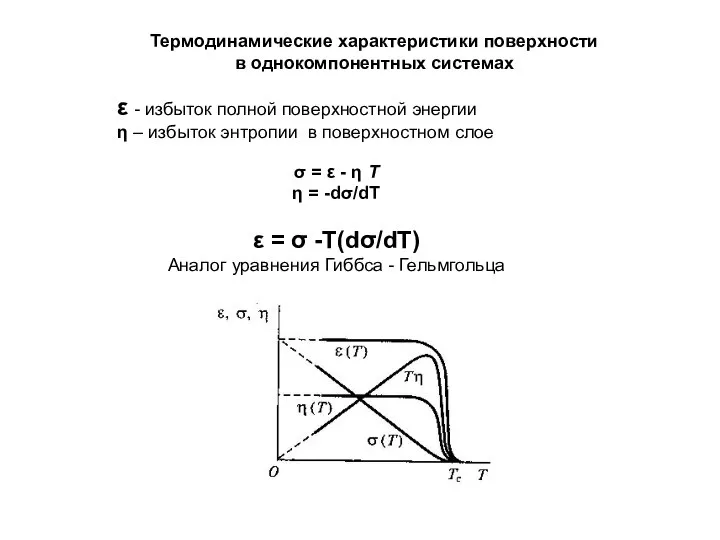 Презентация по Химии "Термодинамические характеристики поверхности" - скачать смотреть
Презентация по Химии "Термодинамические характеристики поверхности" - скачать смотреть  Строение электронных оболочек атомов
Строение электронных оболочек атомов Тотықтырғыштар
Тотықтырғыштар Производная в химии
Производная в химии Классификация кислот
Классификация кислот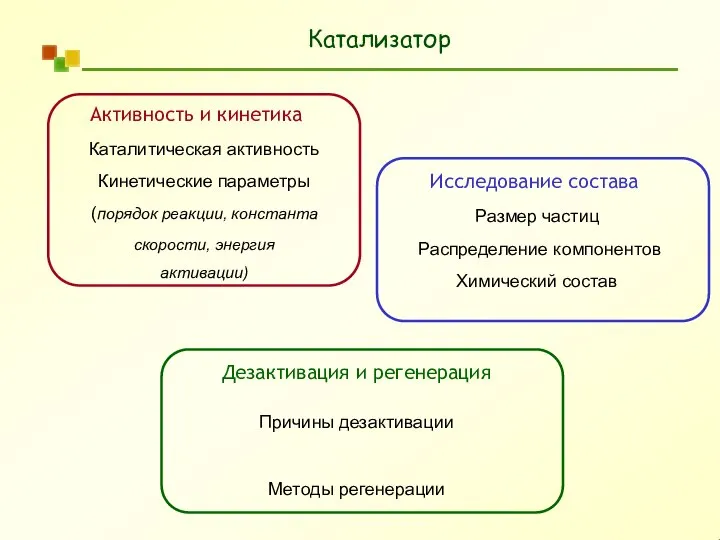 Катализатор. Анализ кинетических данных
Катализатор. Анализ кинетических данных Важнейшие классы неорганических соединений
Важнейшие классы неорганических соединений Биотрансформация чужеродных соединений в организме. (Лекция 5)
Биотрансформация чужеродных соединений в организме. (Лекция 5) Презентация по Химии "Ферменты. Роль и функции" - скачать смотреть
Презентация по Химии "Ферменты. Роль и функции" - скачать смотреть  Краткая история химии
Краткая история химии Презентация по Химии "Дмитро Менделєєв" - скачать смотреть бесплатно
Презентация по Химии "Дмитро Менделєєв" - скачать смотреть бесплатно Методы разделения и концентрирования
Методы разделения и концентрирования Л3.12 Композицитонные материалы
Л3.12 Композицитонные материалы