Содержание
- 2. Неон история Неон открыли в июне 1898 года английские химики Уильям Рамзай и Морис Траверс[4]. Они
- 3. Название происходит от греч. νέος — новый. Существует легенда, согласно которой название элементу дал тринадцатилетний сын
- 4. Физические свойства Благородные газы — бесцветные одноатомные газы без вкуса и запаха. Инертные газы обладают более
- 5. Химические свойства Все благородные газы имеют завершенную электронную оболочку, поэтому они химически инертны. Химическая инертность неона
- 7. Скачать презентацию
Слайд 2
Неон история
Неон открыли в июне 1898 года английские химики Уильям Рамзай и Морис Траверс[4]. Они выделили
Неон история
Неон открыли в июне 1898 года английские химики Уильям Рамзай и Морис Траверс[4]. Они выделили
этот инертный газ «методом исключения» после того, как кислород, азот и все более тяжёлые компоненты воздуха были сжижены. Элементу дали незамысловатое название «неон», что в переводе с греческого означает «новый». В декабре 1910 года французский изобретатель Жорж Клод создал газоразрядную лампу, заполненную неоном.
Слайд 3
Название происходит от греч. νέος — новый.
Существует легенда, согласно которой название элементу дал тринадцатилетний
Название происходит от греч. νέος — новый.
Существует легенда, согласно которой название элементу дал тринадцатилетний
сын Рамзая — Вилли, который спросил у отца, как тот собирается назвать новый газ, заметив при этом, что хотел бы дать ему имя novum (лат. — новый). Его отцу понравилась эта идея, однако он посчитал, что название neon, образованное от греческого синонима, будет звучать лучше[5].
Слайд 4
Физические свойства
Благородные газы — бесцветные одноатомные газы без вкуса и запаха.
Инертные газы
Физические свойства
Благородные газы — бесцветные одноатомные газы без вкуса и запаха.
Инертные газы
обладают более высокой электропроводностью по сравнению с другими газами и при прохождении через них тока ярко светятся, в частности неон огненно-красным светом, так как самые яркие его линии лежат в красной части спектра.
Эмиссионный спектр неона (слева направо: от ультрафиолетовых до инфракрасных линий. Линии, находящиеся в невидимых глазом участках спектра, изображены белым цветом).
Насыщенность внешних электронных оболочек атомов инертных газов обусловливает более низкие точки сжижения и отвердевания, чем у других газов с близкими молекулярными массами.
Эмиссионный спектр неона (слева направо: от ультрафиолетовых до инфракрасных линий. Линии, находящиеся в невидимых глазом участках спектра, изображены белым цветом).
Насыщенность внешних электронных оболочек атомов инертных газов обусловливает более низкие точки сжижения и отвердевания, чем у других газов с близкими молекулярными массами.
Слайд 5
Химические свойства
Все благородные газы имеют завершенную электронную оболочку, поэтому они химически инертны.
Химические свойства
Все благородные газы имеют завершенную электронную оболочку, поэтому они химически инертны.
Химическая инертность неона исключительна, в этом с ним может конкурировать только гелий. Пока не получено ни одного его валентного соединения. Даже так называемые клатратные соединения неона с водой (Ne·6Н2О), гидрохиноном и другими веществами (подобные соединения тяжелых благородных газов — радона, ксенона, криптона и даже аргона — широко известны) получить и сохранить очень трудно.
Однако, с помощью методов оптической спектроскопии и масс-спектрометрии установлено существование ионов Ne+, (NeAr)+, (NeH)+, и (HeNe)+.
Однако, с помощью методов оптической спектроскопии и масс-спектрометрии установлено существование ионов Ne+, (NeAr)+, (NeH)+, и (HeNe)+.
- Предыдущая
Численность и воспроизводство населения мираСледующая -
Растительный и животный мир Южной Америки



 Обзор основных методов исследования супрамолекулярных объектов
Обзор основных методов исследования супрамолекулярных объектов Презентация по Химии "Многоатомные спирты" - скачать смотреть
Презентация по Химии "Многоатомные спирты" - скачать смотреть  Родючість ґрунтів , можливості її регулювання. Учень 9-Г класу Юрчак Владислав Керівник Садовська Т.Я.
Родючість ґрунтів , можливості її регулювання. Учень 9-Г класу Юрчак Владислав Керівник Садовська Т.Я. Симметрия в химии. Кристаллы
Симметрия в химии. Кристаллы Количественное определение лекарственных средств
Количественное определение лекарственных средств Электронные конфигурации атомов
Электронные конфигурации атомов Презентація З хімії На тему : ” Майбутнє альтернативного палива” Виконала учениця 11-А класу Твердохліб Анжеліка
Презентація З хімії На тему : ” Майбутнє альтернативного палива” Виконала учениця 11-А класу Твердохліб Анжеліка  Кислоты органические и неорганические.
Кислоты органические и неорганические. Синтетические моющие средства.(СМС) Подготовила Живулько Елена.
Синтетические моющие средства.(СМС) Подготовила Живулько Елена.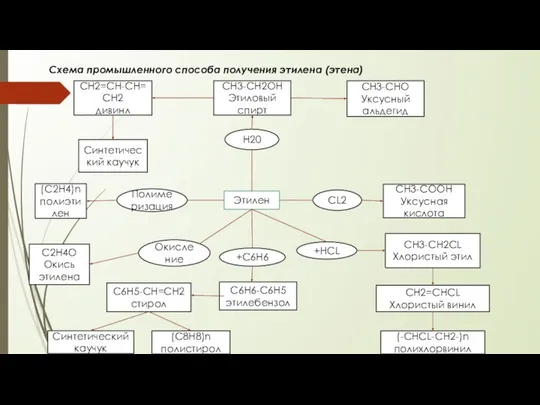 Промышленній способ получения этилена (этена)
Промышленній способ получения этилена (этена) Сложные эфиры
Сложные эфиры Растворы. Способы выражения концентрации растворенного вещества
Растворы. Способы выражения концентрации растворенного вещества Титани органічної хімії
Титани органічної хімії Энергетика химических процессов
Энергетика химических процессов Презентация по химии Химические уравнения Реакции обмена
Презентация по химии Химические уравнения Реакции обмена  Выращивание кристаллов в домашних условиях
Выращивание кристаллов в домашних условиях Неметаллы. Обобщение. Открытый урок
Неметаллы. Обобщение. Открытый урок Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Биогеохимия Оренбургской области
Биогеохимия Оренбургской области Химия элементов VIA группы. Сера
Химия элементов VIA группы. Сера Кремнийорганическая гипотеза
Кремнийорганическая гипотеза Неметаллы. Положение неметаллов в ПСХЭ
Неметаллы. Положение неметаллов в ПСХЭ Полифункциональды (гетерофункциональды) биоорганикалық қосылыстар: оксиқышқылдар, альдегидо- және кетоқышқылдар
Полифункциональды (гетерофункциональды) биоорганикалық қосылыстар: оксиқышқылдар, альдегидо- және кетоқышқылдар - Это оружие массового поражения, действие которого основано на токсических свойствах химических веществ. - Это оружие массового
- Это оружие массового поражения, действие которого основано на токсических свойствах химических веществ. - Это оружие массового  Задачи по теме Энергетический обмен
Задачи по теме Энергетический обмен Горение паро-газо-воздушного облака
Горение паро-газо-воздушного облака Ковалентная полярная связь
Ковалентная полярная связь Нітратна кислота. Нітрати Підготувала:Рибальчук Вікторія
Нітратна кислота. Нітрати Підготувала:Рибальчук Вікторія