Содержание
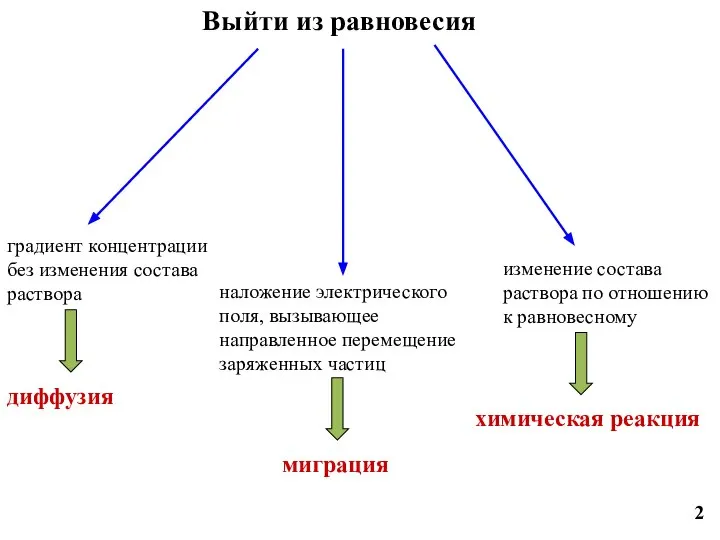
- 2. Выйти из равновесия градиент концентрации без изменения состава раствора диффузия наложение электрического поля, вызывающее направленное перемещение
- 3. Диффузия градиент концентрации Движение ионов в растворе происходит по принципу прыжка с одного места в растворителе
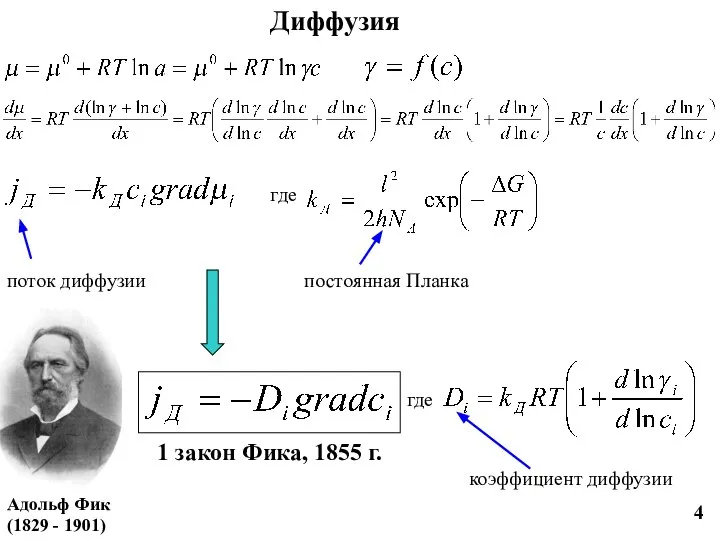
- 4. 4 Диффузия поток диффузии где постоянная Планка 1 закон Фика, 1855 г. где коэффициент диффузии Адольф
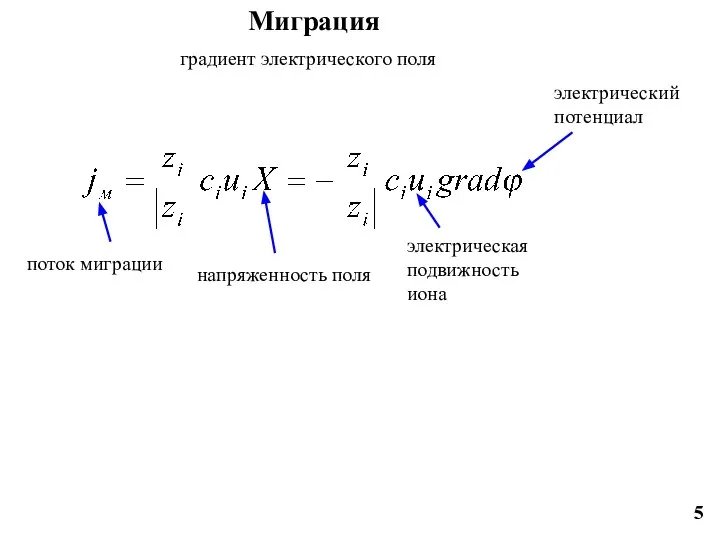
- 5. 5 Миграция градиент электрического поля поток миграции напряженность поля электрическая подвижность иона электрический потенциал
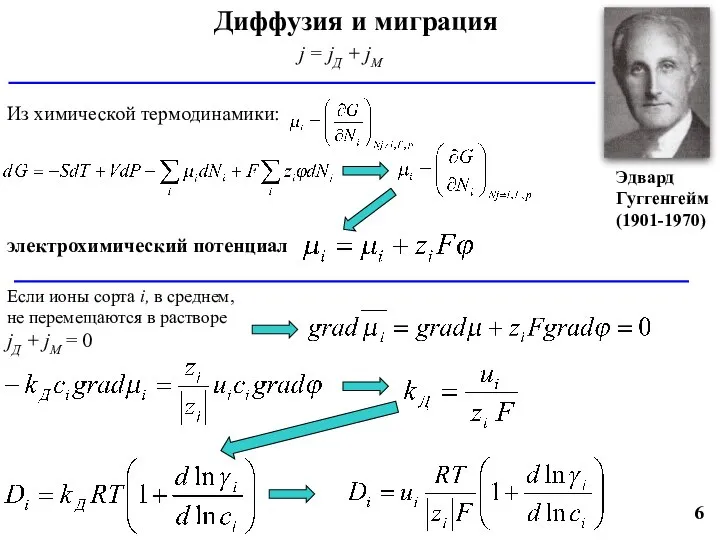
- 6. электрохимический потенциал 6 Диффузия и миграция j = jД + jМ Если ионы сорта i, в
- 7. 7 Уравнение Нернста-Эйнштейна Для идеального раствора ci → 0, γi → 1, Di=Di0, ui=ui0 Уравнение Нернста-Эйнштейна
- 8. R - + I I - удельная электропроводность Электропроводность ρ – удельное сопротивление; l – длина
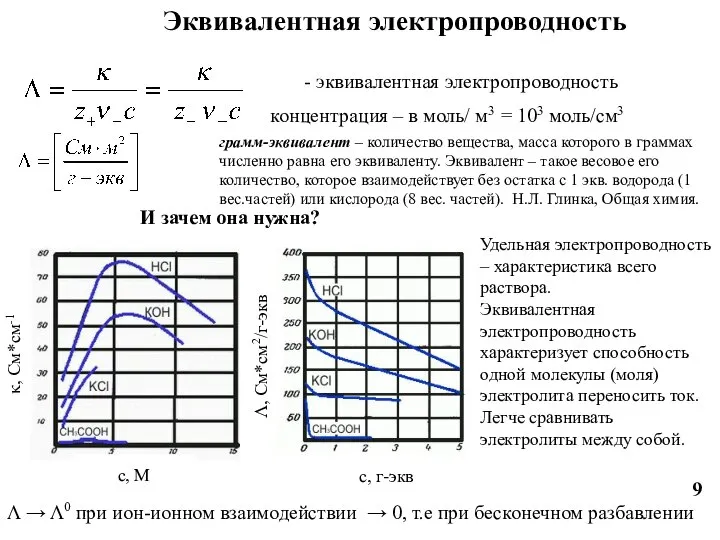
- 9. - эквивалентная электропроводность грамм-эквивалент – количество вещества, масса которого в граммах численно равна его эквиваленту. Эквивалент
- 10. Молярная электропроводность разбавленных водных растворов электролитов при 25 °С Для диапазона С = 0,001 – 0,1
- 11. α - степень диссоциации λ+ , λ− - ионные электропроводности или подвижности ионов В переносе тока
- 12. - если в растворе несколько электролитов Электрическое число переноса - доля тока, создаваемого ионами данного вида
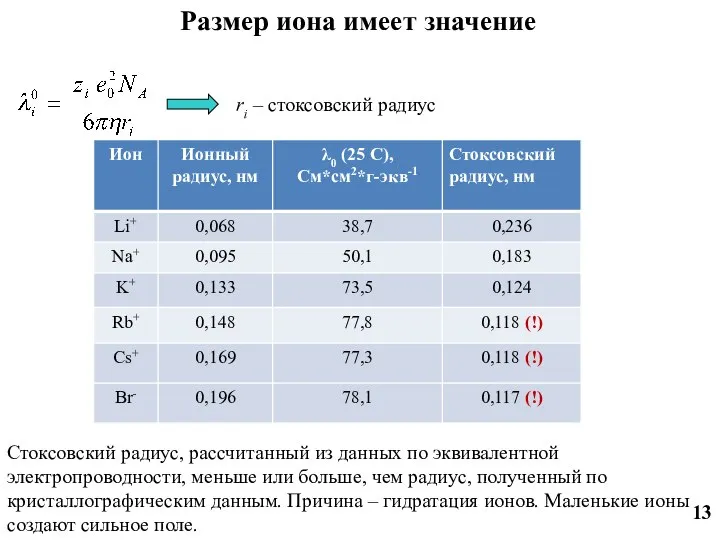
- 13. - cкороcть движения шарика радиусом r под действием силы P в среде вязкостью η. Из уравнения
- 14. Стоксовский радиус, рассчитанный из данных по эквивалентной электропроводности, меньше или больше, чем радиус, полученный по кристаллографическим
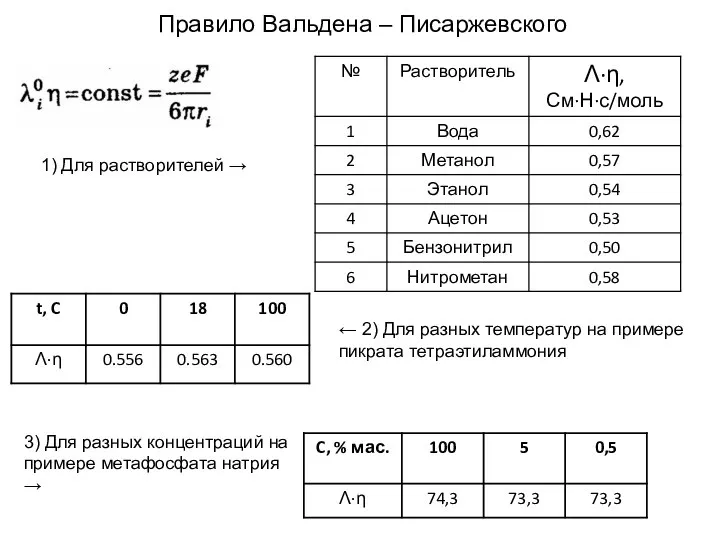
- 15. Правило Вальдена – Писаржевского 1) Для растворителей → ← 2) Для разных температур на примере пикрата
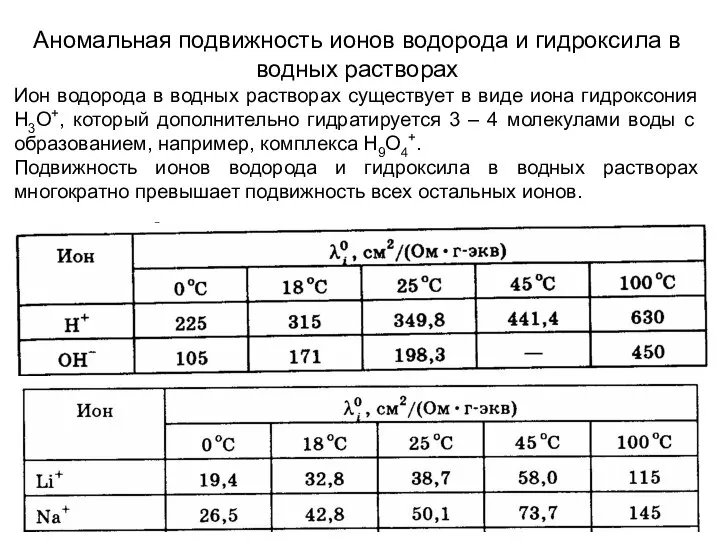
- 17. Аномальная подвижность ионов водорода и гидроксила в водных растворах Ион водорода в водных растворах существует в
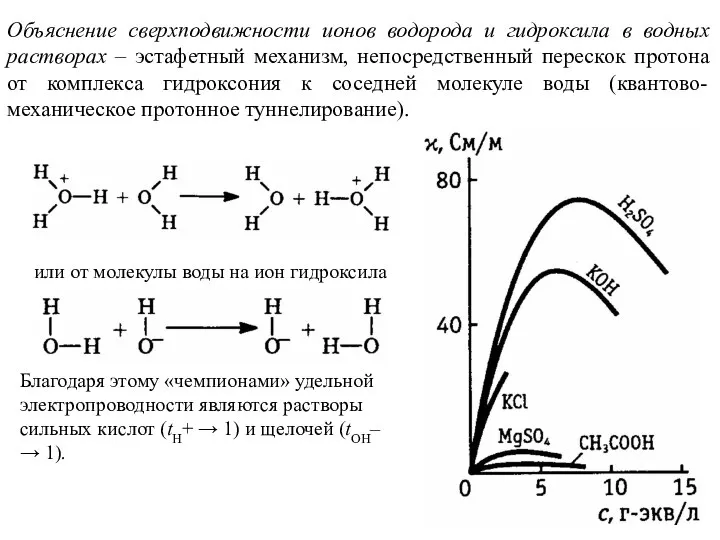
- 18. Объяснение сверхподвижности ионов водорода и гидроксила в водных растворах – эстафетный механизм, непосредственный перескок протона от
- 19. Центральный ион и ионная атмосфера заряжены противоположно. Ионная атмосфера движется навстречу центральному иону, движение которого, соответственно,
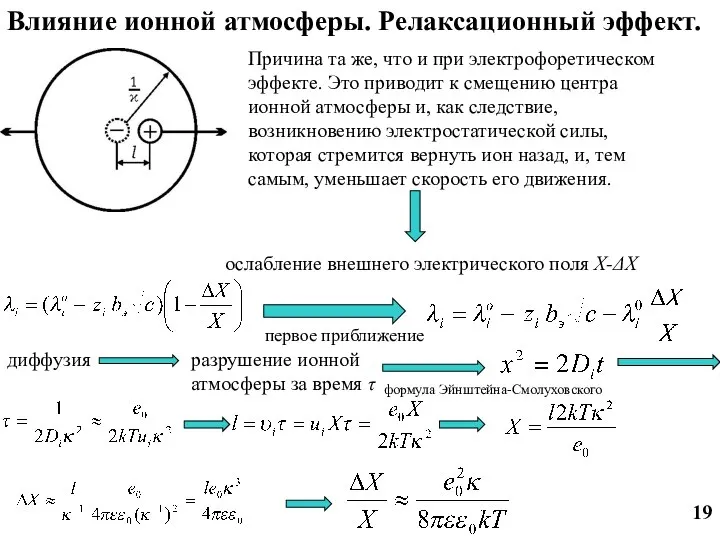
- 20. Причина та же, что и при электрофоретическом эффекте. Это приводит к смещению центра ионной атмосферы и,
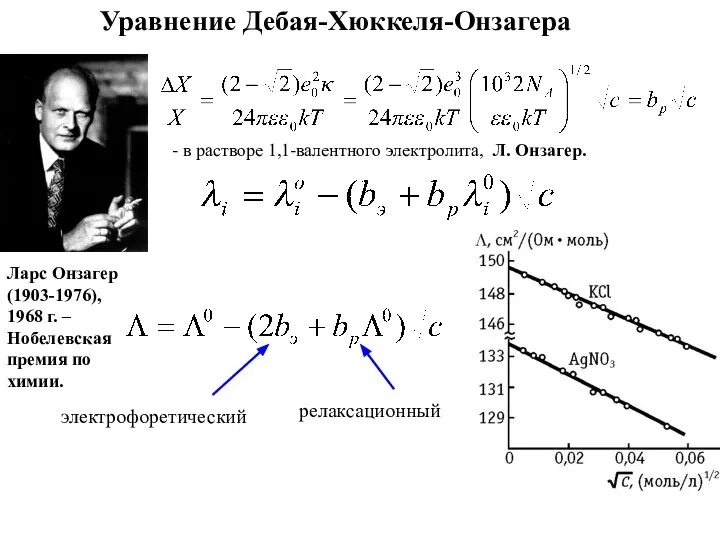
- 21. Уравнение Дебая-Хюккеля-Онзагера Ларс Онзагер (1903-1976), 1968 г. – Нобелевская премия по химии. - в растворе 1,1-валентного
- 22. Lars Onsager Электропроводность. Теория vs. эксперимент 20 Trans. Faraday Soc., 1927, 23, 341-349
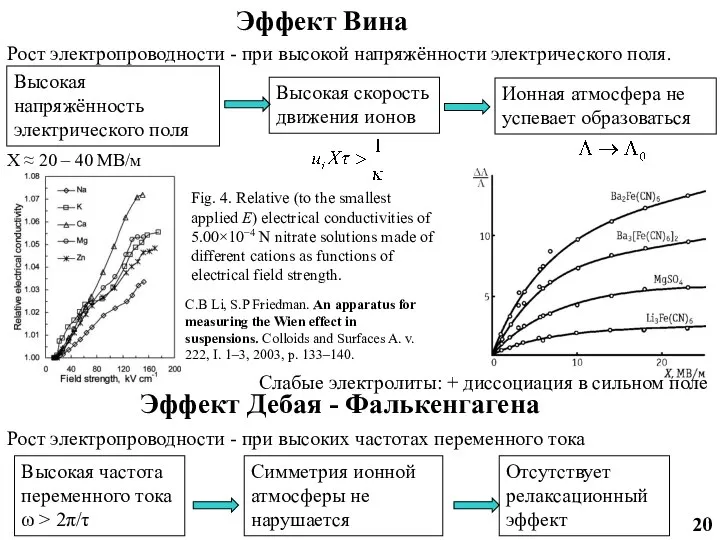
- 23. Слабые электролиты: + диссоциация в сильном поле Эффект Вина Рост электропроводности - при высокой напряжённости электрического
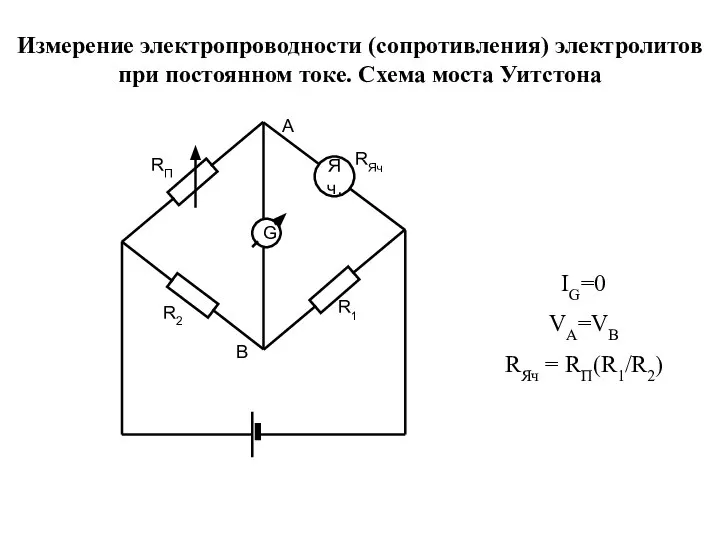
- 24. IG=0 VA=VB RЯч = RП(R1/R2) Измерение электропроводности (сопротивления) электролитов при постоянном токе. Схема моста Уитстона
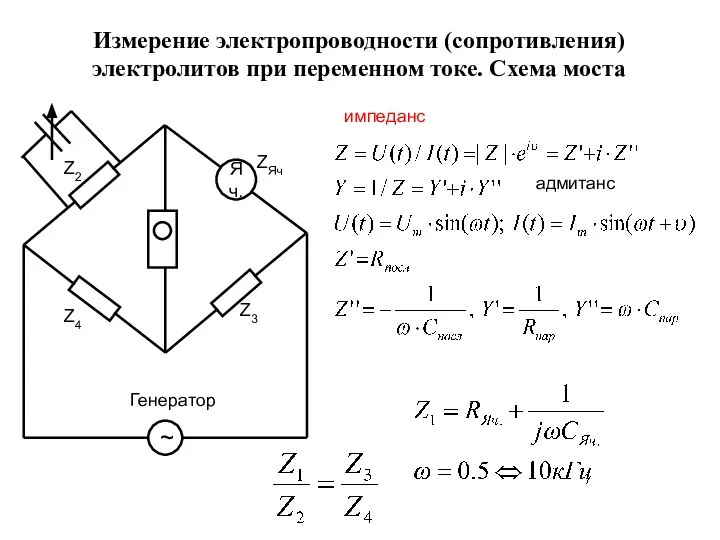
- 25. Измерение электропроводности (сопротивления) электролитов при переменном токе. Схема моста импеданс адмитанс
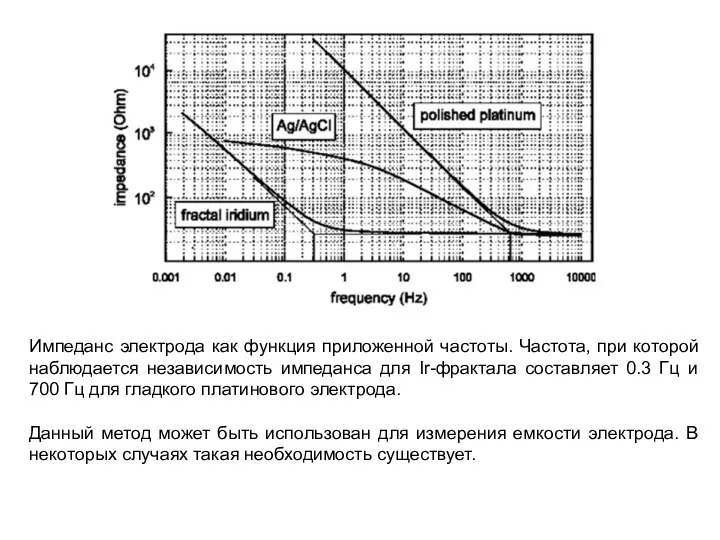
- 26. Импеданс электрода как функция приложенной частоты. Частота, при которой наблюдается независимость импеданса для Ir-фрактала составляет 0.3
- 27. Метод кондуктометрии Основное уравнение: æ= (1/R)·K где æ - удельная электропроводность раствора, R - сопротивление, К
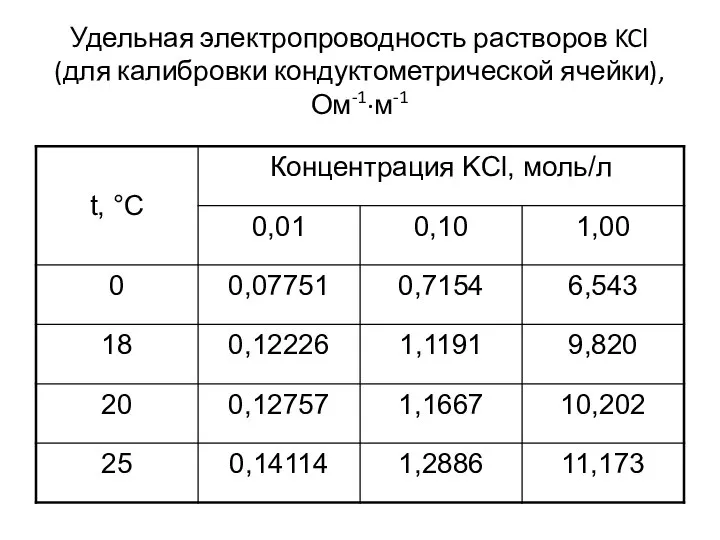
- 28. Удельная электропроводность растворов KCl (для калибровки кондуктометрической ячейки), Ом-1·м-1
- 29. Примеры применения метода кондуктометрии Определение удельной электропроводности воды и растворителей Определение константы диссоциации слабого электролита Определение
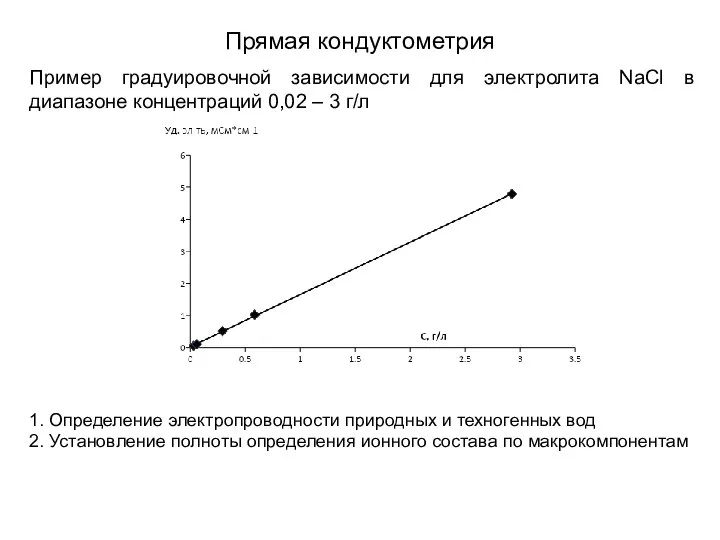
- 30. Прямая кондуктометрия 1. Определение электропроводности природных и техногенных вод 2. Установление полноты определения ионного состава по
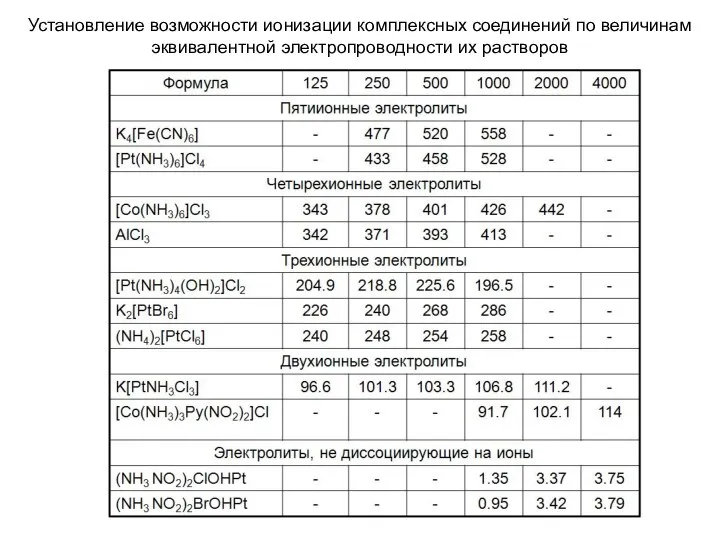
- 31. Установление возможности ионизации комплексных соединений по величинам эквивалентной электропроводности их растворов
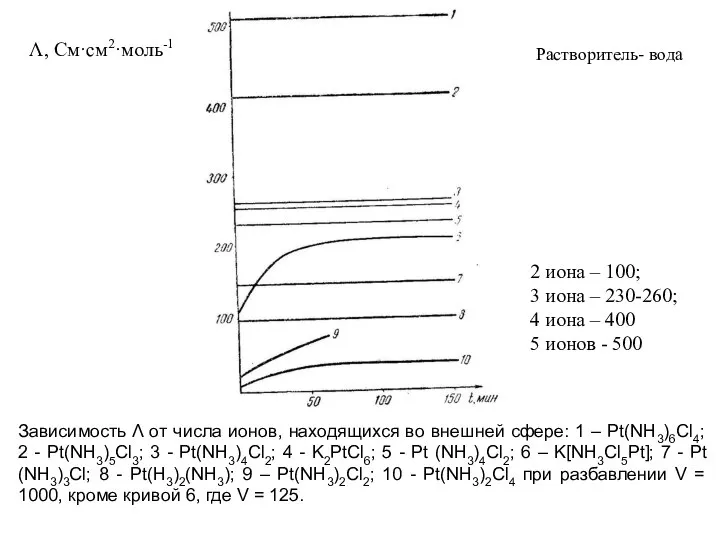
- 32. Λ, См·см2·моль-1 Зависимость Λ от числа ионов, находящихся во внешней сфере: 1 – Pt(NH3)6Cl4; 2 -
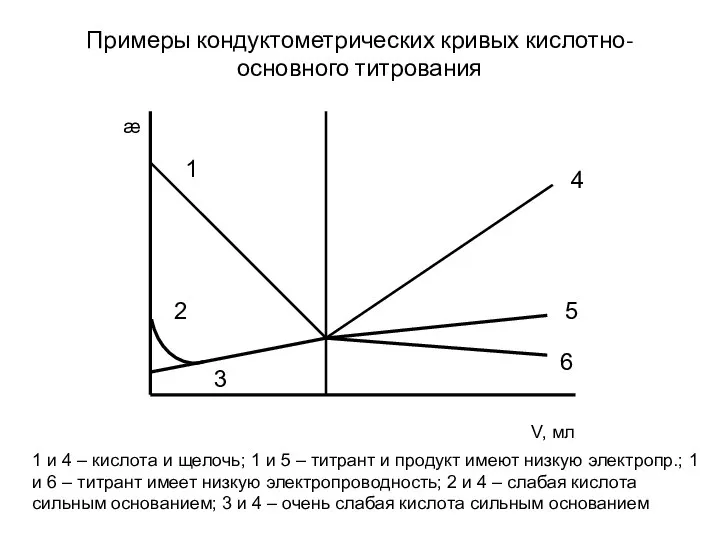
- 33. Примеры кондуктометрических кривых кислотно-основного титрования 1 и 4 – кислота и щелочь; 1 и 5 –
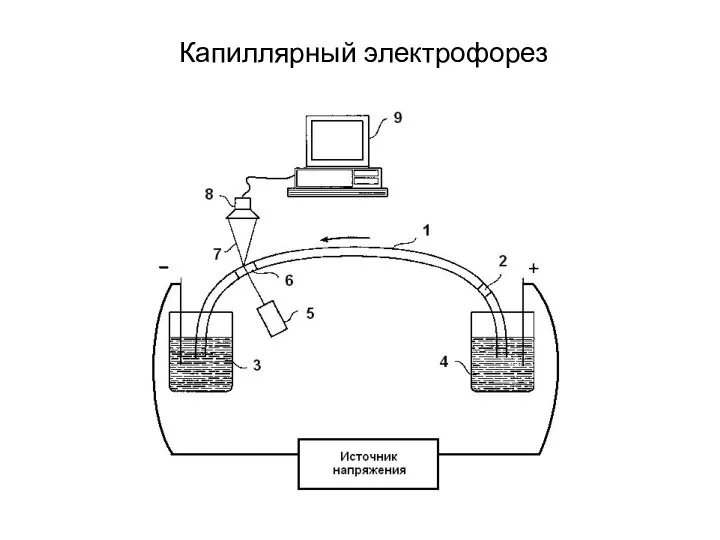
- 34. Капиллярный электрофорез
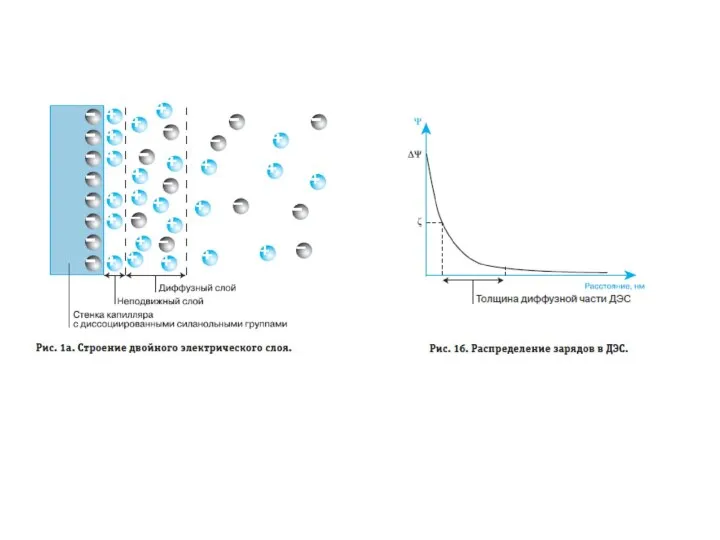
- 35. Схема движения потоков в капилляре
- 38. Скачать презентацию












 Сера и ее важнейшие соединения 16S 1s22s22p63s23p4 (р- элемент) S8 – ромбическая сера (наиболее устойчивая аллотропная модификация серы;
Сера и ее важнейшие соединения 16S 1s22s22p63s23p4 (р- элемент) S8 – ромбическая сера (наиболее устойчивая аллотропная модификация серы; Оцтова кислота Презентація підготовлена ученицею 9 класу Лук'яновою Іриною
Оцтова кислота Презентація підготовлена ученицею 9 класу Лук'яновою Іриною  Основы коллоидной химии и коагуляции загрязняющих веществ в процессах очистки воды
Основы коллоидной химии и коагуляции загрязняющих веществ в процессах очистки воды Характеристика ядов, изолируемых минерализацией в клинической фармации
Характеристика ядов, изолируемых минерализацией в клинической фармации Технология кварцевого стекла
Технология кварцевого стекла Физическая химия. Химическая термодинамика
Физическая химия. Химическая термодинамика Метод БЭТ. Методы и средства измерений сорбционных свойств наноструктурированных материалов
Метод БЭТ. Методы и средства измерений сорбционных свойств наноструктурированных материалов Вклад М.В. Ломоносова в развитие химии
Вклад М.В. Ломоносова в развитие химии Cвойства цементного камня с введением кольматирующей добавки системы «Пенетрон-Адмикс»
Cвойства цементного камня с введением кольматирующей добавки системы «Пенетрон-Адмикс» Окислительные свойства азотной кислоты
Окислительные свойства азотной кислоты Органічні сполуки в побуті
Органічні сполуки в побуті Эвапориты. Химические осадки из ионных растворов
Эвапориты. Химические осадки из ионных растворов Душистые вещества животного и растительного происхождения
Душистые вещества животного и растительного происхождения Химические предприятия Саратовской области
Химические предприятия Саратовской области вогнегасники Принцип дії вогнегасника
вогнегасники Принцип дії вогнегасника  Алкадиены. Классификация алкадиенов
Алкадиены. Классификация алкадиенов Периодический закон и периодическая система элементов Д.И. Менделеева
Периодический закон и периодическая система элементов Д.И. Менделеева КУБАНСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ КАФЕДРА ФУНДАМЕНТАЛЬНОЙ И КЛИНИЧЕСКОЙ БИОХИМИИ Лекция по теме: «Обмен липид
КУБАНСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ КАФЕДРА ФУНДАМЕНТАЛЬНОЙ И КЛИНИЧЕСКОЙ БИОХИМИИ Лекция по теме: «Обмен липид Методы упрочнения металлических сплавов. Тема 2.3
Методы упрочнения металлических сплавов. Тема 2.3 Строение атома
Строение атома Электрические свойства дисперсных систем. (Лекция 5)
Электрические свойства дисперсных систем. (Лекция 5) Водород, нахождение в природе. Получение водорода и его физические свойства
Водород, нахождение в природе. Получение водорода и его физические свойства Таза зат және қоспа. Қоспаларды бөлу әдістері. Қосылыс Рure substances and mixtures . Мethods for separating mixtures. Compound
Таза зат және қоспа. Қоспаларды бөлу әдістері. Қосылыс Рure substances and mixtures . Мethods for separating mixtures. Compound Презентация по Химии "Сильнодіючі отруйні речовини: поняття та класифікація." - скачать смотреть бесплатно
Презентация по Химии "Сильнодіючі отруйні речовини: поняття та класифікація." - скачать смотреть бесплатно Введение в органическую химию
Введение в органическую химию Кристаллография. История развития
Кристаллография. История развития Этот удивительный кремний Без любопытства и фантазии наука невозможна! А. Эйнштейн
Этот удивительный кремний Без любопытства и фантазии наука невозможна! А. Эйнштейн Урок №5 8 класс по учебнику О.С.Габриеляна Учитель химии I категории МОУ СОШ №6 Нягани ХМАО-Югры Тюменской области Ким Наталья
Урок №5 8 класс по учебнику О.С.Габриеляна Учитель химии I категории МОУ СОШ №6 Нягани ХМАО-Югры Тюменской области Ким Наталья