Содержание
- 2. ФИЗИЧЕСКАЯ ХИМИЯ Химическая термодинамика Химическая кинетика Электрохимия Коллоидная химия и химия поверхностных явлений Квантовая химия ХИМИЧЕСАКАЯ
- 3. ХИМИЧЕСКАЯ ТЕРМОДИНАМИКА Уравнения состояния идеальных газов Законы термодинамики Термодинамические функции состояния системы Химическое равновесие Термодинамика фазовых
- 4. Кудряшева, Н.С. Физическая химия: Учеб. пособие / Н. С. Кудряшева, Л.Г. Бондарева. — Издательство Юрайт, 2011.
- 5. Физическая химия – наука о закономерностях химических процессов и явлений, дающая объяснение на основе фундаментальных положений
- 6. Основные задачи физической химии: Изучение и объяснение основных закономерностей, определяющих направленность химических процессов Изучение скоростей процессов,
- 7. ФИЗИЧЕСКАЯ ХИМИЯ Химическая термодинамика Теоретические методы физики для решения задач физической химии: Термодинамический метод Молекулярно-кинетическая теория
- 8. ФИЗИЧЕСКАЯ ХИМИЯ Химическая термодинамика Теоретические методы физики для решения задач физической химии: Термодинамический метод Молекулярно-кинетическая теория
- 9. ФИЗИЧЕСКАЯ ХИМИЯ Химическая термодинамика Теоретические методы физики для решения задач физической химии: Термодинамический метод Молекулярно-кинетическая теория
- 10. ФИЗИЧЕСКАЯ ХИМИЯ Химическая термодинамика Впервые курс прочитан в 1752 – 1753 гг. М.В. Ломоносовым Первый учебник
- 11. ФИЗИЧЕСКАЯ ХИМИЯ Химическая термодинамика Впервые курс прочитан в 1752 – 1753 гг. М.В. Ломоносовым Первый учебник
- 12. ФИЗИЧЕСКАЯ ХИМИЯ Химическая термодинамика Впервые курс прочитан в 1752 – 1753 гг. М.В. Ломоносовым Первый учебник
- 13. ХИМИЧЕСКАЯ ТЕРМОДИНАМИКА Термодинамика Наука, изучающая переход энергии из одной формы в другую и от одной части
- 14. Термодинамик базируется на ряде положений – первый, второй и третий закон термодинамики. К открытию первого закона
- 15. Термодинамик базируется на ряде положений – первый, второй и третий закон термодинамики. К открытию второго закона
- 16. Термодинамик базируется на ряде положений – первый, второй и третий закон термодинамики. Дальнейшее развитие связано с
- 17. Объект исследования – макроскопическая система. Термодинамикой не рассматривается: - молекулярная структура вещества - характер сил взаимодействия
- 18. Назначение термодинамики: - расчет тепловых балансов при протекании химических и физических процессов, - определение благоприятных условий
- 19. Система – тело или группа тел, мысленно или физически выделенных из окружающей среды. ХИМИЧЕСКАЯ ТЕРМОДИНАМИКА Основные
- 20. Системы делятся на Открытые, Закрытые, Изолированные. ХИМИЧЕСКАЯ ТЕРМОДИНАМИКА Основные понятия Открытой системой называется система, которая может
- 21. Системы делятся на Открытые, Закрытые, Изолированные. ХИМИЧЕСКАЯ ТЕРМОДИНАМИКА Основные понятия Закрытой системой называется система, в которой
- 22. Системы делятся на Открытые, Закрытые, Изолированные. ХИМИЧЕСКАЯ ТЕРМОДИНАМИКА Основные понятия Изолированной системой называется система, объем которой
- 23. Системы делятся на Гомогенные, Гетерогенные. ХИМИЧЕСКАЯ ТЕРМОДИНАМИКА Основные понятия Фаза – часть системы, которая отделена от
- 24. Системы делятся на Гомогенные, Гетерогенные. ХИМИЧЕСКАЯ ТЕРМОДИНАМИКА Основные понятия Система называется гомогенной (однородной), если она состоит
- 25. Системы делятся на Гомогенные, Гетерогенные. ХИМИЧЕСКАЯ ТЕРМОДИНАМИКА Основные понятия Гетерогенная (неоднородная) система обязательно содержит несколько фаз.
- 26. Состояние системы – совокупность всех физических и химических свойств системы. Рассматриваю те свойства, которые могут быть
- 27. Параметры состояния системы связываются между собой соотношением – уравнение состояния системы. f(p, V, T) = 0
- 28. Свойства системы делятся на : экстенсивные и интенсивные. Экстенсивные свойства пропорциональны массе системы ХИМИЧЕСКАЯ ТЕРМОДИНАМИКА Основные
- 29. Свойства системы делятся на : экстенсивные и интенсивные. Интенсивные свойства не зависят от массы системы ХИМИЧЕСКАЯ
- 30. Термодинамические процессы Если при наблюдении за системой происходит изменение хотя бы одного из термодинамических свойств, то
- 31. ХИМИЧЕСКАЯ ТЕРМОДИНАМИКА Основные понятия Процесс, при протекании которого система снова возвращается в исходное состояние, называется круговым
- 32. Равновесное состояние системы такое состояние, которое сохраняется неизменным во времени, причем это состояние не поддерживается каким-либо
- 33. Для описания состояния газ достаточно определить только два термодинамических параметра: P – T; P – V;
- 34. Роберт Бойль (1662г) При постоянной температуре объем, V, постоянной массы данного газа обратно пропорционален его давлению.
- 35. Шарль (1787) Гей-Люссак (1802) При постоянном давлении объем постоянной массы данного газа прямо пропорционален его температуре
- 36. ХИМИЧЕСКАЯ ТЕРМОДИНАМИКА Законы идеального газа: Бойля-Мариатта, Шарля-Гей-Люссака, Авагадро. Амедео Авогадро, 1776 - 1856 А. Авагадро (1811)
- 37. Идеальный газ – математическая модель, в которой предполагается, что потенциальной энергией взаимодействия молекул можно пренебречь Свойства
- 38. ХИМИЧЕСКАЯ ТЕРМОДИНАМИКА Уравнение состояние идеального газа
- 39. V = f(P, T) ХИМИЧЕСКАЯ ТЕРМОДИНАМИКА Уравнение состояние идеального газа PV = k1T V = k2T
- 40. Признаки критического состояния вещества: Критическому состоянию соответствуют давление и температура, при которых газ и жидкость становятся
- 41. ХИМИЧЕСКАЯ ТЕРМОДИНАМИКА Константы, характеризующие критическое состояние Изотермы для изопропана, обнаруживающие существование критической области
- 42. ХИМИЧЕСКАЯ ТЕРМОДИНАМИКА Константы, характеризующие критическое состояние Изотермы для изопропана, обнаруживающие существование критической области
- 43. ХИМИЧЕСКАЯ ТЕРМОДИНАМИКА Константы, характеризующие критическое состояние Определение критического объема системы Соотношение Кальете - Матиаса
- 44. ХИМИЧЕСКАЯ ТЕРМОДИНАМИКА Уравнение Ван-дер-Ваальса
- 45. ХИМИЧЕСКАЯ ТЕРМОДИНАМИКА Уравнение Ван-дер-Ваальса Учет влияния эффективного давления за счет притяжения молекул
- 46. ХИМИЧЕСКАЯ ТЕРМОДИНАМИКА Уравнение Ван-дер-Ваальса Учет уменьшения объема, в котором могут двигаются молекулы
- 47. ХИМИЧЕСКАЯ ТЕРМОДИНАМИКА Уравнение Ван-дер-Ваальса При
- 48. ХИМИЧЕСКАЯ ТЕРМОДИНАМИКА Первый закон термодинамики
- 49. Внутренняя энергия – функция состояния системы. Не зависит от промежуточных стадий процесса, определяется только начальным и
- 50. Измеряется только изменение внутренней энергии В любой неизолированной системе в результате какого-либо процесса происходит изменение энергии.
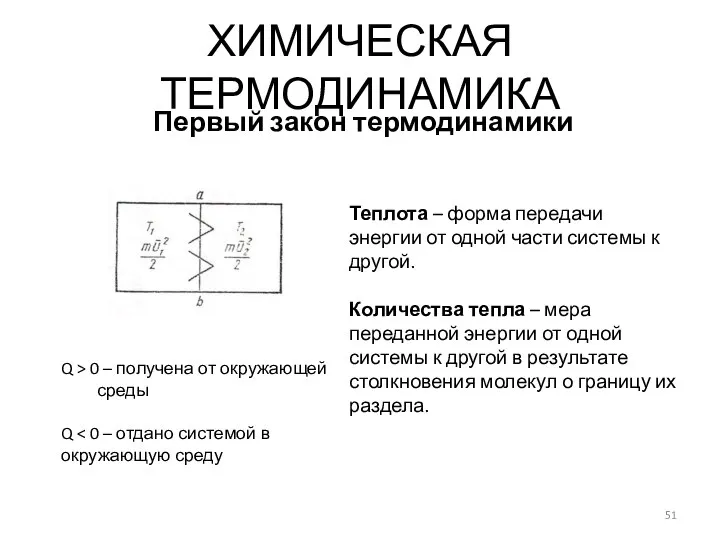
- 51. ХИМИЧЕСКАЯ ТЕРМОДИНАМИКА Первый закон термодинамики Теплота – форма передачи энергии от одной части системы к другой.
- 52. Обмен энергии между системой и внешней средой обуславливается работой, совершаемой системой или над системой. Элементарная работа:
- 53. Передача энергии: Теплота столкновение молекул с поверхность раздела систем в результате хаотичного движения Работа упорядоченного движения
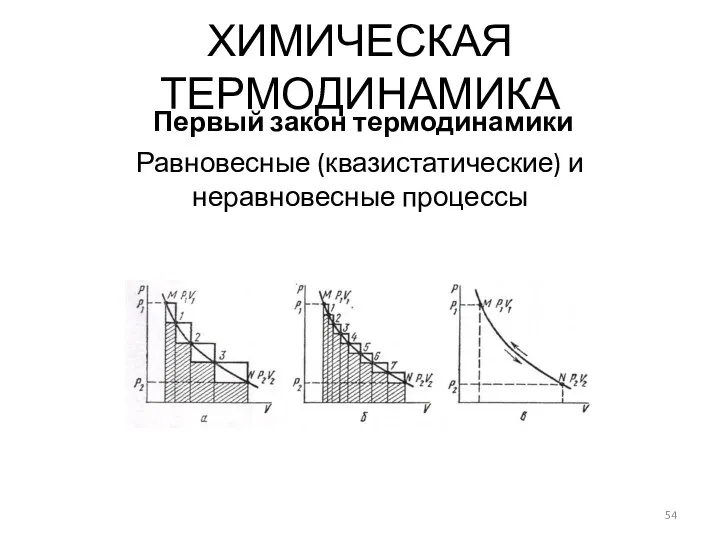
- 54. Равновесные (квазистатические) и неравновесные процессы ХИМИЧЕСКАЯ ТЕРМОДИНАМИКА Первый закон термодинамики
- 55. ХИМИЧЕСКАЯ ТЕРМОДИНАМИКА Первый закон термодинамики При квазистатическом процессе:
- 56. Из закона сохранения энергии следует: Q=∆U + W Для бесконечно малых элементарных процессов: δQ = dU
- 57. Внутренняя энергия изолированной системы есть величина постоянная. ∆U = 0 Если в неизолированной системе протекает процесс,
- 58. Изохорный процесс (V = const) δW = PdV = 0 δQV = dU + PdV =
- 59. ХИМИЧЕСКАЯ ТЕРМОДИНАМИКА Первый закон термодинамики
- 60. При отсутствии немеханической работы: ХИМИЧЕСКАЯ ТЕРМОДИНАМИКА Тепловой эффект. Термохимия. QV = ∆U QP = ∆H Тепловым
- 61. Тепловой эффект процесса не зависит от промежуточных стадий, а определяется лишь начальным и конечным состояниями системы
- 62. Термохимия – раздел химической термодинамики позволяющий рассчитывать тепловые эффекты химических реакций и экспериментально их определять. Основные
- 64. Скачать презентацию



























































 Серная кислота. (9 класс)
Серная кислота. (9 класс) Ароматические углеводороды (Арены)
Ароматические углеводороды (Арены) Atomic number, Mass number and Isotopes
Atomic number, Mass number and Isotopes Ароматические углеводороды
Ароматические углеводороды Каталитикалық крекинг
Каталитикалық крекинг Аттестационная работа. Проектно-исследовательская деятельность учащихся на уроках химии и во внеурочной работе
Аттестационная работа. Проектно-исследовательская деятельность учащихся на уроках химии и во внеурочной работе Синтез и свойства кукурбитурилов
Синтез и свойства кукурбитурилов Характеристика элементов VI-В группы. Хром
Характеристика элементов VI-В группы. Хром Строение атома. Периодичность свойств элементов и их соединений
Строение атома. Периодичность свойств элементов и их соединений Вольфрам және молибден
Вольфрам және молибден КРАХМАЛ и ЦЕЛЛЮЛОЗА (С6Н10О5)n
КРАХМАЛ и ЦЕЛЛЮЛОЗА (С6Н10О5)n  Ш. Мәрҗани исемендәге Комыргуҗа урта мәктәбе Физика укытучысы Шәрәфетдинова Р.З. 2012 ел
Ш. Мәрҗани исемендәге Комыргуҗа урта мәктәбе Физика укытучысы Шәрәфетдинова Р.З. 2012 ел Познаваемость мира. Сведения о клетке. Подготовила ученица 11 класса Шапаренко Екатерина
Познаваемость мира. Сведения о клетке. Подготовила ученица 11 класса Шапаренко Екатерина Химия элементов IVA группы
Химия элементов IVA группы Ионы кальция, как важное звено в нейроцитотоксическом действии кадмия
Ионы кальция, как важное звено в нейроцитотоксическом действии кадмия Органическое топливо. Теплота сгорания топлива
Органическое топливо. Теплота сгорания топлива Химические свойства и получение алканов
Химические свойства и получение алканов Кислород и его применение
Кислород и его применение Кислотно-основное титрование в неводных средах
Кислотно-основное титрование в неводных средах Алюминий және оның қосылыстары
Алюминий және оның қосылыстары Кремний и его соединения
Кремний и его соединения Характеристика металу Ферум
Характеристика металу Ферум Виды присадок к моторному топливу. Керосин
Виды присадок к моторному топливу. Керосин Предмет химии. Вещества и их физические свойства. (8 класс)
Предмет химии. Вещества и их физические свойства. (8 класс)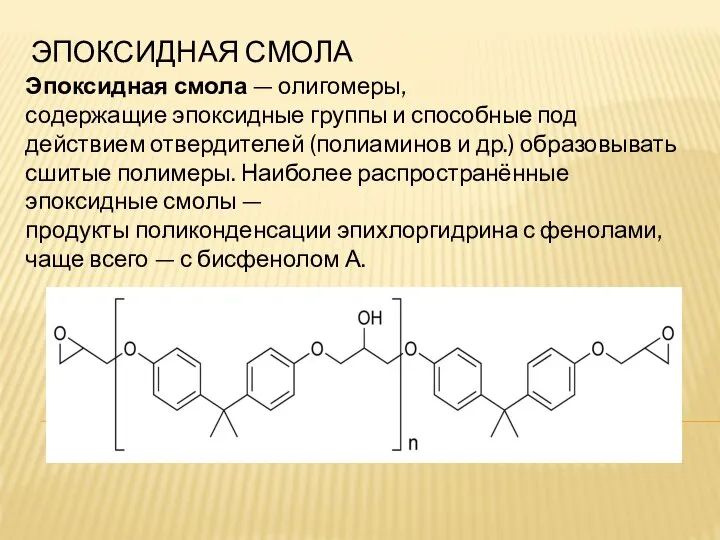 Эпоксидная смола
Эпоксидная смола Материя и цвет. Свет
Материя и цвет. Свет Способы выражения состава раствора. Решение задач
Способы выражения состава раствора. Решение задач Метаболизм источников энергии
Метаболизм источников энергии