Содержание
- 2. Вычислите объем оксида серы (IV), который надо взять для реакции с кислородом, чтобы получить оксид серы
- 3. Характеристика элемента – металла по положению в ПСХЭ Д.И.Менделеева Li B 1. Металлы находятся в I-III
- 4. Изменение металлических свойств в ПСХЭ В группах: металлические свойства усиливаются причина: 1.увеличивается заряд ядра, 2.число электронов
- 5. 4. Соединения металлов Ме С.О. +1, +2 С.О. +3 С.О. +4 и больше Ме2О МеО основные
- 6. 5.Нахождение в природе Самый распространённый Al, затем Fe, Ca, Na, K… Встречаются только в виде соединений,
- 7. Характеристика простых веществ металлов 1. Состав и строение молекул металлов Молекулы Ме – одноатомны. Металлическая связь
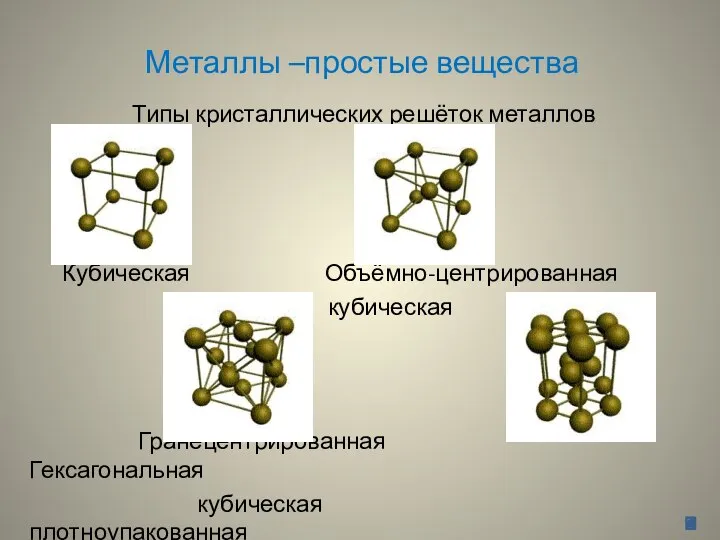
- 8. Металлы –простые вещества Типы кристаллических решёток металлов Кубическая Объёмно-центрированная кубическая Гранецентрированная Гексагональная кубическая плотноупакованная
- 9. Химическая связь в металлах В узлах кристаллической решётки атом-ионы, между которыми свободно перемещаются свободные электроны («электронный
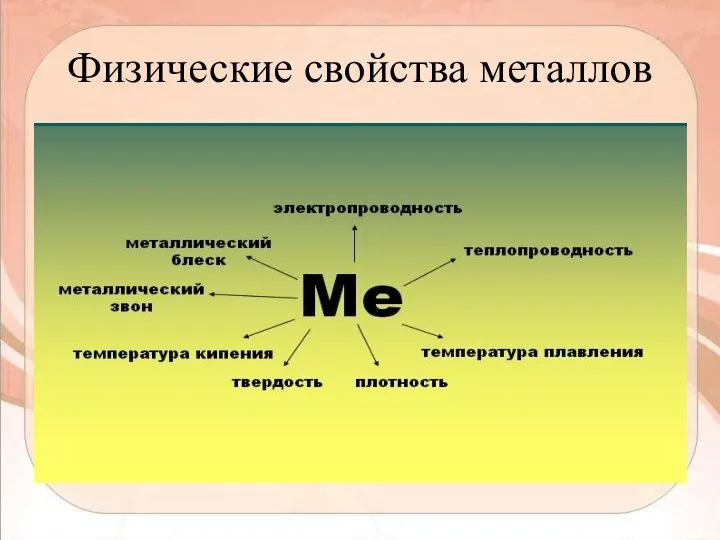
- 10. Физические свойства металлов теплопроводность твёрдость плотность Ме металлический пластичность блеск и ковкость электропроводность
- 11. Физические свойства металлов (продолжение) Физические свойства металлов: пластичность, металлический блеск, теплопроводность и электропро- водность обусловлены наличием
- 12. Металлы - «рекордсмены» W - самый тугоплавкий Ag - самый электропроводный Li - самый лёгкий AI
- 13. Физические свойства металлов
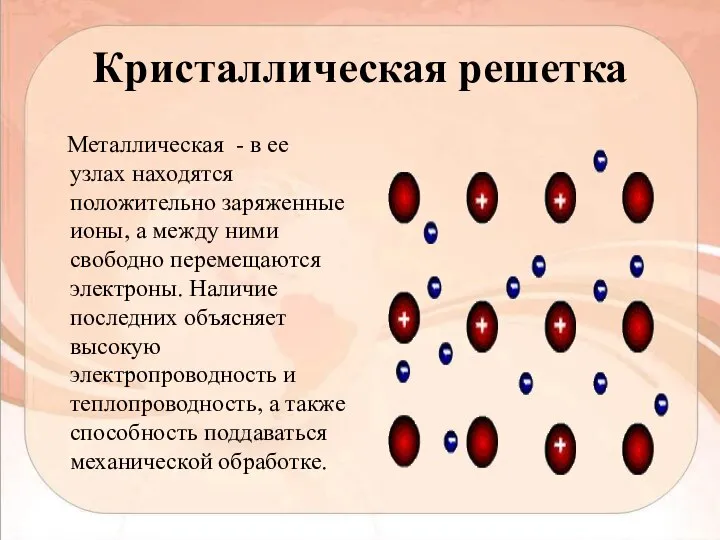
- 14. Кристаллическая решетка Металлическая - в ее узлах находятся положительно заряженные ионы, а между ними свободно перемещаются
- 15. Агрегатное состояние Все металлы твердые, исключение ртуть - единственный жидкий металл.
- 16. Ковкость Изготовление различных изделий из железа в кузнице.
- 17. Способность намагничиваться - железо, кобальт, никель. Находит применение при изготовлении магнитов.
- 18. Пластичность Способность изменять свою форму при ударе, прокатываться в тонкие листы, вытягиваться в проволоку: золото, серебро,
- 19. Пластичность Всем известна алюминиевая фольга. Алюминиевая фольга - это тонкий слой алюминия, в котором отлично сохраняются
- 20. Пластичность Оловянная фольга, которая используется для заворачивания лучших сортов шоколада.
- 21. Металлический блеск Световые лучи падают на поверхность металла и отталкиваются от неё свободными электронами, создавая эффект
- 22. Металлический блеск Зеркало состоит из гладкого стекла, на которое наносят очень тонкий слой металла. Часто зеркала
- 23. Электропроводность Высокая электропроводность уменьшается в ряду металлов: Аg Сu Аu Аl Мg Zn Fе РЬ Hg
- 24. Теплопроводность Хорошая теплопроводность, уменьшается в ряду металлов: Аg Сu Аu Аl Мg Zn Fе РЬ Hg
- 25. Все металлы делятся на две большие группы: Черные металлы : Имеют темно-серый цвет, большую плотность, высокую
- 26. Цветные металлы: Имеют характерную окраску: красную, желтую, белую; обладают большой пластичностью, малой твердостью, относительно низкой температурой
- 27. Плотность В зависимости от своей плотности металлы делятся на: Легкие (плотность не более 5 г/см3 )К
- 28. Плотность Тяжелые (плотность больше 5 г/см3).К тяжелым металлам относятся: цинк , медь , железо , олово
- 29. Твёрдость Металлы различаются по своей твердости: — мягкие: режутся даже ножом (натрий , калий , индий
- 30. Температура плавления В зависимости от температуры плавления металлы условно делятся на: Легкоплавкие (температура плавления до 1539°С).
- 32. Скачать презентацию


























 Соли Mg SO4 – сульфат магния
Соли Mg SO4 – сульфат магния Коррозия металлов. (Лекция 7)
Коррозия металлов. (Лекция 7) Презентация по Химии "Химия неметаллов. Общая характеристика" - скачать смотреть
Презентация по Химии "Химия неметаллов. Общая характеристика" - скачать смотреть  Химическая реакция
Химическая реакция Презентация по Химии "Химическая природа белка" - скачать смотреть
Презентация по Химии "Химическая природа белка" - скачать смотреть  Презентация по Химии "БЕНЗОЛ" - скачать смотреть
Презентация по Химии "БЕНЗОЛ" - скачать смотреть  Woda jako rozpuszczalnik
Woda jako rozpuszczalnik Тест с подсказками для закрепления знаний по теме Кислоты (8 класс)
Тест с подсказками для закрепления знаний по теме Кислоты (8 класс) Алкены
Алкены Алкины. Этин (Ацетилен)
Алкины. Этин (Ацетилен) Кинетика ферментативного катализа. (Лекция 5)
Кинетика ферментативного катализа. (Лекция 5) Теория Кристаллического Поля
Теория Кристаллического Поля Барий Подготовила ученица 10 класса Баштовая Анастасия
Барий Подготовила ученица 10 класса Баштовая Анастасия  Строение атома и периодическая система элементов Д. И. Менделеева
Строение атома и периодическая система элементов Д. И. Менделеева Кальций в океане: кораллы и жемчуг. Кальций в строительстве: гипс и алебастр
Кальций в океане: кораллы и жемчуг. Кальций в строительстве: гипс и алебастр Презентация по Химии "Бинарные соединения" - скачать смотреть
Презентация по Химии "Бинарные соединения" - скачать смотреть  Сильные и слабые электролиты. Степень диссоциации
Сильные и слабые электролиты. Степень диссоциации Массовая доля химического элемента в соединении
Массовая доля химического элемента в соединении Высокомолекулярные соединения (ВМС)
Высокомолекулярные соединения (ВМС) Статья двумя способами. Приготовление катализатора
Статья двумя способами. Приготовление катализатора Предельные одноатомные спирты. 10 класс
Предельные одноатомные спирты. 10 класс Радиоматериалы и радиокомпоненты. Зонная теория
Радиоматериалы и радиокомпоненты. Зонная теория Что изучает химия
Что изучает химия Осадочные горные породы
Осадочные горные породы Презентация по Химии "сульфиды" - скачать смотреть бесплатно
Презентация по Химии "сульфиды" - скачать смотреть бесплатно Окислительно-восстановительные процессы
Окислительно-восстановительные процессы Роль отечественных и зарубежных ученых в развитии неорганической химии
Роль отечественных и зарубежных ученых в развитии неорганической химии Строение сплавов
Строение сплавов