Содержание
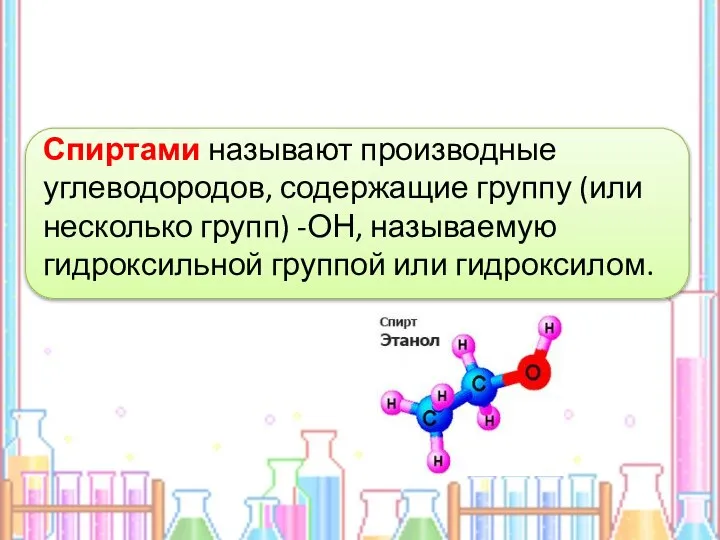
- 2. Спиртами называют производные углеводородов, содержащие группу (или несколько групп) -ОН, называемую гидроксильной группой или гидроксилом.
- 3. Функциональной называют группу атомов, которая определяет наиболее характерные свойства вещества и его принадлежность к определенному классу
- 4. Предельными одноатомными спиртами или, алканолами называют органические соединения, в молекулах которых алкильный радикал (R) связан с
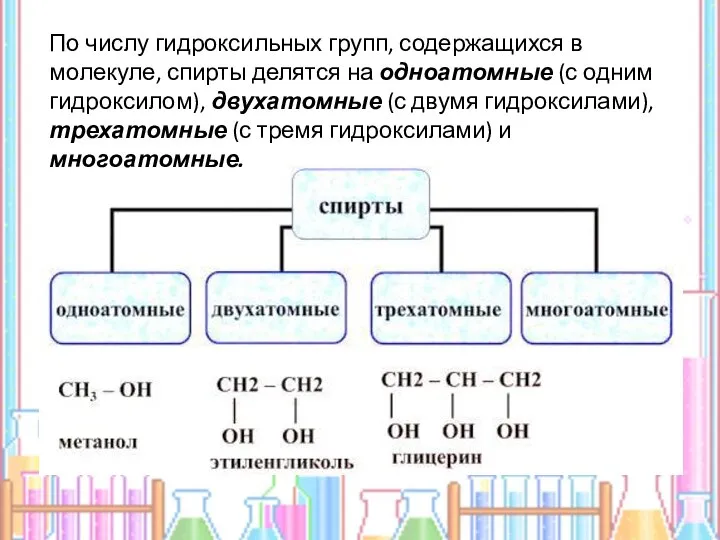
- 5. По числу гидроксильных групп, содержащихся в молекуле, спирты делятся на одноатомные (с одним гидроксилом), двухатомные (с
- 6. Номенклатура спиртов Систематические названия даются по названию углеводорода с добавлением суффикса -ол и цифры, указывающей положение
- 7. Изомерия спиртов 1. Для спиртов характерна структурная изомерия: изомерия положения ОН-группы (начиная с С3) 2. углеродного
- 8. Водородная связь Уменьшение расстояния между молекулами спиртов приводит к тому, что среди спиртов нет газообразных Веществ,
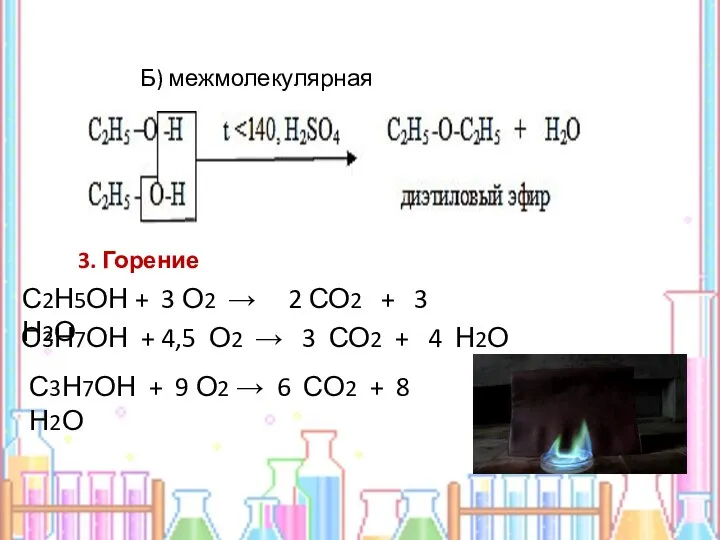
- 9. Химические свойства спиртов 1. Взаимодействие с галогеноводородами, подобно взаимодействию щелочей с кислотами 2. Дегидратация. А) внутримолекулярная
- 10. Б) межмолекулярная 3. Горение С2Н5ОН + 3 О2 → 2 СО2 + 3 Н2О С3Н7ОН +
- 11. 4. Спирты взаимодействуют со щелочными и щелочно-земельными металлами 2СН3-СН2-ОН + 2К → 2СН3-СН2-ОК + Н2↑ 2СН3-СН2-ОН
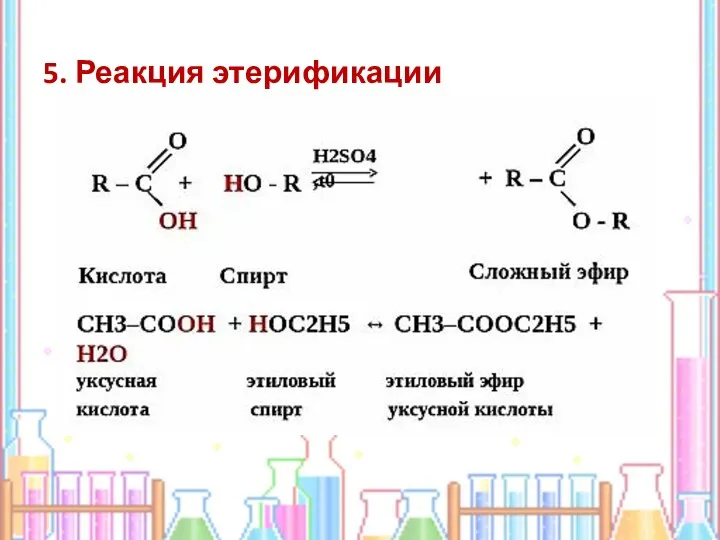
- 12. 5. Реакция этерификации
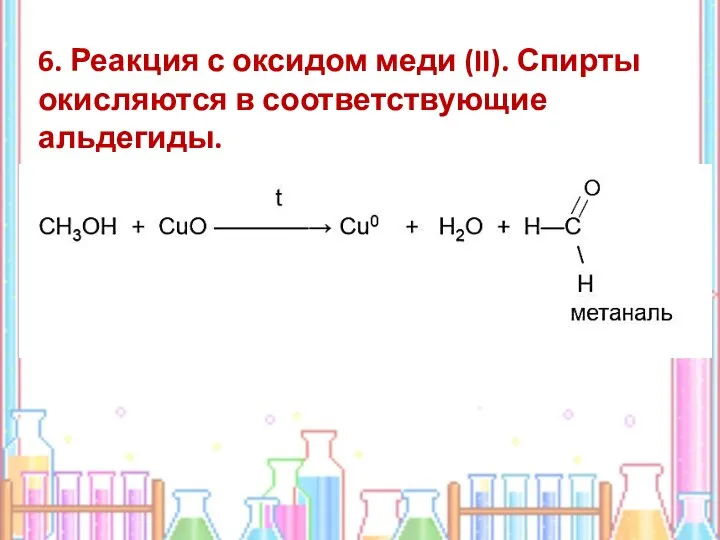
- 13. 6. Реакция с оксидом меди (II). Спирты окисляются в соответствующие альдегиды.
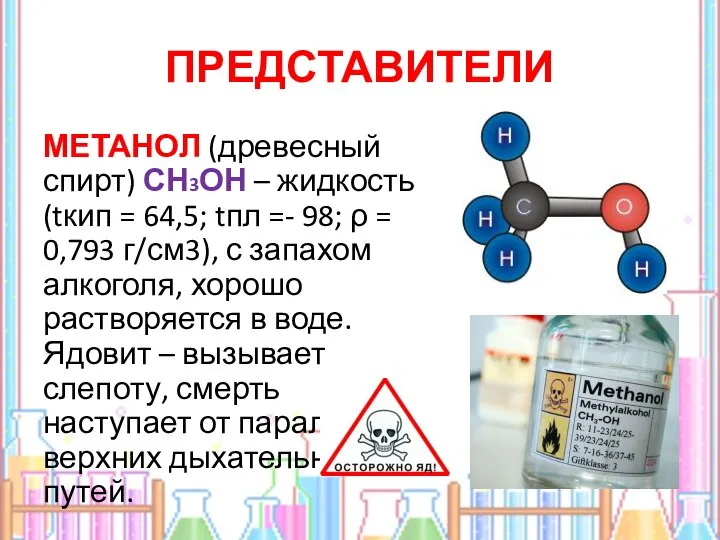
- 14. ПРЕДСТАВИТЕЛИ МЕТАНОЛ (древесный спирт) СН3ОН – жидкость (tкип = 64,5; tпл =- 98; ρ = 0,793
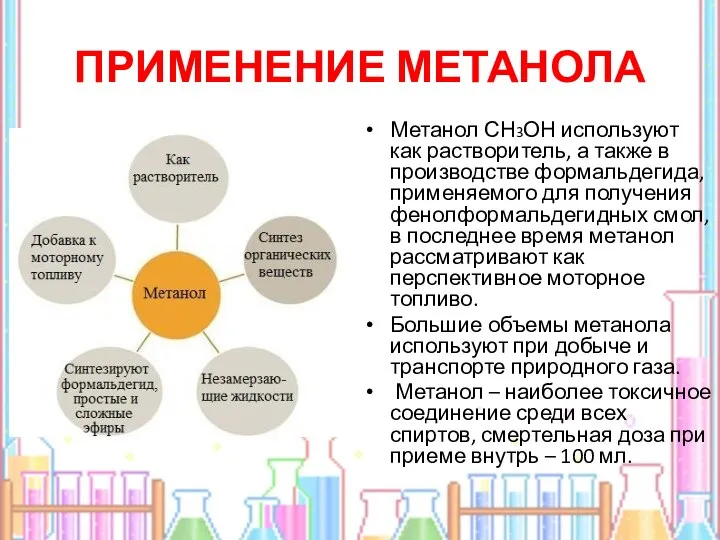
- 15. ПРИМЕНЕНИЕ МЕТАНОЛА Метанол СН3ОН используют как растворитель, а также в производстве формальдегида, применяемого для получения фенолформальдегидных
- 17. ЭТАНОЛ (винный спирт) С2Н5ОН – бесцветная жидкость, с запахом спирта, хорошо смешивается с водой, ядовитое наркотическое
- 18. ПРИМЕНЕНИЕ ЭТАНОЛА Этанол С2Н5ОН – исходное соединение для получения ацетальдегида, уксусной кислоты, а также для производства
- 19. спиртовое брожение глюкозы: C6H12O6 → 2C2H5OH + 2CO2↑ глюкоза → спирт этанол получение спирта из алкена:
- 21. Скачать презентацию











 Химическая природа и состав нефти и газа. Физико-химические свойства нефтей и нефтепродуктов
Химическая природа и состав нефти и газа. Физико-химические свойства нефтей и нефтепродуктов Молекулы и атомы. Простые и сложные вещества
Молекулы и атомы. Простые и сложные вещества Lead
Lead Презентация по Химии "Высшие природные полимеры - Белки и Нуклеиновые кислоты" - скачать смотреть
Презентация по Химии "Высшие природные полимеры - Белки и Нуклеиновые кислоты" - скачать смотреть  Алмаз, графит и фуллерен Строковой Натальи 9б
Алмаз, графит и фуллерен Строковой Натальи 9б  Взаимодействие кислоты с основанием
Взаимодействие кислоты с основанием Минералогия и кристаллография
Минералогия и кристаллография Оксид кремния
Оксид кремния Неметаллы. Аллотропия. Куцапкина Людмила Васильевна учитель химии ГБОУ гимназии № 343 Невского района Санкт- Петербурга
Неметаллы. Аллотропия. Куцапкина Людмила Васильевна учитель химии ГБОУ гимназии № 343 Невского района Санкт- Петербурга Рідкісні кристали і полімери. Їх властивості та застосування
Рідкісні кристали і полімери. Їх властивості та застосування Тема урока : Скорость химической реакции
Тема урока : Скорость химической реакции  Презентация Правила безопасности в кабинете химии
Презентация Правила безопасности в кабинете химии Глицерин
Глицерин Контейнерная химия: комплексоны, комплексообразование, применение
Контейнерная химия: комплексоны, комплексообразование, применение Тотығып фосфорлану
Тотығып фосфорлану Оксид серы(VI). Серная кислота
Оксид серы(VI). Серная кислота Явище ізомерії. Структурна ізомерія. Близнюки органічного світу
Явище ізомерії. Структурна ізомерія. Близнюки органічного світу Презентация по Химии "Водні Ресурси" - скачать смотреть
Презентация по Химии "Водні Ресурси" - скачать смотреть  Алюминий, его физические и химические свойства
Алюминий, его физические и химические свойства неметаллы Общая характеристика
неметаллы Общая характеристика Изучение содержания углекислого газа в классном помещении и определение оптимальных условий для проветривания. Муниципальное об
Изучение содержания углекислого газа в классном помещении и определение оптимальных условий для проветривания. Муниципальное об Вода. Свойства воды
Вода. Свойства воды Аттестационная работа. Рабочая программа курса внеурочной деятельности «Химия. Мои первые опыты»
Аттестационная работа. Рабочая программа курса внеурочной деятельности «Химия. Мои первые опыты» Протолитическое равновесие в водных и неводных растворах
Протолитическое равновесие в водных и неводных растворах Методы трансформации карбоновых кислот и их производных
Методы трансформации карбоновых кислот и их производных Простые вещества, металлы
Простые вещества, металлы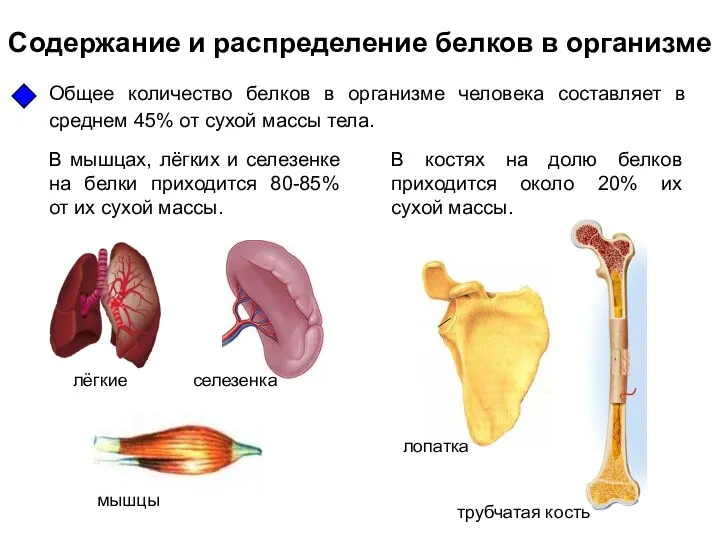 Содержание и распределение белков в организме
Содержание и распределение белков в организме Структурный тип
Структурный тип