Содержание
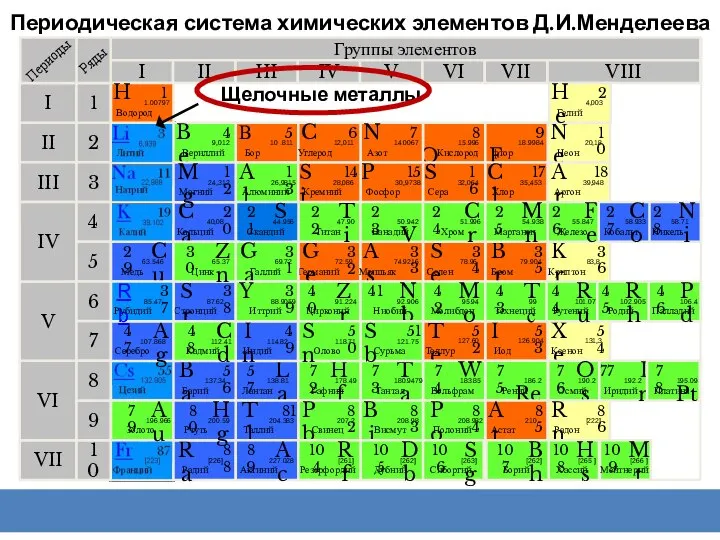
- 2. Периодическая система химических элементов Д.И.Менделеева Группы элементов I III II VIII IV V VI VII II
- 3. Группы элементов I III II VIII IV V VI VII II I III VII VI V
- 4. * Fr K Na Li Изменение свойств группе Увеличиваются восстановительные свойства (способность отдавать электроны) Уменьшается прочность
- 5. СТРОЕНИЕ АТОМОВ ЩЕЛОЧНЫХ МЕТАЛЛОВ Строение внешнего энергетического уровня ns1 степень окисления +1.
- 6. ОТКРЫТИЕ ЩЕЛОЧНЫХ МЕТАЛЛОВ Литий был открыт шведским химиком Й. Арфведсоном в 1817 г. И назван литием
- 7. ОТКРЫТИЕ ЩЕЛОЧНЫХ МЕТАЛЛОВ Натрий и калий были впервые получены английским химиком и физиком Г. Дэви в
- 8. * Эти металлы получили название щелочных, потому что большинство их соединений растворимы в воде. По-славянски «выщелачивать»
- 9. Физические свойства Все металлы этой подгруппы имеют серебристо-белый цвет (кроме серебристо-жёлтого цезия). калий рубидий литий натрий
- 10. Франций радиоактивный щелочной металл В природе не существует в таких количествах, которые достаточны для изучения его
- 11. Физические свойства Литий, натрий и калий легче воды и плавают на её поверхности, реагируя с ней.
- 12. Они очень мягкие, их можно резать ножом, скальпелем. Физические свойства
- 13. ХИМИЧЕСКИЕ СВОЙСТВА Из-за высокой химической активности щелочных металлов по отношению к воде, кислороду, и иногда даже
- 14. Нахождение в природе Как очень активные металлы, они встречаются в природе только в виде соединений. Натрий
- 15. Сподуменн LiAl[Si2O6]
- 16. Галит NaСl
- 17. Природные соединения калия Сильвин КСl
- 18. Лепидолит- один из основных источников редких щелочных металлов, рубидия и цезия
- 19. ХИМИЧЕСКИЕ СВОЙСТВА ВЗАИМОДЕЙСТВИЕ С КИСЛОРОДОМ: 4Li + O2 =2Li2O(оксид лития)
- 20. ВЗАИМОДЕЙСТВИЕ С КИСЛОРОДОМ: Щелочной металл на воздухе легко окисляется до оксида натрия. 2Na + O2 =
- 21. ХИМИЧЕСКИЕ СВОЙСТВА Реакции с неметаллами : 2Li + Cl2 = 2LiCl(галогениды) 2Na + S = Na2S(сульфиды)
- 22. Взаимодействие с водой Li - спокойно, Na - энергично, остальные – со взрывом – воспламеняется выделяющийся
- 23. С кислотами: https://www.youtube.com/watch?v=Td6itaNfJrU&t=3s 2Na+ Н2SО4 = Na2SО4 + Н2 (протекают очень бурно)
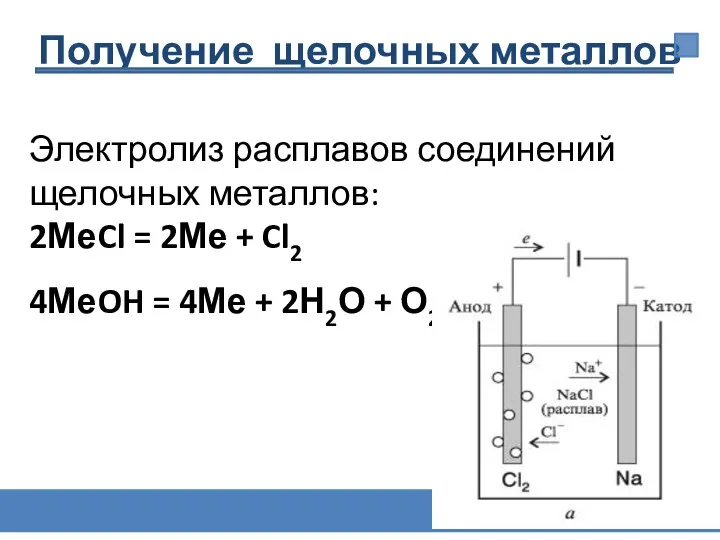
- 24. Электролиз расплавов соединений щелочных металлов: 2МеCl = 2Ме + Cl2 4МеOH = 4Ме + 2Н2О +
- 25. * Окраска пламени ионами щелочных металлов Li+ карминово- красный K+ Na+ желтый Cs+ фиолетовый Качественная реакция
- 26. Оксид натрия Хранить оксид натрия Na2O лучше всего в безводном бензоле.
- 27. Пероксид натрия Na2O2
- 28. ПОЛУЧЕНИЕ ОКСИДОВ Чистый оксид натрия получить непосредственным окислением натрия нельзя, так как образуется смесь, состоящая из
- 29. 1) Для получения оксидов натрия и калия нагревают смеси гидроксида, пероксида или надпероксида с избытком металла
- 30. Общая формула – МеОН Белые кристаллические вещества, гигроскопичны, хорошо растворимы в воде (с выделением тепла). Растворы
- 31. Едкий натр (гидроксид натрия) NaOH
- 32. Едкое кали (гидроксид калия) КOH
- 33. Схема образования гидроксида натрия: Н ОН Na гидроксид натрия
- 34. Фенолфталеин - малиновый
- 35. Они участвуют во всех реакциях, характерных для оснований — реагируют с кислотами, кислотными и амфотерными оксидами,
- 36. Химические свойства 1.С кислотами Основание + кислота = Соль + вода NaOH + HCl = NaCl
- 37. 2. С кислотными оксидами Щёлочь + кислотный оксид = соль + вода (р-ция обмена) Ca(OH)2 +
- 38. 3. С амфотерными гидроксидами: 2 NaOH + Zn(ОН)2 → Na2[Zn(OH)4] Тетрагидроксоцинкат натрия
- 39. Химические свойства 4. С солями Щёлочь + соли = (новое)основание + (новая) соль. NaOH + CuSO4
- 40. Соли натрия Na2CO310H2O – кристаллическая сода используется в стекольном производстве, мыловарении, в производстве стиральных и чистящих
- 41. Цезий - самый активный металл на Земле! https://www.youtube.com/watch?v=1gh5JJDvdiQ
- 42. Значение и роль калия в организме Натриий и калий отвечают за нормальный водный баланс в организме.
- 43. источники натрия Натрий содержится в капусте брокколи, цветной капусте, картофеле, фасоли, винограде, арбузе.
- 44. источники калия Калий содержится в продуктах растительного происхождения: фруктах, овощах, картофеле, бобовых и злаковых культурах.
- 45. Мыла – это натриевые или калиевые соли высших жирных кислот, гидролизующихся в водном растворе с образованием
- 46. Рубидий Играет немалую роль в организме и оказывает такое влияние: оказывает антигистаминное воздействие (борется с воздействием
- 47. ПОВТОРИМ: Наиболее выраженные металлические свойства проявляет: ? алюминий ? натрий ? магний ? бериллий ? железо
- 48. Калий взаимодействует с водой с образованием.... и .... ? соли ? водорода ? щелочи ? оксида
- 50. Скачать презентацию












![Сподуменн LiAl[Si2O6]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1395862/slide-14.jpg)





















![3. С амфотерными гидроксидами: 2 NaOH + Zn(ОН)2 → Na2[Zn(OH)4] Тетрагидроксоцинкат натрия](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1395862/slide-37.jpg)










 Введение. Основные понятия химии
Введение. Основные понятия химии I закон термодинамики, его применение для расчёта тепловых эффектов
I закон термодинамики, его применение для расчёта тепловых эффектов Дозиметрия ионизирующих излучений. Влияние радиации на организм человека
Дозиметрия ионизирующих излучений. Влияние радиации на организм человека Камни и Рак
Камни и Рак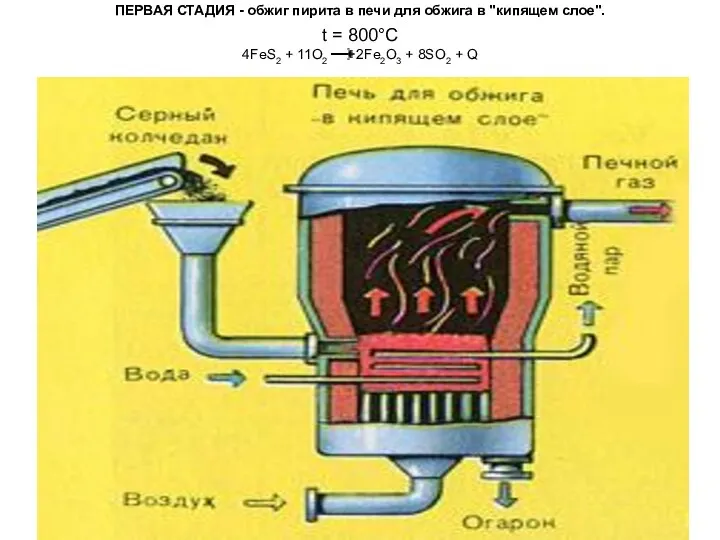 Получение серной кислоты
Получение серной кислоты Презентация Спирты
Презентация Спирты Глицерин Свойства - применение Выполнила учитель химии МОУ «Средняя школа №7» г. Балаково Саратовской области Трибунская Е
Глицерин Свойства - применение Выполнила учитель химии МОУ «Средняя школа №7» г. Балаково Саратовской области Трибунская Е Получение водорода в промышленности и его применение Химия 8 класс
Получение водорода в промышленности и его применение Химия 8 класс  Исследование влияния концентрации наночастиц никеля в водных растворах на генерацию активных форм кислорода при лазерном пробое
Исследование влияния концентрации наночастиц никеля в водных растворах на генерацию активных форм кислорода при лазерном пробое Классификация химических элементтов
Классификация химических элементтов Презентация по Химии "Нитраты - минеральные удобрения" - скачать смотреть
Презентация по Химии "Нитраты - минеральные удобрения" - скачать смотреть  Фізичні та хімічні явища. (7 клас)
Фізичні та хімічні явища. (7 клас) Каучук. История открытия
Каучук. История открытия Материаловедение. Теория термической обработки стали. (Тема 8)
Материаловедение. Теория термической обработки стали. (Тема 8) Органические вещества. Валентность. Теория химического строения
Органические вещества. Валентность. Теория химического строения Основы общей химии
Основы общей химии Важнейшие химические понятия и законы
Важнейшие химические понятия и законы Презентация по химии Неорганические и органические основания.
Презентация по химии Неорганические и органические основания.  Особенности строения, реакционной способности и методы синтеза алкенов
Особенности строения, реакционной способности и методы синтеза алкенов Водород, нахождение в природе. Получение водорода и его физические свойства
Водород, нахождение в природе. Получение водорода и его физические свойства Классификация оснований
Классификация оснований PSKhE
PSKhE Электрофизические свойства GaAs, зонная структура, полупроводящий и полуизолирующий GaAs, способы создания p-n перехода
Электрофизические свойства GaAs, зонная структура, полупроводящий и полуизолирующий GaAs, способы создания p-n перехода Деструкция углеводородов
Деструкция углеводородов Физические, химические свойства предельных и непредельных карбоновых кислот, получение
Физические, химические свойства предельных и непредельных карбоновых кислот, получение Классификация силикатов
Классификация силикатов - Это оружие массового поражения, действие которого основано на токсических свойствах химических веществ. - Это оружие массового
- Это оружие массового поражения, действие которого основано на токсических свойствах химических веществ. - Это оружие массового  Алюминий и его органические производные
Алюминий и его органические производные