Содержание
- 2. Механизм окислительно-восстановительных реакций . Принятая модель переноса электронов не является строгой и чаще всего не соответствует
- 3. Считается, что перенос электронов осуществляется через образование активного комплекса, как в реакции: Hg2++Sn 2+→[Hg2+∙ Sn 2+
- 4. Иногда перенос электронов связан с переносом атомов, как в реакции: [NO2]−+HClO+H2O =NO3- +H3O+ + Cl- .
- 5. О направлении ОВР. В теории окислительно-восстановительных реакций главными являются следующие вопросы: – возможен или невозможен тот
- 6. В случае ОВР в водных растворах необходимо использовать традиционную схему, в основе которой лежит понятие окислительно-
- 7. Иначе можно сказать, если φок > φвс в объединенном процессе, т. е. ΔE > 0 (при
- 8. Выводы: – окислительно-восстановительный процесс возможен, если ΔЕ > 0 (при этом ΔG – окислительно-восстановительный процесс протекает
- 9. Стандартные значения (Е0) получены при концентрациях 1 моль/дм3 для всех участников полуреакции, при температуре 298 К,
- 10. Возможность же осуществления окислительно- восстановительного процесса определится неравенством φок > φвс, так как при этом ΔG
- 11. Окислительно-восстановительные реакции в водных растворах Направление процесса с позиций термодинамики определяется также изменением свободной энергии ΔG,
- 12. Если условия проведения процесса отличаются от стандартных, то электродный определяется уравнением Нернста. В реальных ОВР значение
- 13. Концентрационные эффекты. Анализ уравнения Нернста показывает, что даже при достаточно большом изменении (уменьшении или увеличении) концентраций
- 14. Сильно концентрационные эффекты проявляются в тех случаях, когда концентрация одного из участников окислительно-восстановительного процесса уменьшается на
- 15. Влияние температуры и давления. На ОВР в водных растворах оказывают влияние многие факторы. Влияние температуры на
- 16. Кислотность среды. Наиболее важным фактором является кислотность среды концентрация гидратированных катионов водорода и гидроксид-ионов. Поскольку эти
- 17. Окислительный потенциал полуреакции меняется с изменением рН раствора во всех случаях, когда изменение рН вызывает изменение
- 18. Второй способ К такому же выводу можно прийти формальным путем, вычислив φ по уравнению Нернста. В
- 19. ВЫВОДЫ – если при изменении рН водного раствора окислительные потенциалы двух полуреакций, составляющих единый окислительно-восстановительный процесс,
- 20. С увеличением концентрации водородных катионов окислительная способность (особенно кислородсодержащих соединений) нарастает; восстановительная же способность веществ в
- 21. Диаграммы φ – рН. Вода является хорошим растворителем для большинства веществ, которые могли бы быть использованы
- 22. Очень часто взаимосвязь между кислотностью среды (рН) и окислительно-восстановительными потенциалами (φ) изображают в виде диаграмм φ
- 23. Эти линии характеризуют термодинамическое равновесное состояние рассматриваемой электрохимической системы при изменении рН. Такую линию легко построить
- 24. в кислой среде восстановление воды описывается 2Н + +2ē = Н2 φ = 0,00 – 0,059
- 25. Так как вода проявляет cвойства и окислителя и восстановителя, то необходимо предусмотреть возможность окислительно- восстановительного процесса
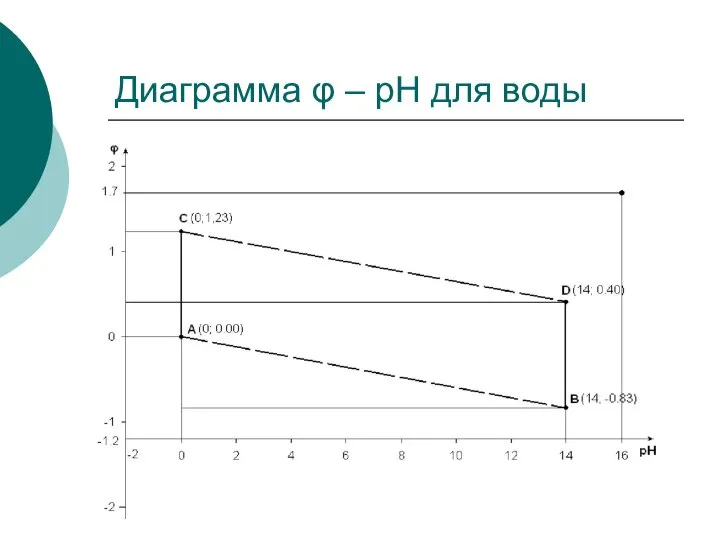
- 26. Диаграмма φ – рН для воды
- 27. По двум точкам с координатами А (рН = 0; φ = 0,00) и В (рН =
- 28. Интервал значений рН на диаграмме φ – рН ограничен областью 0–14, что обусловлено свойствами воды и
- 29. Выводы Электрохимические системы, имеющие электродный потенциал (φx) меньший, чем потенциал восстановления воды, будут взаимодействовать с водой.
- 30. Системы, имеющие электродный потенциал (φx) меньше, чем потенциал окисления воды устойчивы в воде. Иначе, если значение
- 31. Значение диаграмм φ – рН Кроме того, можно построить на фоне параллелограмма ABCD линии φx –
- 32. Окислительно-восстановительные реакции в неводных растворах Принципиально окислительно-восстановительные реакции в неводных средах должны протекать так же, как
- 33. Несмотря на экспериментальные трудности ОВ потенциалы определены для многих систем в большом числе растворителей. Если расположить
- 34. Влияние растворителя на диапазон возможных ОВР Смена растворителя может изменить диапазон возможных ОВР для синтеза. Представленные
- 35. В жидком аммиаке можно работать с веществами, которые являются чрезвычайно сильными восстановителями (например со щелочными металлами)
- 36. ОВР в расплавах Интересными и перспективными могут быть ОВР в расплавленных солях, которые являются хорошими растворителями
- 37. В качестве растворителей часто используются расплавы галогенидов щелочных и щелочноземельных металлов, так как по отношению ко
- 38. Окислительно-восстановительные реакции в твердой фазе Механизмы протекания ОВР в твердой фазе сложны и разнообразны. Моментом для
- 39. Экспериментально доказано, что электронный переход, обусловливающий проводимость, происходит не между катионом и анионом, а внутри анионной
- 40. Исследование разложения перманганата калия, входящего в состав твердого раствора с перхлоратом калия, показало, что часть перманганат-ионов
- 41. Экспериментально установлено: – добавки некоторых оксидов (CuO, NiO, MnO) ускоряют термолиз перманганата калия; – диоксид марганца,
- 42. ОВР в газовой фазе Классическим примером реакции, в которой все вещества – участники процесса – находятся
- 43. Механизм ОВР в газовой фазе Лимитирующей стадией синтеза аммиака на поверхности железного катализатора является хемосорбция азота,
- 44. Большой теоретический и практический интерес представляет вопрос фиксации азота с применением перекиси водорода. Проблема связывания азота
- 45. Сопряженные реакции в ОВР в газовой фазе. Представляет интерес разработка таких химико-технологических процессов, в которых используются
- 46. Механизмы каталитических реакций окисления При обсуждении механизма каталитических окислительно- восстановительных реакций часто используют два подхода: –
- 47. Сущность стадийного механизма ОВР При стадийном механизме предполагается, что каталитический процесс состоит, по крайней мере, из
- 48. Примеры синтезов со стадийным механизмом Стадийный механизм характерен для реакций, протекающих при сравнительно высоких температурах (выше
- 49. Сущность ассоциативного механизма Для ассоциативного механизма ОВР (или одновременного взаимодействия с катализатором обоих реагирующих веществ) теоретическим
- 51. Скачать презентацию


![Иногда перенос электронов связан с переносом атомов, как в реакции: [NO2]−+HClO+H2O](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1408031/slide-3.jpg)












































 Алканы
Алканы Щелочные и щелочно-земельные металлы Na K Li Cs Ba Rb Fr
Щелочные и щелочно-земельные металлы Na K Li Cs Ba Rb Fr  Опасные химикаты
Опасные химикаты Методы защиты от коррозии
Методы защиты от коррозии Тест 1.Тип кристаллической решетки у белого фосфора…. а) молекулярный б) атомный в) ионный а) молекулярный Р4 2. У фосфора…..
Тест 1.Тип кристаллической решетки у белого фосфора…. а) молекулярный б) атомный в) ионный а) молекулярный Р4 2. У фосфора…..  Презентация Мыло. Синтетические моющие средства
Презентация Мыло. Синтетические моющие средства Алколоиды
Алколоиды Презентация по Химии "Металлы на теле человека" - скачать смотреть
Презентация по Химии "Металлы на теле человека" - скачать смотреть  Әртүрлі заттардың кристаллдық тор энергиясын, сольваттану энергиясын, гидратация жылуын есептеу
Әртүрлі заттардың кристаллдық тор энергиясын, сольваттану энергиясын, гидратация жылуын есептеу Промышленные типы месторождений железа
Промышленные типы месторождений железа Вычисления по химическим уравнениям
Вычисления по химическим уравнениям Эксперимент. Качественная реакция на крахмал
Эксперимент. Качественная реакция на крахмал Строение твердых и жидких металлов. Зональная ликвация
Строение твердых и жидких металлов. Зональная ликвация Алмазы, искусственный и естественный рост
Алмазы, искусственный и естественный рост Кремний және оның қосылыстары
Кремний және оның қосылыстары Предельные и непредельные углеводороды
Предельные и непредельные углеводороды Презентация по Химии "Уран" - скачать смотреть
Презентация по Химии "Уран" - скачать смотреть  Алкогольді мастықты талдаудың физико-химиялық әдістері
Алкогольді мастықты талдаудың физико-химиялық әдістері Макрокинетика гетерогенно-каталитических процессов
Макрокинетика гетерогенно-каталитических процессов Альдегиды и кетоны
Альдегиды и кетоны Характеристика элементов VIIA-группы (галогены)
Характеристика элементов VIIA-группы (галогены) Стеклянные товары. Основные сырьевые материалы для производства стекла
Стеклянные товары. Основные сырьевые материалы для производства стекла Бинарный интегрированный урок (география + химия) . 8 класс
Бинарный интегрированный урок (география + химия) . 8 класс Химическая формула. Относительная атомная и относительная молекулярная массы
Химическая формула. Относительная атомная и относительная молекулярная массы Презентация тест по химии
Презентация тест по химии Металдар
Металдар Цезій (Cs) Підготувала Учениця 10 класу СЗШ №12 Максименко Анастасія 2015р.
Цезій (Cs) Підготувала Учениця 10 класу СЗШ №12 Максименко Анастасія 2015р.  Взаимодействие веществ
Взаимодействие веществ