Содержание
- 2. В 300 мг 20% раствора HNO3 растворили 10 мл аммиака. Определить массу полученной соли. Задача:
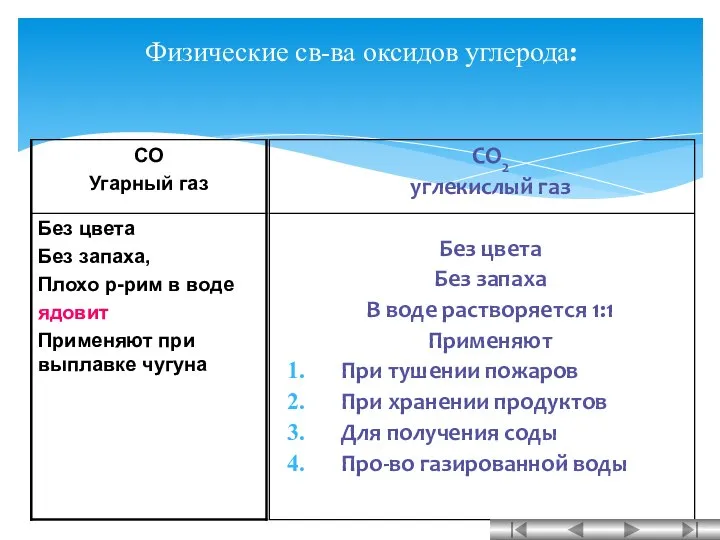
- 3. CO2 углекислый газ Без цвета Без запаха В воде растворяется 1:1 Применяют При тушении пожаров При
- 4. Сублимация (возгонка) – переход из твердого состояния в газообразное минуя жидкое Классификация оксидов углерода
- 5. 1. кислотный оксид, тяжелее воздуха, не поддерживает горение и не горит, кроме Mg: CO2 + Mg
- 6. 1. В лаборатории: CaCO3 + 2HCl = CaCl2 + CO2↑+ H2O 2. В промышленности: CaCO3 =
- 8. Скачать презентацию




 Углеводы. Карбоновые кислоты и их производные
Углеводы. Карбоновые кислоты и их производные Урок химии в 9-ом классе Тема урока "Сера"
Урок химии в 9-ом классе Тема урока "Сера" Пространственное строение органических соединений. (Лекция 2)
Пространственное строение органических соединений. (Лекция 2) Особенности химического состава клетки
Особенности химического состава клетки Каркасные силикаты
Каркасные силикаты Обмен белков и аминокислот. Азотистый баланс. (Лекция 14)
Обмен белков и аминокислот. Азотистый баланс. (Лекция 14) IVA группа С, Si, Ge, Sn, Pb (подгруппа титана)
IVA группа С, Si, Ge, Sn, Pb (подгруппа титана) Минерал как химическое соединение
Минерал как химическое соединение Тест по неорганической химии
Тест по неорганической химии Никель Ni
Никель Ni солі в природі Солі препарати замінення атомів водної кислоти
солі в природі Солі препарати замінення атомів водної кислоти  Камень, скользящий на льду
Камень, скользящий на льду Defect in solid
Defect in solid Элемент № 24 периодической таблицы. Хром
Элемент № 24 периодической таблицы. Хром Химическая термодинамика и биоэнергетика. Второй закон термодинамики
Химическая термодинамика и биоэнергетика. Второй закон термодинамики КУБАНСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ КАФЕДРА ФУНДАМЕНТАЛЬНОЙ И КЛИНИЧЕСКОЙ БИОХИМИИ Лекция по теме: «Матричные б
КУБАНСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ КАФЕДРА ФУНДАМЕНТАЛЬНОЙ И КЛИНИЧЕСКОЙ БИОХИМИИ Лекция по теме: «Матричные б Основные классы неорганических и органических соединений
Основные классы неорганических и органических соединений Реакция обменного разложения веществ водой - гидролиз
Реакция обменного разложения веществ водой - гидролиз Ресурсы и энергоснабжение
Ресурсы и энергоснабжение Газообразное состояние вещества
Газообразное состояние вещества Презентация по Химии "Алюминий (11 класс)" - скачать смотреть
Презентация по Химии "Алюминий (11 класс)" - скачать смотреть  Типы изомерии 1.Историческая справка 2.Изомерия. Изомеры. 3.Типы изомерии. Классификация изомеров.
Типы изомерии 1.Историческая справка 2.Изомерия. Изомеры. 3.Типы изомерии. Классификация изомеров.  Органическая химия и важнейшие органические соединения углевода
Органическая химия и важнейшие органические соединения углевода Состав, структура, свойства ДНК. (Лекция 2)
Состав, структура, свойства ДНК. (Лекция 2) Логическая структура модуля по дисциплине "Аналитическая химия"
Логическая структура модуля по дисциплине "Аналитическая химия" Мило
Мило  Роль микро- и макроэлементов в здоровье человека
Роль микро- и макроэлементов в здоровье человека Кремний и его «родственники»
Кремний и его «родственники»