Содержание
- 2. Рекомендуемая литература О.А.Реутов, А.Л.Курц, К.П.Бутин, Органическая химия, т.1,2,3,4, “Бином”, Москва, 2005 г. А.Л.Курц и др. Задачи
- 3. Дополнительная литература Органикум (практикум по органической химии) т.1 и т.2 "Мир",1980 г. А.А.Терней, Современная органическая химия,
- 4. Введение Отличительной особенностью органической химии можно считать то, что объектом ее изучения являются соединения, в составе
- 5. Основные этапы развития химии 1. Предалхимический период: до III в. н.э. 2. Алхимический период: III –
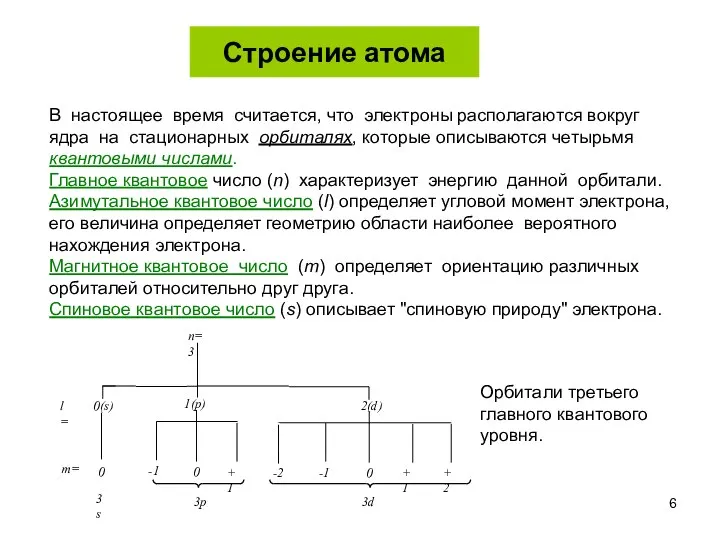
- 6. Строение атома В настоящее время считается, что электроны располагаются вокруг ядра на стационарных орбиталях, которые описываются
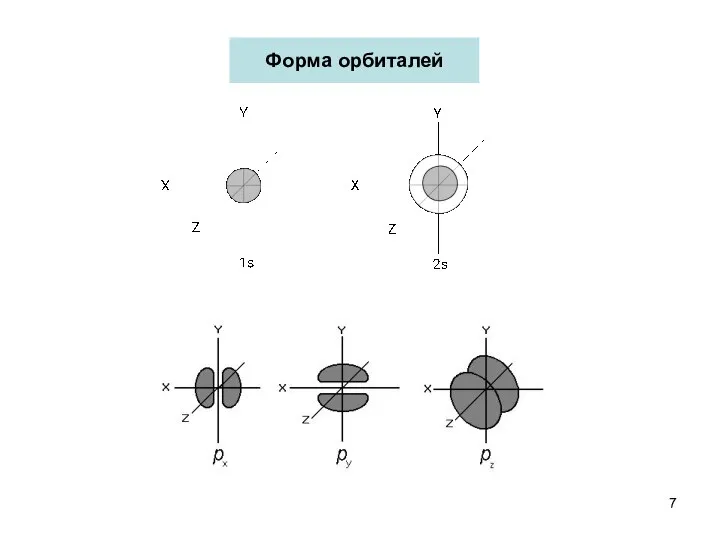
- 7. Форма орбиталей
- 8. Потенциал ионизации - количество энергии, необходимое для отрыва электрона от молекулы. Сродство к электрону - количество
- 9. Структурная теория А.М.Бутлерова 1.В молекулах веществ существует строгая последовательность химического связывания элементов, которая называется химической структурой
- 10. Типы связей Ионная связь образуется за счет электростатического притяжения между двумя противоположно заряженными частицами: ион-ионные (взаимодействия
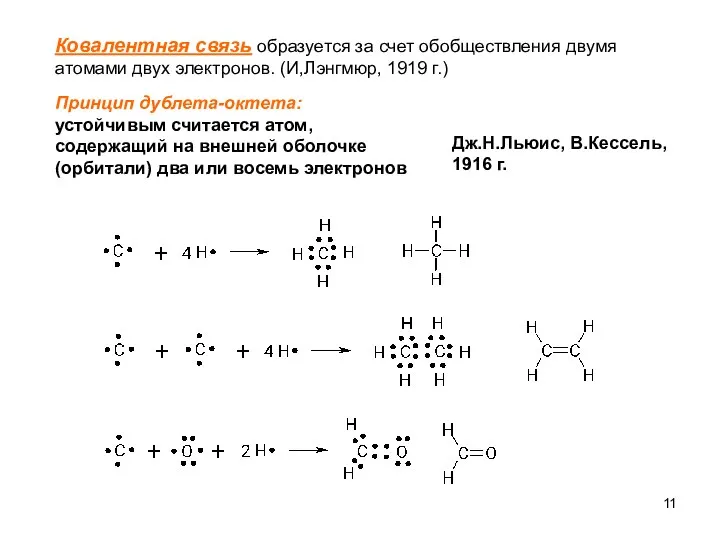
- 11. Ковалентная связь образуется за счет обобществления двумя атомами двух электронов. (И,Лэнгмюр, 1919 г.) Принцип дублета-октета: устойчивым
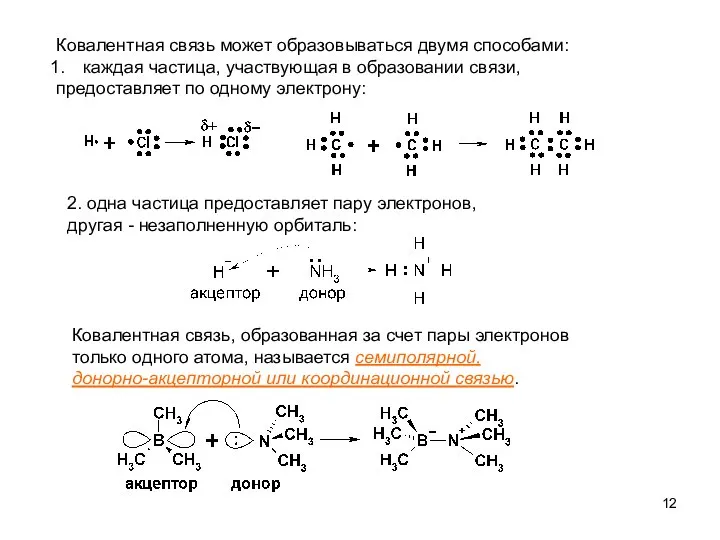
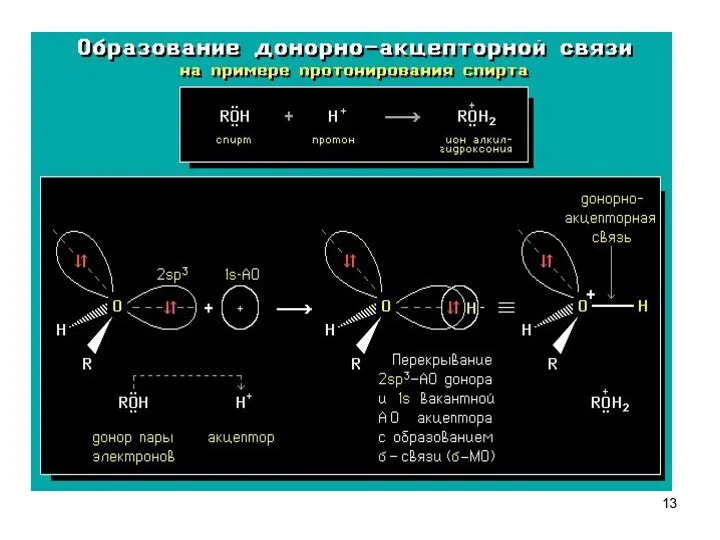
- 12. Ковалентная связь может образовываться двумя способами: каждая частица, участвующая в образовании связи, предоставляет по одному электрону:
- 14. Водородная связь обусловленная электростатическим притяжением и ковалентным взаимодействием между протонированным водородом одной молекулы и электроотрицательным атомом
- 15. Ковалентная связь образуется за счет перекрывания атомных орбиталей, на которых находились электроны, образовавшие связь. При этом
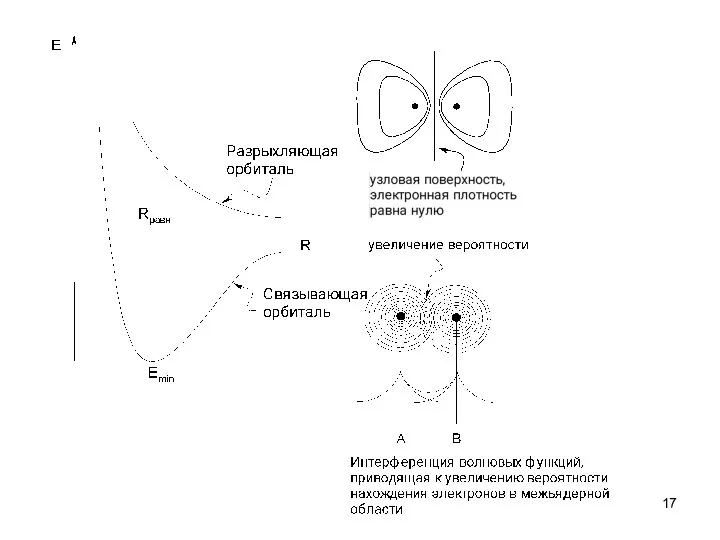
- 16. Разрыхляющая орбиталь Связывающая орбиталь
- 18. φ=c1χ1+ c2χ2+…+ cμχμ+…+ cnχn Состояние электронов в молекуле описывается относительно всех атомов этой молекулы с помощью
- 19. Граничные орбитали. Заполнение МО электронами подчиняется тем же правилам, что и заполнение АО. Занятая электронами МО
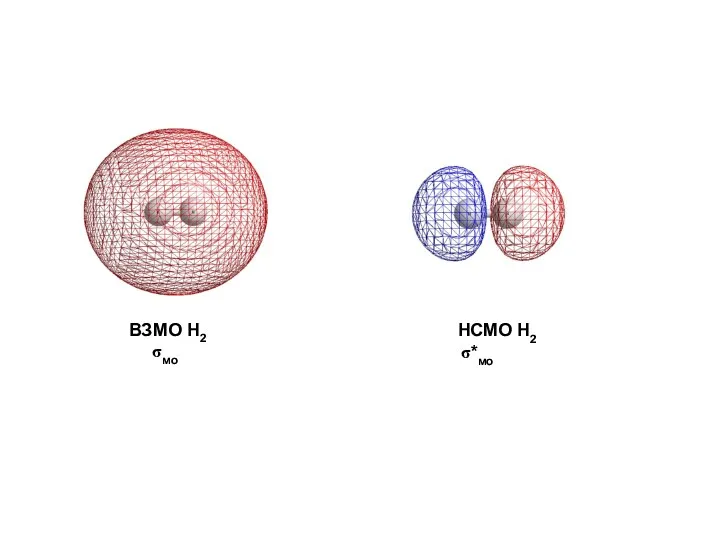
- 20. ВЗМО H2 σмо НСМО H2 σ*мо
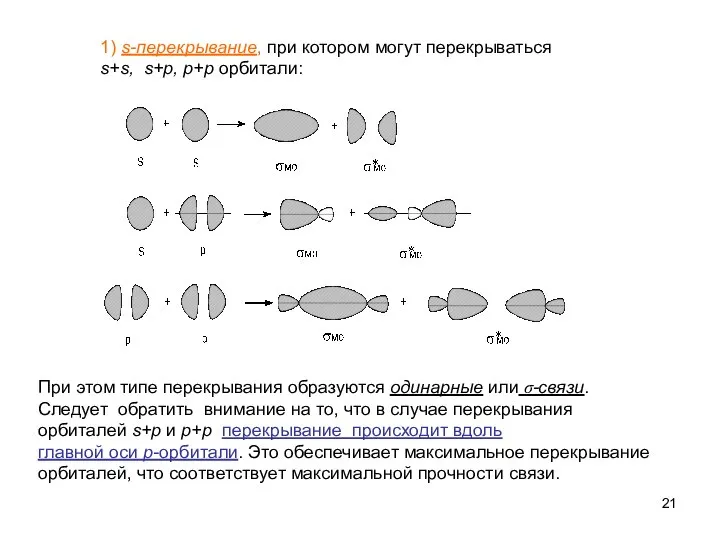
- 21. 1) s-перекрывание, при котором могут перекрываться s+s, s+p, p+p орбитали: При этом типе перекрывания образуются одинарные
- 22. 2) p-перекрывание, в котором могут участвовать только p-орбитали. При этом главные оси орбиталей параллельны. Такие связи
- 23. Характерные свойства ковалентной связи Направленность Насыщаемость Полярность Поляризуемость Они определяют химические и физические свойства соединений. Направленность
- 24. Энергия связи – средняя энергия, которая необходима для гомолитического разрыва связи (энергия диссоциации). Длина – равновесное
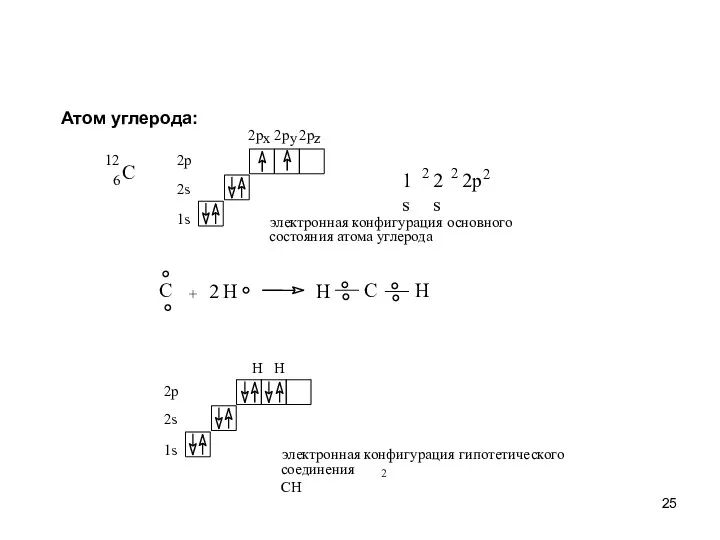
- 25. Атом углерода: C 12 6 1s 2s 2 2 2 2p C + H 2 H
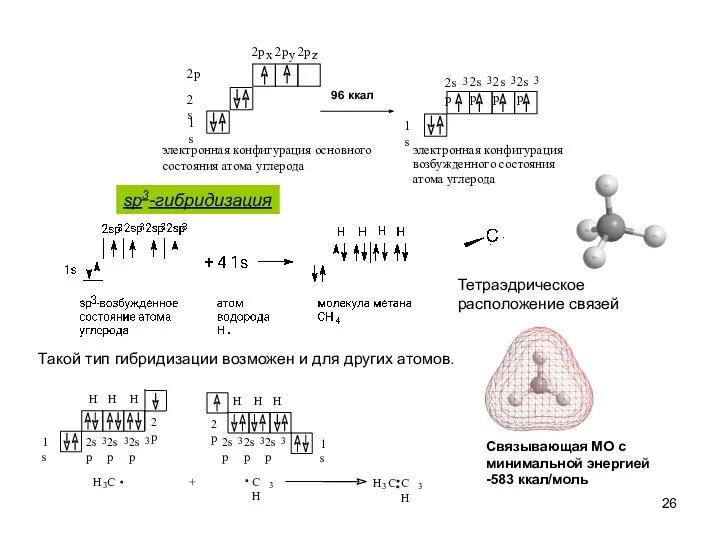
- 26. Такой тип гибридизации возможен и для других атомов. sp3-гибридизация Тетраэдрическое расположение связей Связывающая МО с минимальной
- 27. sp2-гибридизация Тригональное расположение связей электронная конфигурация sp 2 возбужденного состояния атома углерода 2p z 2p y
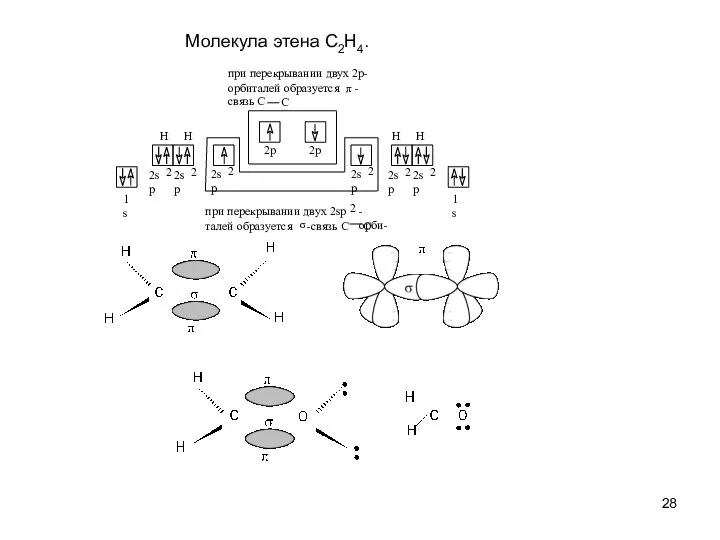
- 28. Молекула этена C2H4. 1s 2sp 2 2sp 2 H H 2sp 2 2p при перекрывании двух
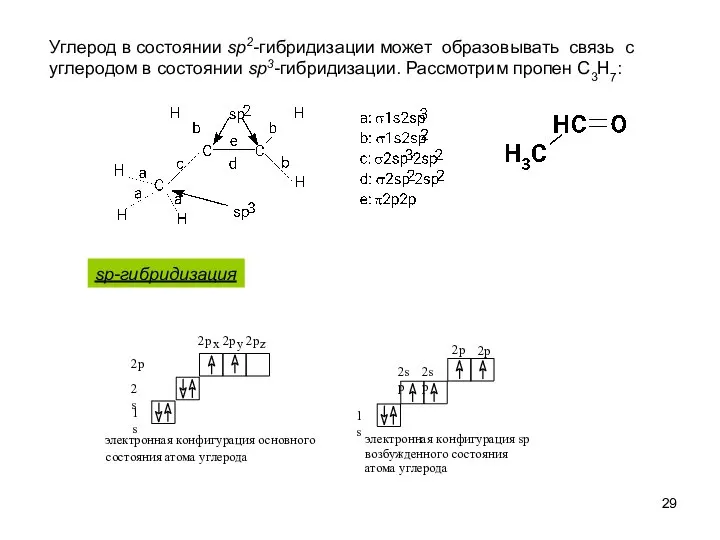
- 29. Углерод в состоянии sp2-гибридизации может образовывать связь с углеродом в состоянии sp3-гибридизации. Рассмотрим пропен C3H7: sp-гибридизация
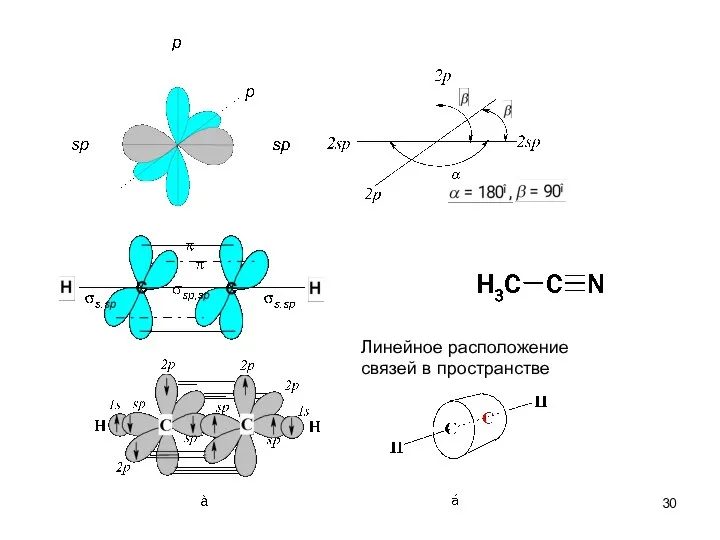
- 30. Линейное расположение связей в пространстве
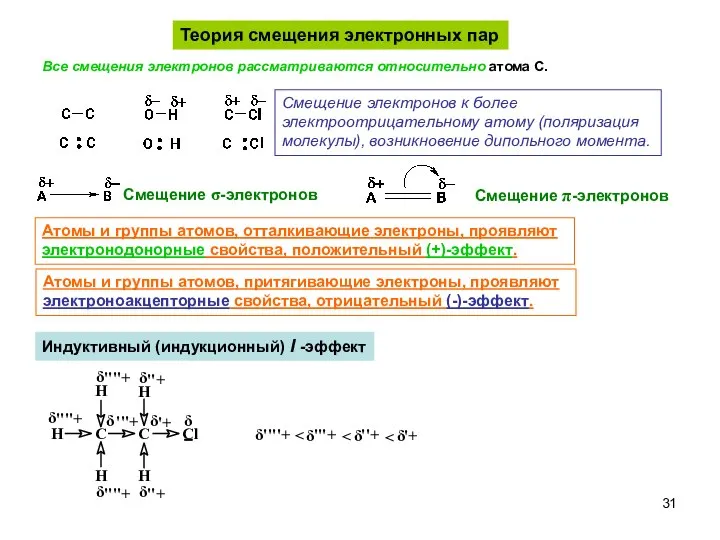
- 31. Теория смещения электронных пар Смещение электронов к более электроотрицательному атому (поляризация молекулы), возникновение дипольного момента. Смещение
- 32. Атомы и группы атомов, отталкивающие σ−электроны, проявляют электронодонорные свойства, положительный (+I)-индуктивный эффект. Атомы и группы атомов,
- 33. Мезомерный (М-)эффект Электронные эффекты в молекулах, имеющих сопряженные электронные системы. Сопряженная электронная система – система, в
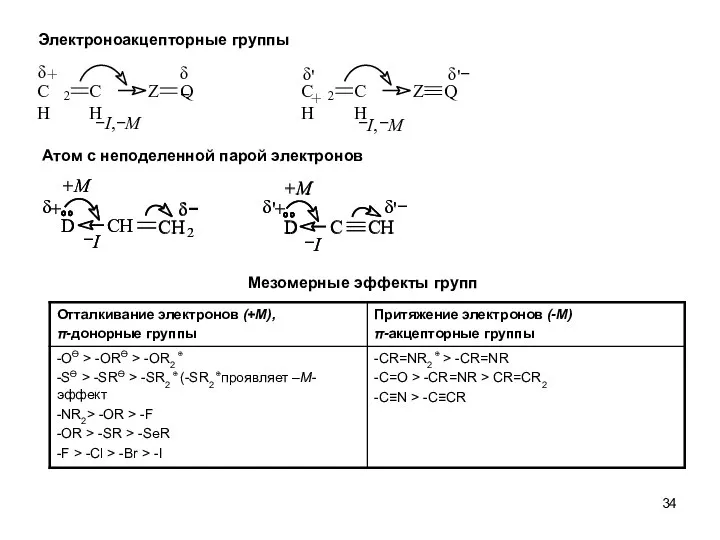
- 34. Электроноакцепторные группы Атом с неподеленной парой электронов Мезомерные эффекты групп
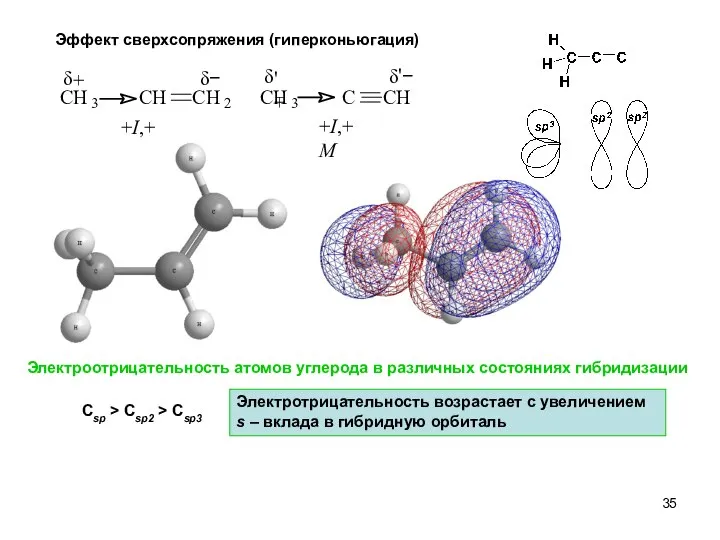
- 35. Эффект сверхсопряжения (гиперконьюгация) CH 3 CH CH 2 CH 3 C CH δ + δ− δ
- 36. Основные понятия о реакционной способности органических соединений Элементарный акт реакции это процесс, в котором происходит разрыв
- 37. Формальный заряд Атом состоит из двух частей: «остова» и внешних электронов (Дж.Н.Льюис). «Остов» это ядро атома
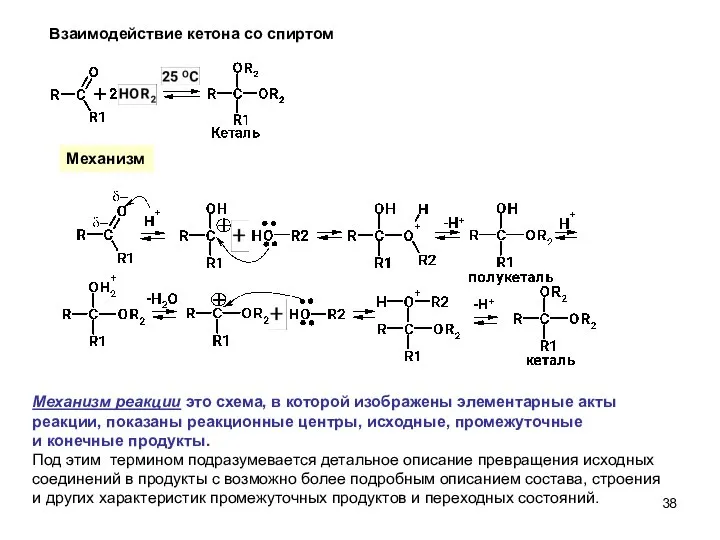
- 38. Взаимодействие кетона со спиртом Механизм Механизм реакции это схема, в которой изображены элементарные акты реакции, показаны
- 39. Энергия активации - это минимальная энергия, которой должна обладать молекула (атом, ион, радикал), чтобы преодолеть энергетический
- 40. Поверхность потенциальной энергии
- 41. Реакция образования 3-фенил-5-метил-1,2,4-оксадиазола Механизм
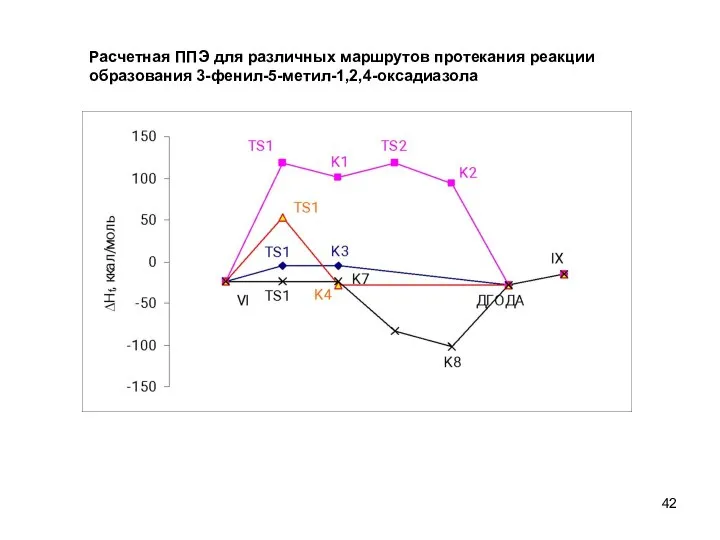
- 42. Расчетная ППЭ для различных маршрутов протекания реакции образования 3-фенил-5-метил-1,2,4-оксадиазола
- 43. Омепразол
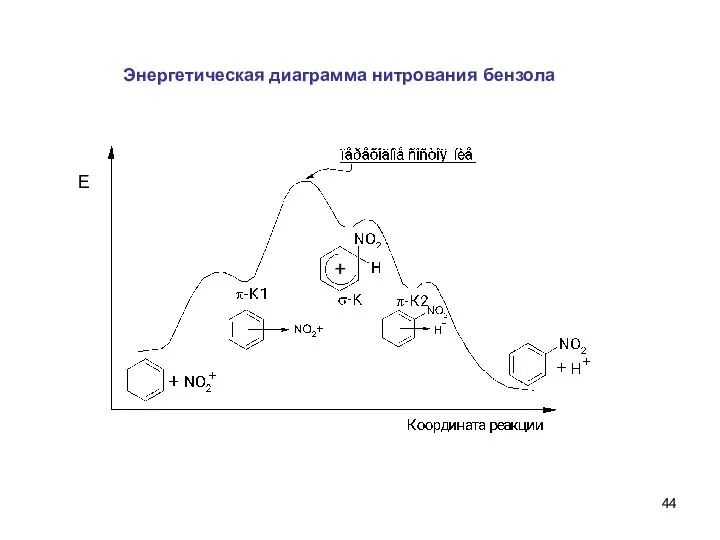
- 44. Энергетическая диаграмма нитрования бензола Е
- 45. Постулат Хэммонда. Малые изменения энергии молекулы могут соответствовать только малым изменениям структуры. Вследствие этого переходное состояние
- 46. Кинетика органических реакций. Химическая кинетика изучает скорости протекания химических реакций и их зависимость от концентрации реагирующих
- 47. Обратимые (равновесные) реакции характеризуются константой равновесия К Концепция кислотности и основности. Протолитическая концепция кислот и оснований
- 48. + Процесс ионизации основания в растворителе Sol: Кислоты характеризуются константой кислотности (K) или показателем кислотности (pKa):
- 49. Концепция кислот и оснований Д. Льюиса. Кислотами называются все молекулы и катионы - акцепторы пары электронов.
- 50. Мягкие кислоты – кислоты Льюиса, имеющие акцепторные атомы большого размера, малый положительный заряд, небольшую электроотрицательность, высокую
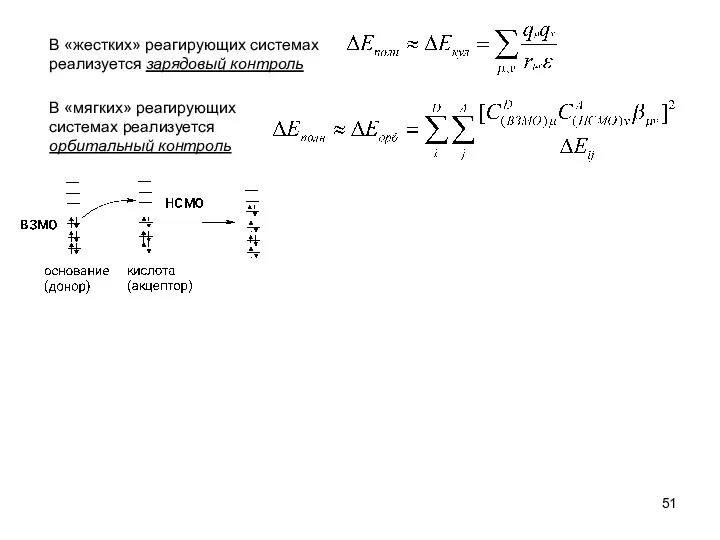
- 51. В «жестких» реагирующих системах реализуется зарядовый контроль В «мягких» реагирующих системах реализуется орбитальный контроль
- 52. ПОНЯТИЕ О "ЖМКО" НУКЛЕОФИЛЫ Жесткие кислоты – Al3+>Mg2+>Na+. Мягкие кислоты : Ag+> Cd2+>Au3+> Sn4+. Катионы Ж
- 53. Типы реакций. 1) реакции замещения (S) R − X + A R − A + X
- 54. Нуклеофильность и основность Нуклеофильность Кинетически контролируемая реакция электронной пары донора с электрофильным атомом (С), с образованием
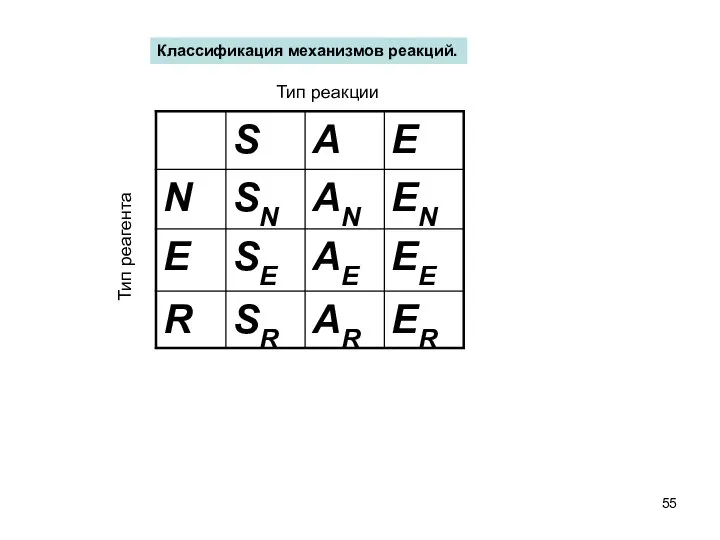
- 55. Классификация механизмов реакций. Тип реакции Тип реагента
- 56. Субстрат – исходное вещество, структура которого определяет структуру целевого продукта реакции. Реагент – исходное вещество, структура
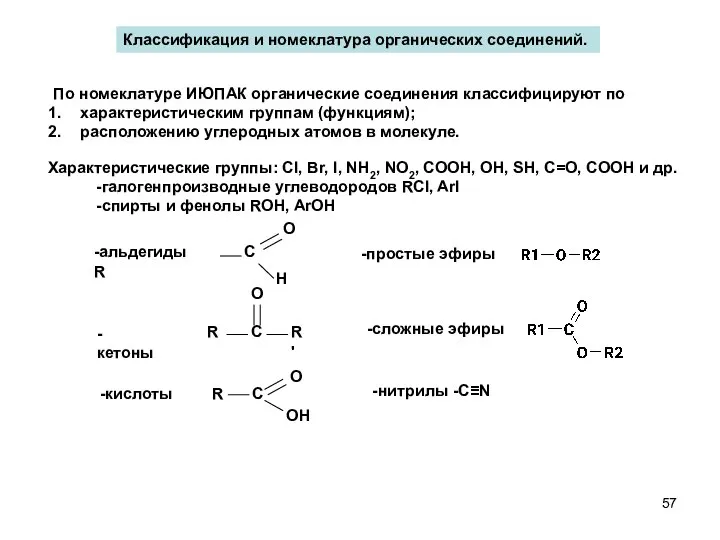
- 57. Классификация и номеклатура органических соединений. По номеклатуре ИЮПАК органические соединения классифицируют по характеристическим группам (функциям); расположению
- 58. По расположению атомов углерода в молекуле органические соединения делятся на: ациклические соединения - соединения с открытой
- 60. Скачать презентацию



































 Хімічні зв’язки
Хімічні зв’язки Минерал клинохлор. Месторождения
Минерал клинохлор. Месторождения Ковалентная неполярная химическая связь
Ковалентная неполярная химическая связь Нітрати в продуктах харчування
Нітрати в продуктах харчування  Метаморфические горные породы
Метаморфические горные породы Sample Kit Kemira 3f. External
Sample Kit Kemira 3f. External Биологическое значение элементов неорганоненов и их применение в медицине
Биологическое значение элементов неорганоненов и их применение в медицине Формирование навыков научно-исследовательской деятельности школьников 5-7 классов
Формирование навыков научно-исследовательской деятельности школьников 5-7 классов Физические и химические явления
Физические и химические явления Синтетические лекарственные средства
Синтетические лекарственные средства Школьное мероприятие Д. И. Менделеев в высказываниях Автор: Ким Наталья Викторовна учитель химии
Школьное мероприятие Д. И. Менделеев в высказываниях Автор: Ким Наталья Викторовна учитель химии  Алканы. Строение алканов
Алканы. Строение алканов Разработка технологии получения раствора коагулянта в условиях филиала «Азот» АО «ОХК «УРАЛХИМ»
Разработка технологии получения раствора коагулянта в условиях филиала «Азот» АО «ОХК «УРАЛХИМ» Радиоуглеродный анализ
Радиоуглеродный анализ БИОЛОГИЧЕСКИ АКТИВНЫЕ НИЗКОМОЛЕКУЛЯРНЫЕ ВЕЩЕСТВА
БИОЛОГИЧЕСКИ АКТИВНЫЕ НИЗКОМОЛЕКУЛЯРНЫЕ ВЕЩЕСТВА  Презентация Вещества и их свойства
Презентация Вещества и их свойства Химические свойства хрома и его соединений
Химические свойства хрома и его соединений Свинец. Строение атома свинца
Свинец. Строение атома свинца Лекция 10. Химия s-элементов
Лекция 10. Химия s-элементов Аттестационная работа. Влияние электромагнитного излучения смартфонов на жизнедеятельность микроорганизмов
Аттестационная работа. Влияние электромагнитного излучения смартфонов на жизнедеятельность микроорганизмов Медициналық тәжірибедегі потенциометриялар
Медициналық тәжірибедегі потенциометриялар Презентация по Химии "Презентация Войди в природу другом" - скачать смотреть
Презентация по Химии "Презентация Войди в природу другом" - скачать смотреть  Наноструктурированные тонкие пленки суперсплавов Mo, W и Re с 3d6-8 металлами
Наноструктурированные тонкие пленки суперсплавов Mo, W и Re с 3d6-8 металлами Гидрокаталитические процессы
Гидрокаталитические процессы Гидролиз. Фармацевтический филиал ГБОУ СПО Сомк
Гидролиз. Фармацевтический филиал ГБОУ СПО Сомк Алканы. Задания
Алканы. Задания Применение закона действующих масс к окислительно-восстановительным равновесиям. (Лекция 6)
Применение закона действующих масс к окислительно-восстановительным равновесиям. (Лекция 6) Колообіг води Виконав Проданчук Олег Учень 10-А класу
Колообіг води Виконав Проданчук Олег Учень 10-А класу