Содержание
- 2. Основания
- 3. Основания KOH, Ca(OH)2, Al(OH)3
- 4. Определение KOH, Ca(OH)2, Al(OH)3
- 5. Н2О или Н-ОН «гидро» – от греческого hydor – вода первая составная часть сложных слов, обозначающая:
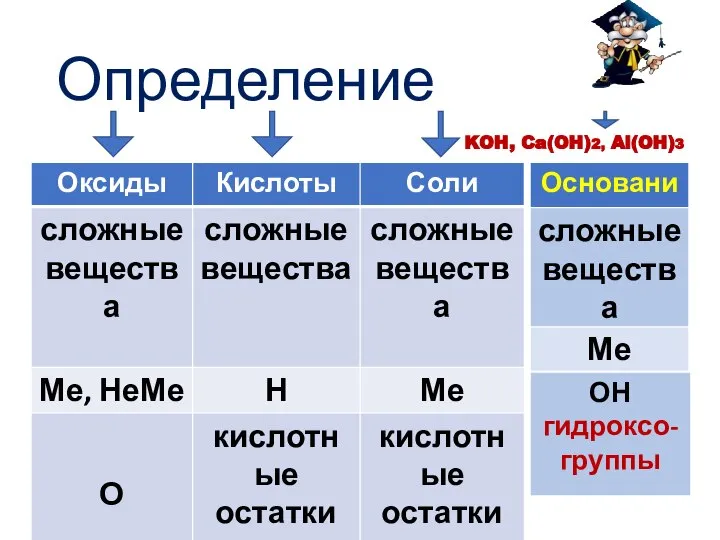
- 6. Определение Основания – сложные вещества, состоящие из атомов металлов и одной или нескольких гидроксогрупп (ОН)
- 7. ОН - гидроксогруппа KOH, Ca(OH)2, Al(OH)3 Как можно определить валентность гидроксогруппы? Вывод: валентность гидроксогруппы – l
- 8. Названия ОН - гидроксогруппа «гидроксид» + «металла» + (валентность, если переменная) Cu(OH)2 – гидроксид меди (ll)
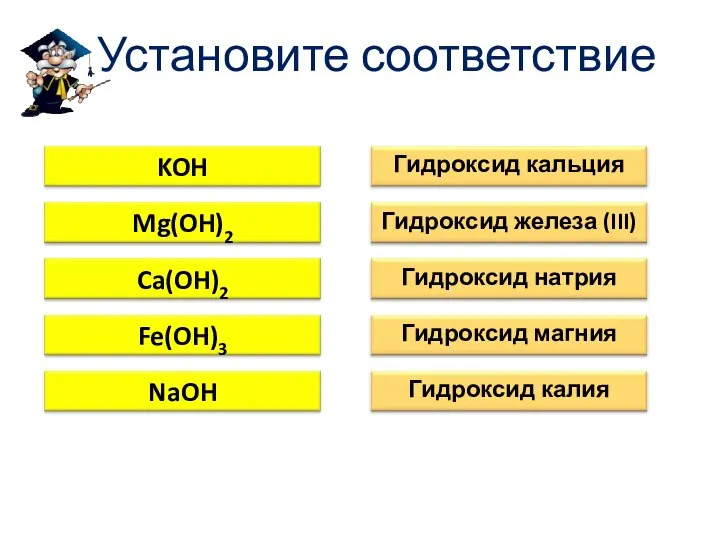
- 9. Установите соответствие
- 10. Назовите основания Cu(OH)2 – Ba(OH)2 – Al(OH)3 – LiOH – Zn(OH)2 – гидроксид меди (ll) гидроксид
- 11. Составьте формулы оснований Гидроксид натрия – Гидроксид железа(ll) – Гидроксид алюминия – lll Na (OH) l
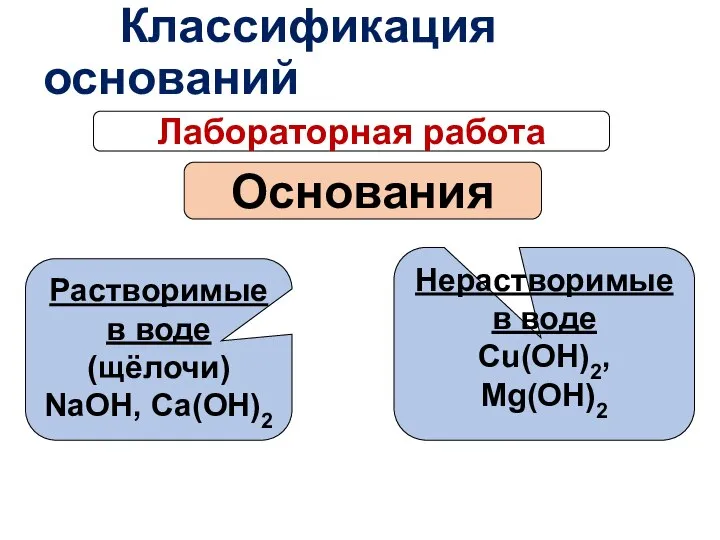
- 13. Нерастворимые в воде Cu(OH)2, Mg(OH)2 Растворимые в воде (щёлочи) NaOH, Ca(OH)2 Основания Классификация оснований Лабораторная работа
- 14. Действие индикаторов Лабораторная работа кислая среда лакмус + НCl + НCl Фенол фталеин лакмус Фенол фталеин
- 15. Упражнение Из предложенных веществ укажите формулы оснований, распределите их по группам на растворимые (щёлочи) и нерастворимые
- 16. Самопроверка Растворимые основания - щёлочи KOH NaOH Ba(OH)2 Нерастворимые основания Fe(OH)3 Mg(OH)2 Cu(OH)2 Дать названия основаниям
- 17. Домашнее задание
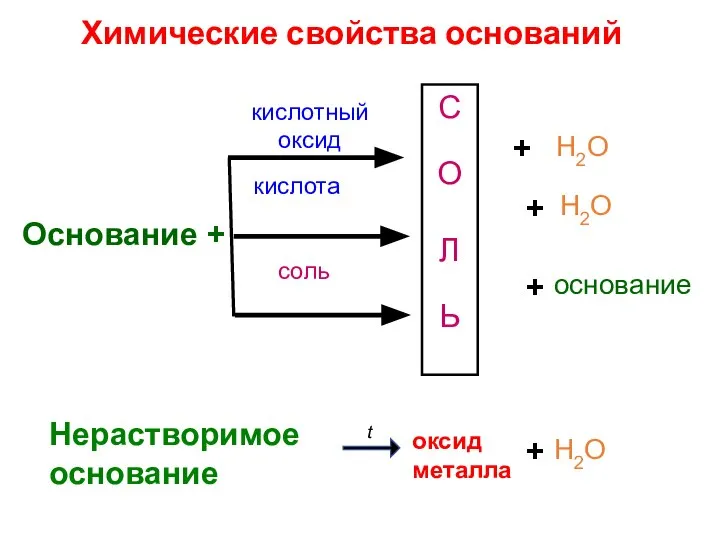
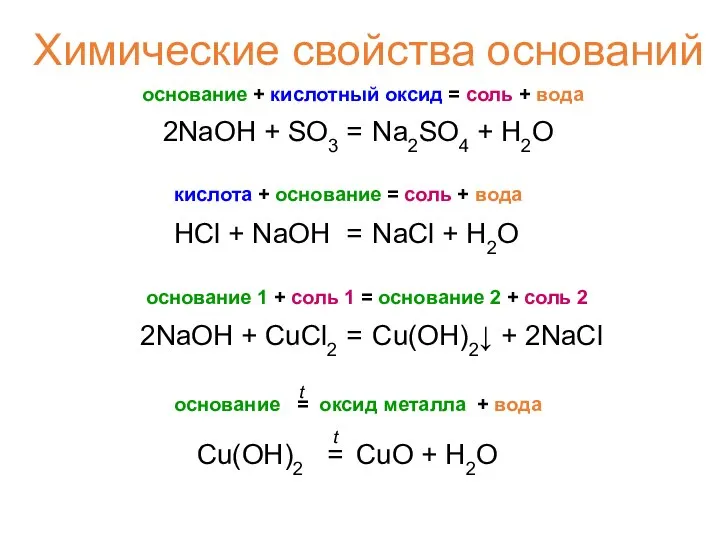
- 19. Химические свойства оснований Основание + С О Л Ь кислотный оксид кислота соль + Н2О Н2О
- 20. Химические свойства оснований основание + кислотный оксид = соль + вода 2NaOH + SO3 = Na2SO4
- 25. Скачать презентацию

















 Общие понятия и определения опасных химических веществ. Модуль 1.1
Общие понятия и определения опасных химических веществ. Модуль 1.1 Химическая посуда и лабораторное оборудование
Химическая посуда и лабораторное оборудование Природный газ Презентацию подготовили ученики 11-А класса Алчевской ИТГ Мозолевская Анастасия, Ткаченко Анастасия, Тульнов
Природный газ Презентацию подготовили ученики 11-А класса Алчевской ИТГ Мозолевская Анастасия, Ткаченко Анастасия, Тульнов  Растворы электролитов
Растворы электролитов Физико-математические основы химии: Количество вещества, Молярная масса, Молярный объём, Число Авогадро
Физико-математические основы химии: Количество вещества, Молярная масса, Молярный объём, Число Авогадро Генезис различных типов промежуточных фаз. Теория плотнейших упаковок
Генезис различных типов промежуточных фаз. Теория плотнейших упаковок Алмаз. Внутренняя структура алмаза
Алмаз. Внутренняя структура алмаза Жесткость воды
Жесткость воды Углекислый газ
Углекислый газ Трифенилметановые красители
Трифенилметановые красители Муниципальное образовательное учреждение «Лицей №3» Научно-исследовательская работа по химии «Получение ароматических масел»
Муниципальное образовательное учреждение «Лицей №3» Научно-исследовательская работа по химии «Получение ароматических масел» Электролитическая диссоциация
Электролитическая диссоциация Мысты электролитті тазалау
Мысты электролитті тазалау Классификация неорганических веществ
Классификация неорганических веществ Химические уравнения
Химические уравнения Презентация по Химии "Золото" - скачать смотреть бесплатно
Презентация по Химии "Золото" - скачать смотреть бесплатно Строение молекул некоторых широко распространенных гербицидов
Строение молекул некоторых широко распространенных гербицидов Функции белков «Жизнь – это способ существования белковых тел». Ф.Энгельс
Функции белков «Жизнь – это способ существования белковых тел». Ф.Энгельс Классификация и номенклатура органических соединений. (Лекция 1)
Классификация и номенклатура органических соединений. (Лекция 1) Поняття про лікарські препарати Підготували Стебко Марія, Бондар Аліна 11-Ф
Поняття про лікарські препарати Підготували Стебко Марія, Бондар Аліна 11-Ф  Загрязнение пищевых продуктов пестицидами
Загрязнение пищевых продуктов пестицидами Лавсан (полиэтилентерефталат)
Лавсан (полиэтилентерефталат) Предмет и задачи химии
Предмет и задачи химии Electron configuration and periodicity
Electron configuration and periodicity Всасывание продуктов гидролиза липидов в тонком кишечнике. Ресинтез жиров. Образование смешанных мицелл
Всасывание продуктов гидролиза липидов в тонком кишечнике. Ресинтез жиров. Образование смешанных мицелл Продолжение лекции «Химическая связь»
Продолжение лекции «Химическая связь» Химия в решении сырьевой проблемы
Химия в решении сырьевой проблемы Тағамдық және биологиялық белсенді қоспалар туралы жалпы мағлұматтар
Тағамдық және биологиялық белсенді қоспалар туралы жалпы мағлұматтар