Содержание
- 2. сформировать понятие об основаниях как электролитах; рассмотреть классификацию оснований по различным признакам; познакомить практически с химическими
- 3. ЗАДАЧИ УРОКА: учиться проводить химические реакции и записывать уравнения химических реакций в молекулярной, полной и сокращенной
- 4. Основания - это сложные вещества, в которых атом металла связан с одной или несколькими гидроксогруппами (ОН).
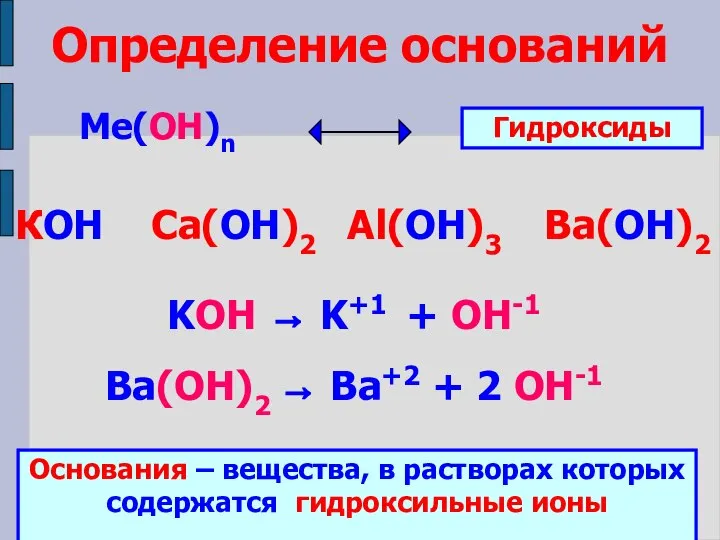
- 5. Определение оснований Ме(ОН)n КОН Ca(ОН)2 Al(ОН)3 Ba(ОН)2 Гидроксиды KOH → K+1 + OH-1 Ba(ОН)2 → Ba+2
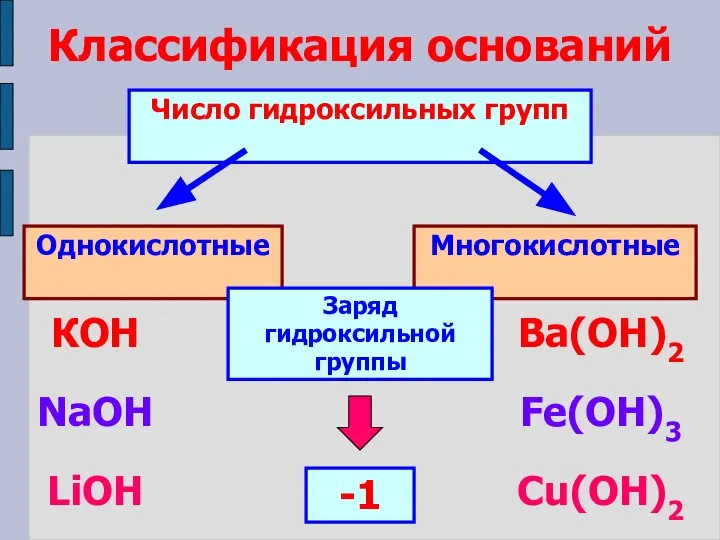
- 6. Классификация оснований Число гидроксильных групп Однокислотные Многокислотные КОН NaOH LiOH Ba(ОН)2 Fe(OH)3 Cu(OH)2 Заряд гидроксильной группы
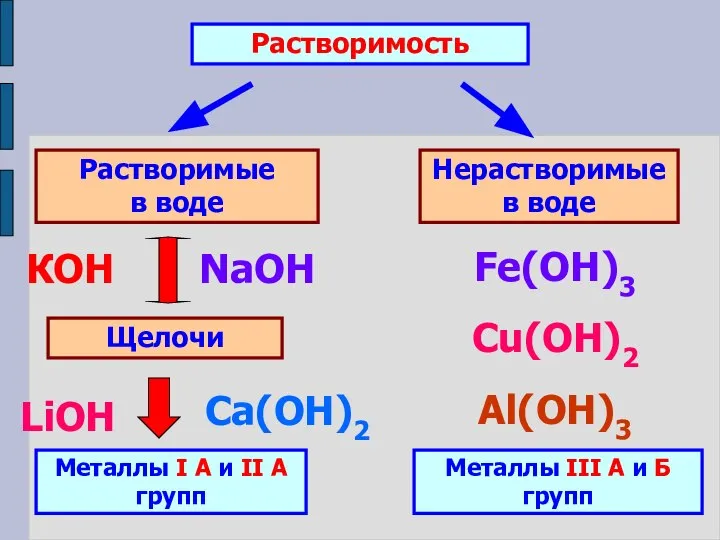
- 7. Растворимость Растворимые в воде Нерастворимые в воде Щелочи Металлы I А и II А групп КОН
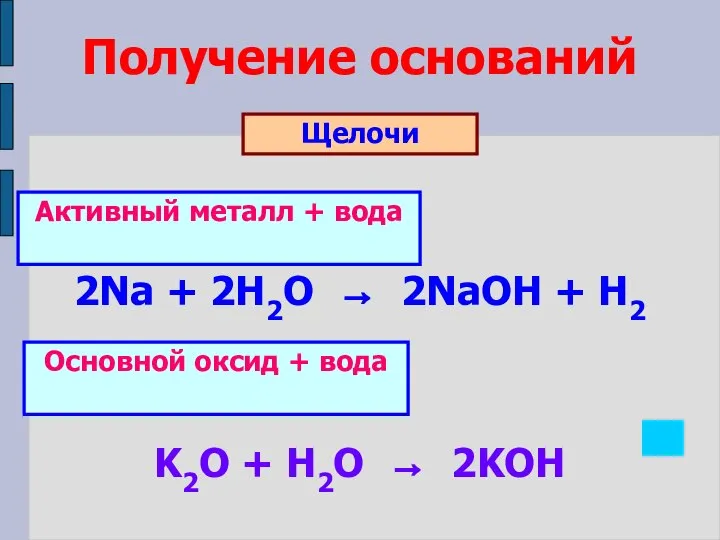
- 8. Получение оснований Щелочи 2Na + 2H2O → 2NaOH + H2 K2O + H2O → 2KOH Активный
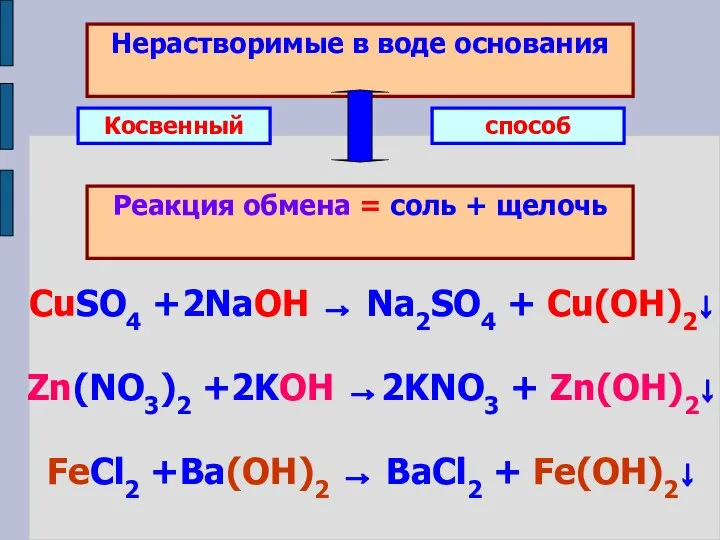
- 9. Нерастворимые в воде основания Реакция обмена = соль + щелочь Косвенный способ CuSO4 +2NaOH → Na2SO4
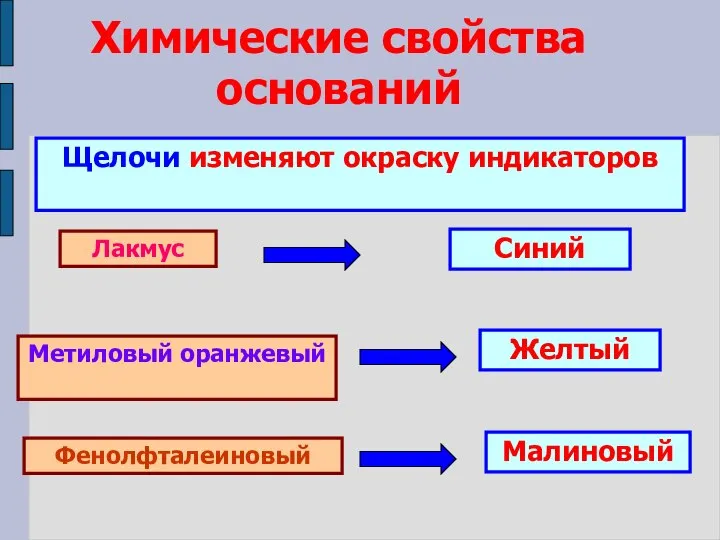
- 10. Химические свойства оснований Щелочи изменяют окраску индикаторов Лакмус Метиловый оранжевый Фенолфталеиновый Синий Желтый Малиновый
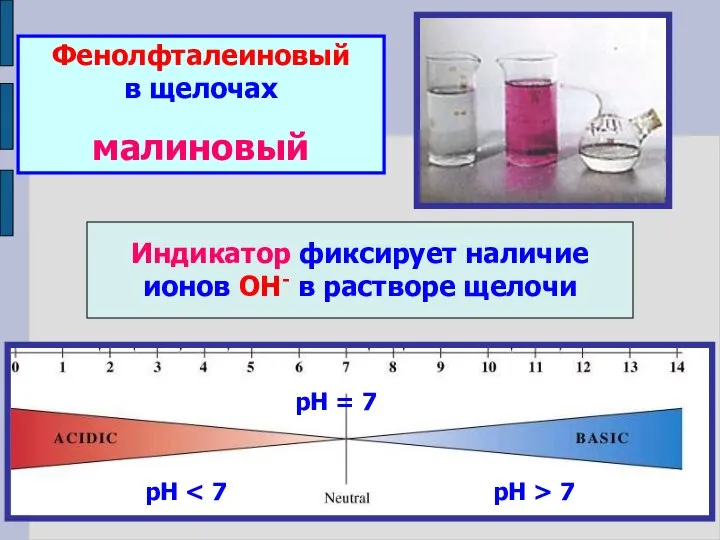
- 11. Фенолфталеиновый в щелочах малиновый Индикатор фиксирует наличие ионов ОН- в растворе щелочи рН рН = 7
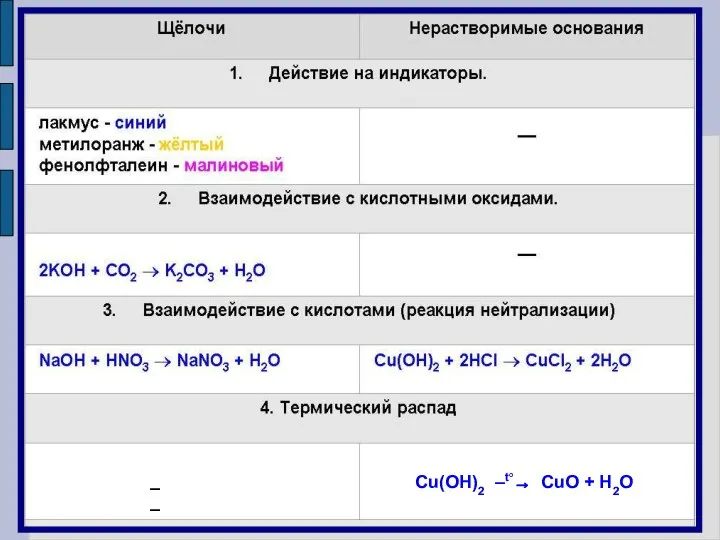
- 13. Cu(OH)2 –t°→ CuO + H2O ––
- 14. Рефлексия: Вариант 1 Вариант2 1. Даны вещества: CaO, AI(OH)3, HCI, KOH, Na2SO4, MgO, BA(OH)2, H2SO4, N2O5,
- 16. Скачать презентацию





 Научная работа по химии: «Создание рисунков на стекле методом травления плавиковой кислотой». Выполнила: Черникова Виктория 11 «
Научная работа по химии: «Создание рисунков на стекле методом травления плавиковой кислотой». Выполнила: Черникова Виктория 11 « МОУ СОШ №5 ст.Бриньковская УРОК ПО ТЕМЕ: «ЧИСТАЯ ВОДА» подготовила учитель химии Беба Е.А.
МОУ СОШ №5 ст.Бриньковская УРОК ПО ТЕМЕ: «ЧИСТАЯ ВОДА» подготовила учитель химии Беба Е.А.  Метод неразрушающего определения теплопроводности защитного покрытия из ПВХ на стальном изделии
Метод неразрушающего определения теплопроводности защитного покрытия из ПВХ на стальном изделии VA группа N и Р (подгруппа ванадия)
VA группа N и Р (подгруппа ванадия) Биологически активные низкомолекулярные вещества
Биологически активные низкомолекулярные вещества Органические производные аммиака амины
Органические производные аммиака амины Неметаллы. Смотр знаний. Для учащихся 9 классов
Неметаллы. Смотр знаний. Для учащихся 9 классов Викторина по химии
Викторина по химии Пластмассы или пластики
Пластмассы или пластики Нефть
Нефть Фізичні та хімічні явища
Фізичні та хімічні явища Основные пути внутриклеточного метаболизма углеводов
Основные пути внутриклеточного метаболизма углеводов Метаболізм ліпідів. Метаболізм білків. Стероїди. (Лекція 2)
Метаболізм ліпідів. Метаболізм білків. Стероїди. (Лекція 2) Синтез лоратадина
Синтез лоратадина EdExcel Unit C2 – Discovering Chemistry
EdExcel Unit C2 – Discovering Chemistry Кислоты
Кислоты Коррозия металлов
Коррозия металлов Жиры – биологически важные органические соединения Работа ученицы 11а класса МБОУ СОШ № 26 Ногинского района Московской области
Жиры – биологически важные органические соединения Работа ученицы 11а класса МБОУ СОШ № 26 Ногинского района Московской области  Тканые армирующие материалы
Тканые армирующие материалы Соли. Классификация сложных веществ
Соли. Классификация сложных веществ Органические и неорганические вещества
Органические и неорганические вещества Презентация по Химии "Защита зоны электродуговой сварки от окисления" - скачать смотреть
Презентация по Химии "Защита зоны электродуговой сварки от окисления" - скачать смотреть  Моделирование фазовых систем. Тройные взаимные системы
Моделирование фазовых систем. Тройные взаимные системы Аттестационная работа. Исследовательская деятельность на уроках химии (8 -9 классы). Исследование речки Беленькой
Аттестационная работа. Исследовательская деятельность на уроках химии (8 -9 классы). Исследование речки Беленькой Азолы. Гетероциклы с двумя гетероатомами
Азолы. Гетероциклы с двумя гетероатомами Соли. CaSO4 - Сульфат кальция
Соли. CaSO4 - Сульфат кальция Ювелирная работа – изысканный шедевр
Ювелирная работа – изысканный шедевр Магний. Электронное строение атома Mg
Магний. Электронное строение атома Mg