Содержание
- 2. 24 Mg +12 0 2e 8e 2e 1s2 2s2 2p6 3s2 Краткая электронная запись 1s2 2s2
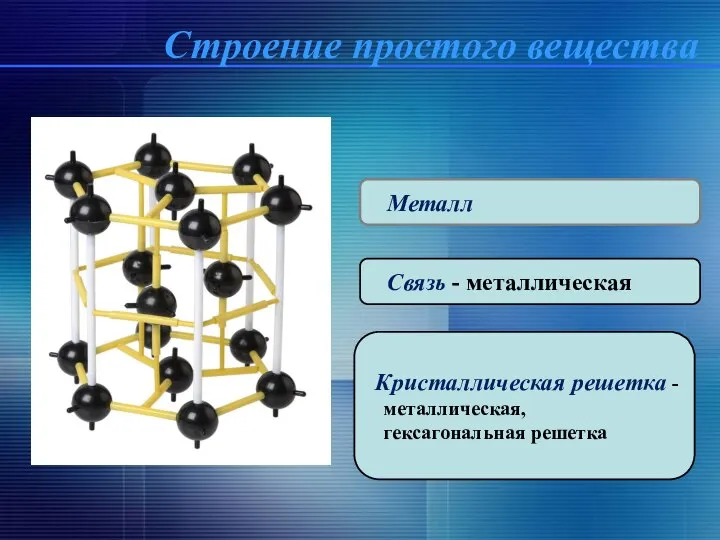
- 3. Металл Связь - металлическая Кристаллическая решетка - металлическая, гексагональная решетка Строение простого вещества
- 4. Физические свойства Mg
- 5. 2Mg + O2 = 2MgO t Mg + S = Mg S C неметаллами ( кислородом,
- 6. Горение Mg в кислороде 2Mg + O2 = 2MgO 2Mg + O2 = 2MgO
- 7. Горение Mg в воде Что будет, если тушить магний водой? На заводе по переработке вторичного сырья
- 8. Горение Mg в хлоре Mg + Cl2 = MgCl2
- 9. Вспышка смеси Mg + AgNO3 от капли воды 3Mg + AgNO3 = 3MgO + 0.5N2 +
- 10. «Горение магния на воздухе» 2Mg + O2 = 2MgO
- 11. Магнийтермия Магнийтермия – получение металлов восстановлением оксидов металлов магнием, которое сопровождается выделением значительного количества теплоты. 4Mg+
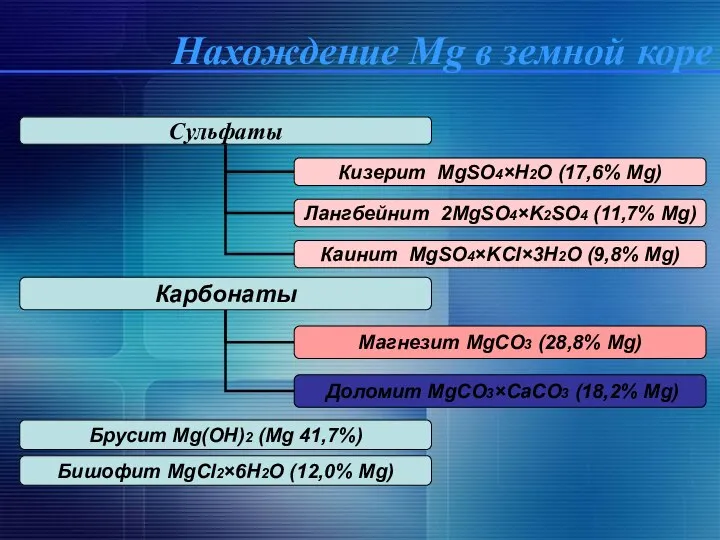
- 12. Нахождение Mg в земной коре
- 13. Получение Mg
- 14. Применение Mg и его сплавов
- 16. Скачать презентацию











 Ядра и частицы
Ядра и частицы Водородная связь
Водородная связь Этанол. Одноатомный спирт
Этанол. Одноатомный спирт Химия полимерных материалов для буровых растворов. Лекция 3. Технологические жидкости для бурения скважин
Химия полимерных материалов для буровых растворов. Лекция 3. Технологические жидкости для бурения скважин Классификация неорганических веществ
Классификация неорганических веществ Презентация по Химии "Патофизиология аритмий сердца ПАТОФИЗИОЛОГИЯ АРИТМИЙ СЕРДЦА" - скачать смотреть бесплатно
Презентация по Химии "Патофизиология аритмий сердца ПАТОФИЗИОЛОГИЯ АРИТМИЙ СЕРДЦА" - скачать смотреть бесплатно Дизельное топливо
Дизельное топливо Гидролиз солей
Гидролиз солей Дисперсные системы
Дисперсные системы Синтетические лекарственные препараты
Синтетические лекарственные препараты Неорганическое композиционное антикоррозионное покрытие для защиты стальных деталей и особенности его формирования
Неорганическое композиционное антикоррозионное покрытие для защиты стальных деталей и особенности его формирования Образовательная программа дополнительного образования «Химия в центре наук»
Образовательная программа дополнительного образования «Химия в центре наук» Configuratia electronica. Sistemul periodic al elementelor. (Curs 3)
Configuratia electronica. Sistemul periodic al elementelor. (Curs 3) Хромотография, явления, атомы и молекулы. 8 класс
Хромотография, явления, атомы и молекулы. 8 класс Дюралюминий. Дюраль
Дюралюминий. Дюраль Роль металлов в истории человеческой цивилизации
Роль металлов в истории человеческой цивилизации Положение металлов в Периодической системе Д.И. Менделеева. Особенности строения атомов, свойства
Положение металлов в Периодической системе Д.И. Менделеева. Особенности строения атомов, свойства Кремний – бог неорганической природы
Кремний – бог неорганической природы Игра по химии Разработала учитель химии МОУ «Яльчикская СОШ» Левая В.Н.
Игра по химии Разработала учитель химии МОУ «Яльчикская СОШ» Левая В.Н. Металлы и их соединения
Металлы и их соединения Биогеохимиялық шет аймақтар туралы түсінік
Биогеохимиялық шет аймақтар туралы түсінік Аминокислоты Модели молекул
Аминокислоты Модели молекул Органическая химия
Органическая химия Обмен нуклеотидов. Матричные биосинтезы
Обмен нуклеотидов. Матричные биосинтезы Основы безопасности при уничтожении химического оружия
Основы безопасности при уничтожении химического оружия Химические волокна. Свойства и технология производства
Химические волокна. Свойства и технология производства Чистые вещества и смеси Способы разделения смесей Цели: 1. Выяснить какое вещество считают чистым. 2. Что такое смесь? Какие бы
Чистые вещества и смеси Способы разделения смесей Цели: 1. Выяснить какое вещество считают чистым. 2. Что такое смесь? Какие бы Минеральные удобрения
Минеральные удобрения