Содержание
- 2. Цель урока: Изучить способы получения водорода в лаборатории и промышленности. Рассмотреть основные области применения водорода.
- 3. Получение водорода в промышленности Очевидно, что при огромных объемах промышленного производства сырьем для получения водорода должны
- 4. Получение водорода в промышленности 1. В основном получают из природного газа путем конверсии (превращения) под действием
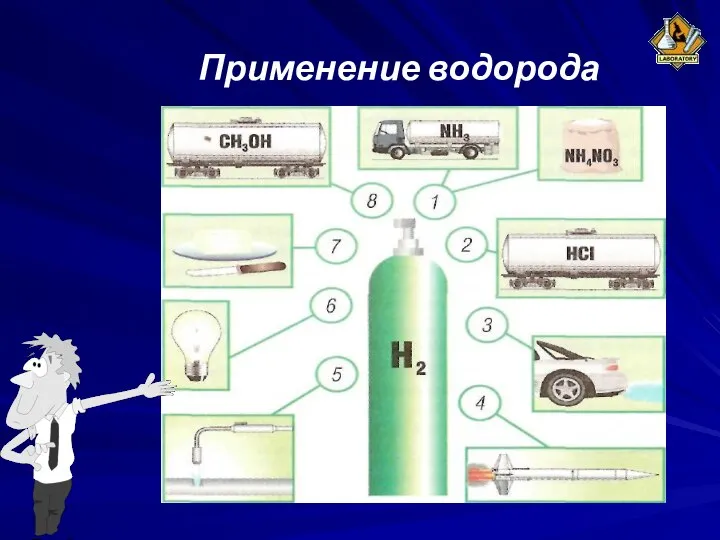
- 5. Применение водорода
- 6. Применение водорода 1 — производство минеральных удобрений 2 — получение соляной кислоты; 3 — водород —
- 7. Выводы: B промышленности для получения водорода используют доступное и дешевое сырье — природный газ, каменный уголь
- 8. Домашнее задание Параграф 31, упр. на странице 134; повторить материал с 25-31 параграф включительно.
- 9. Список использованной литературы: Ерёмин В.В., А.А. Дроздов А.А., Н.Е. Кузьменко Н.Е., В.В. Лунин В.В. Химия 8
- 10. Вопросы: Какие способы получения водорода используют в промышленности? Почему в лаборатории водород получают разложением воды с
- 11. Допиши химические реакции и укажи их тип: 1. H2O2 = 6. HgO= 2. S + O2=
- 12. Ответы: 1. H2O2=2H2O+O2 6. 2HgO=Hg+O2 2. S + O2=SO2 7.4Al +3O2=2Al2O3 3.2Al+6HCl=2AlCl3+3H2 8. Zn+H2SO4=ZnSO4+H2 4. HgO
- 14. Скачать презентацию










 Мышьяк. Висмут. Сурьма
Мышьяк. Висмут. Сурьма Электрохимическая защита
Электрохимическая защита Карбоновые кислоты
Карбоновые кислоты Кислотные и основные свойства биоорганических соединений. (Лекция 2)
Кислотные и основные свойства биоорганических соединений. (Лекция 2) Островные силикаты (Орто)
Островные силикаты (Орто) Производство фенолформальдегидной смолы
Производство фенолформальдегидной смолы Элементы V А группы. Азот и его соединения
Элементы V А группы. Азот и его соединения Валетные состояния атома углерода
Валетные состояния атома углерода Жесткость воды и способы ее устранения
Жесткость воды и способы ее устранения Стимулсезімтал сополимерлердің полимерлік комплексін зерттеу
Стимулсезімтал сополимерлердің полимерлік комплексін зерттеу Смесители. Пропеллерная мешалка
Смесители. Пропеллерная мешалка Титан. Технология титана
Титан. Технология титана Классификация опасных грузов
Классификация опасных грузов Химия лекция (вебинар)
Химия лекция (вебинар) Кислород. Происхождение слова Кислород
Кислород. Происхождение слова Кислород Катализаторы
Катализаторы Презентация по Химии "Законы газового состояния вещества" - скачать смотреть
Презентация по Химии "Законы газового состояния вещества" - скачать смотреть  Выращивание кристаллов из соли
Выращивание кристаллов из соли Релаксационные свойства полимеров
Релаксационные свойства полимеров Создание косметических средств
Создание косметических средств Взаимосвязь между классами неорганических веществ
Взаимосвязь между классами неорганических веществ Степень окисления. Бинарные соединения металлов и не металлов: оксиды, хлориды, сульфиды и др.
Степень окисления. Бинарные соединения металлов и не металлов: оксиды, хлориды, сульфиды и др.  Бу́ферные систе́мы кро́ви
Бу́ферные систе́мы кро́ви Детонаційна стійкість бензину Підготувала учениця 11-Б класу ЖЕЛ №24 Гуленко Катерина
Детонаційна стійкість бензину Підготувала учениця 11-Б класу ЖЕЛ №24 Гуленко Катерина  Особенности переваривания и всасывания липидов. β – окисление жирных кислот в митохондриях
Особенности переваривания и всасывания липидов. β – окисление жирных кислот в митохондриях Atomic structure
Atomic structure Эндогенная серия. Скарновая группа
Эндогенная серия. Скарновая группа Стекло — твердое неорганическое вещество
Стекло — твердое неорганическое вещество