Содержание
- 2. Жидкие растворы подразделяют на растворы электролитов, способные проводить электрический ток, и растворы неэлектролитов, которые не электропроводны.
- 3. К сильным электролитам в водных растворах принадлежит подавляющее большинство солей, щелочи (основания s-элементов, кроме Ве(ОН)2 и
- 4. СЛАБЫЕ ЭЛЕКТРОЛИТЫ. КОНСТАНТА И СТЕПЕНЬ ДИССОЦИАЦИИ В растворах слабых электролитов устанавли-вается равновесие между недиссоциированными молекулами и
- 5. Если обозначить общую концентрацию электролита, например, слабой кислоты НА через С моль/л, то концентрации ионов Н+
- 6. Если степень диссоциации а ≤ 1, то при приближен-ных вычислениях можно принять, что 1-а ≈ 1.
- 7. Если степень диссоциации α СЛАБЫЕ ЭЛЕКТРОЛИТЫ. КОНСТАНТА И СТЕПЕНЬ ДИССОЦИАЦИИ Са2 + Ка - К =
- 8. Пример 1. Степень диссоциации уксусной кислоты в 0,1 М растворе равна 1,32•10-2. Найти константу диссоциации кислоты
- 9. Решение 1. Подставим данные задачи в уравнение закона разбавления К = α2С/(1- α) = (1,32•10-2)2 •0,1/(1-
- 10. ВЛИЯНИЕ ОДНОИМЕННЫХ ИОНОВ НА РАВНОВЕСИЕ ДИССОЦИАЦИИ Как повлияет добавление к раствору уксусной кислоты ее соли (например,
- 11. Вывод. Степень диссоциации слабого электролита уменьшается при добавлении к нему сильного электролита с одноименным ионом. ВЛИЯНИЕ
- 12. ДИССОЦИАЦИЯ МНОГООСНОВНЫХ КИСЛОТ В растворах многоосновных кислот (а также оснований, содержащих несколько ОН-групп) устанавливаются ступенчатые равновесия.
- 13. Диссоциация электролита приводит к тому, что общее число частиц растворенного вещества (молекул и ионов) в растворе
- 14. Эффект увеличения числа частиц в результате диссоциации учитывается в расчетах введением поправочного коэффициента Вант-Грффа i: Росм
- 15. СИЛЬНЫЕ ЭЛЕКТРОЛИТЫ. АКТИВНОСТЬ ИОНОВ В растворах сильных электролитов даже при малой концентрации электролита заметно проявляются силы
- 16. Коэффициенты активности ионов зависят от состава и концентрации раствора, от заряда и природы иона и от
- 17. ИОННОЕ ПРОИЗВЕДЕНИЕ ВОДЫ. ВОДОРОДНЫЙ ПОКАЗАТЕЛЬ Вода, будучи очень слабым электролитом, в незна-чительной степени диссоциирует, образуя ионы
- 18. Поскольку степень диссоциации воды очень мала, то равновесная концентрация недиссоциированных молекул воды [Н2О] с достаточной точностью
- 19. Константа КВ, равная произведению концентраций ионов Н+ и ОН‾ , представляет собой постоянную при данной температуре
- 20. Вместо концентраций ионов Н+ и ОН‾ пользуются их десятичными логарифмами, взятыми с обратным знаком; эти величины
- 21. ВОДОРОДНЫЙ ПОКАЗАТЕЛЬ СРЕДЫ. РН где СН+ — равновесная молярная концентрация Н+, fН+ — коэффициент активности ионов
- 22. Для расчета рН сильных кислот находят активность ионов водорода аН+ по формуле аН+ = fН+[H+], ВОДОРОДНЫЙ
- 23. ПРИМЕРЫ РЕШЕНИЯ ЗАДАЧ
- 24. Пример 1. Константа диссоциации цианово-дорода (синильной кислоты) равна 7,9 • 10-10. Найти степень диссоциации HCN в
- 25. Р е ш е н и е 1. Поскольку константа диссоциации HCN очень мала, то для
- 26. Пример 2. Вычислить концентрацию ионов водорода в 0,1 М растворе хлорноватистой кислоты НОСl (К = 5∙10-8
- 27. Р е ш е н и е 2. Найдем степень диссоциации НОСl: ПРИМЕРЫ РЕШЕНИЯ ЗАДАЧ Отсюда:
- 28. ПРИМЕРЫ РЕШЕНИЯ ЗАДАЧ Пример 3. Оцените степень диссоциации α в 0,005 М и 0,05 М растворах
- 29. ПРИМЕРЫ РЕШЕНИЯ ЗАДАЧ Поскольку К2 10−4), поэтому расчет α следует проводить по строгой формуле Оствальда К
- 30. ПРИМЕРЫ РЕШЕНИЯ ЗАДАЧ (1,7·10−2)2 + 4·5·10−3·1,7·10−2 = -1,7·10−2 + 2·5·10−3 = 0,81 Расчет по приближенной формуле
- 31. ПРИМЕРЫ РЕШЕНИЯ ЗАДАЧ Расчет по приближенной формуле дает α ≈ 0,58, что существенно отличается от рассчитанного
- 32. Пример 4. Во сколько раз уменьшится концентрация ионов водорода в 0,2 М растворе муравьиной кислоты НСООН
- 33. Р е ш е н и е 4. Исходную концентрацию ионов Н+ в растворе (до добавления
- 34. K = [H+][CH3COO‾] [CH3COOH] ПРИМЕРЫ РЕШЕНИЯ ЗАДАЧ = х(0,1+ х) (0,2 - х) = 1,8∙10-4 Так
- 35. Пример 5. Раствор, содержащий 0,85 г хлорида цинка в 125 г воды кристаллизуется при -0,23°С. Определить
- 36. Р е ш е н и е 5. Найдем прежде всего моляльную концентрацию (го) соли в
- 37. Р е ш е н и е 5. i = ∆Tкрист/ ∆Tкрист. выч = 0,23/0,093 =
- 38. Пример 6. Найти изотонический коэффи-циент для 0,2 М раствора электролита, если известно, что в 1 л
- 39. Р е ш е н и е 6. Число молекул электролита, взятых для приготовления 1 л
- 40. Пример 7. Вычислить ионную силу и активность ионов в растворе, содержащем 0,01 моль/л MgSО4 и 0,01
- 41. Р е ш е н и е 7. Ионная сила раствора равна: I = 0,5 (
- 42. Р е ш е н и е 7. ПРИМЕРЫ РЕШЕНИЯ ЗАДАЧ Теперь, пользуясь соотношением а =
- 43. ПРИМЕРЫ РЕШЕНИЯ ЗАДАЧ Пример 8. Рассчитайте рН 0,002 М раствора Н2СO3.
- 44. ПРИМЕРЫ РЕШЕНИЯ ЗАДАЧ Решение 8. При расчетах рН растворов слабых электролитов можно с достаточной точностью использовать
- 45. ПРИМЕРЫ РЕШЕНИЯ ЗАДАЧ Если принять концентрацию диссоциированных молекул Н2СO3 за х (моль/л), то, в соответствии с
- 46. ПРИМЕРЫ РЕШЕНИЯ ЗАДАЧ 2. Поскольку K1 В соответствии с уравнением диссоциации [Н+] = НСО3− и равна
- 47. ПРИМЕРЫ РЕШЕНИЯ ЗАДАЧ Пример 9. Определить активность ионов водорода и значение ран+ в 2,5 • 10-3
- 48. Р е ш е н и е 9. Для электролитов, состоящих из однозарядных ионов, значение ионной
- 49. ЗАДАЧИ ДЛЯ САМОСТОЯТЕЛЬНОГО РЕШЕНИЯ При решении задач этого раздела следует в необходимых случаях пользоваться таблицей констант
- 50. 512. Вычислить [Н+], [HSe-] и [Se2-] в 0,05 М растворе H2Se. 513. Во сколько раз уменьшится
- 51. 532. Вычислить ионную силу и активность ионов в растворе, содержащем 0,01 моль/л Са(NО3)2 и 0,01 моль/л
- 52. 549. Рассчитать рН раствора, полученного смешением 25 мл 0,5 М раствора НСl, 10 мл 0,5 М
- 53. Т Е С Т Ы
- 54. Тест 523. Как соотносятся значения осмотического давления в 0,1 М растворах KNO3 (P1) и СН3СООН (Р2):
- 55. Тест 524. Температуры кристаллизации одномо-ляльных растворов циановодорода HCN и глюкозы С6Н12О6 близки. Какой вывод можно сделать
- 56. Тест 552. Указать, какие из рядов перечисленных ниже кислот соответствуют возрастанию рН в растворах одинаковой молярной
- 57. Тест 554. Как изменится кислотность 0,2 н. раствора HCN при введении в него 0,5 моль/л KCN:
- 58. Тест 556. Сколько ионов водорода содержится в 1 мл раствора, рН которого равен 13: а) 1013;
- 60. Скачать презентацию
































![K = [H+][CH3COO‾] [CH3COOH] ПРИМЕРЫ РЕШЕНИЯ ЗАДАЧ = х(0,1+ х) (0,2](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1246245/slide-33.jpg)















![512. Вычислить [Н+], [HSe-] и [Se2-] в 0,05 М растворе H2Se.](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1246245/slide-49.jpg)








 Реакции щелочно-земельных металлов (Группа 2) – Mg, Ca
Реакции щелочно-земельных металлов (Группа 2) – Mg, Ca Терминология и основные понятия в химии высокомолекулярных соеденений
Терминология и основные понятия в химии высокомолекулярных соеденений Презентация по Химии "Палива" - скачать смотреть бесплатно
Презентация по Химии "Палива" - скачать смотреть бесплатно Композиты. Полимерные композиционные материалы
Композиты. Полимерные композиционные материалы Лед – как состояние воды
Лед – как состояние воды Тест 1.Тип кристаллической решетки у белого фосфора…. а) молекулярный б) атомный в) ионный а) молекулярный Р4 2. У фосфора…..
Тест 1.Тип кристаллической решетки у белого фосфора…. а) молекулярный б) атомный в) ионный а) молекулярный Р4 2. У фосфора….. 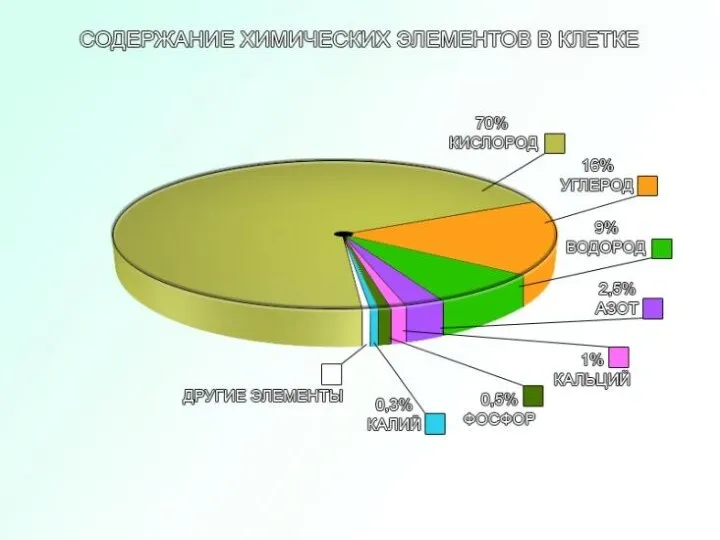 Содержание химических элементов в клетке
Содержание химических элементов в клетке Протолитическая теория кислот и оснований
Протолитическая теория кислот и оснований Простые вещества металлы
Простые вещества металлы УГЛЕВОДЫ И ЛИПИДЫ. ИХ РОЛЬ В ЖИЗНЕДЕЯТЕЛЬНОСТИ КЛЕТКИ Презентация учителя химии, биологии и экологии МОУ СОШ п.Алексеевка Беша
УГЛЕВОДЫ И ЛИПИДЫ. ИХ РОЛЬ В ЖИЗНЕДЕЯТЕЛЬНОСТИ КЛЕТКИ Презентация учителя химии, биологии и экологии МОУ СОШ п.Алексеевка Беша Презентация по Химии "Детонаційна стійкість бензину" - скачать смотреть бесплатно
Презентация по Химии "Детонаційна стійкість бензину" - скачать смотреть бесплатно Полиэтилен — термопластичный полимер этилена
Полиэтилен — термопластичный полимер этилена Алканы
Алканы «Нафта-рідке паливо» Презентація на тему:
«Нафта-рідке паливо» Презентація на тему:  Викторина по химии
Викторина по химии Возбудители колибактериоза
Возбудители колибактериоза Основные характеристи нефти и нефтеподуктов
Основные характеристи нефти и нефтеподуктов Витамины. Общая характеристика. Классификация. Витамины алифатического строения. Витамин С
Витамины. Общая характеристика. Классификация. Витамины алифатического строения. Витамин С Производство аммиака
Производство аммиака Нефть. Углеводороды
Нефть. Углеводороды Циклоалканы
Циклоалканы Радиохимия аспиранты
Радиохимия аспиранты Любовь с точки зрения лаборантов
Любовь с точки зрения лаборантов Історія виникнення мила Підготувала учениця 7-В класу Футрик Лілія
Історія виникнення мила Підготувала учениця 7-В класу Футрик Лілія  Ковалентная связь. Радикалы
Ковалентная связь. Радикалы Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Состав, строение и свойства белков
Состав, строение и свойства белков Химия элементов. Лекция 1 Общая характеристика элементов IVA-группы. Углерод и кремний
Химия элементов. Лекция 1 Общая характеристика элементов IVA-группы. Углерод и кремний