Содержание
- 2. СТРОЕНИЕ АТОМА
- 3. Студент должен: Знать: Основные положения теории строения атома (ядра и состояния электронов), формулировку периодического закона Уметь:
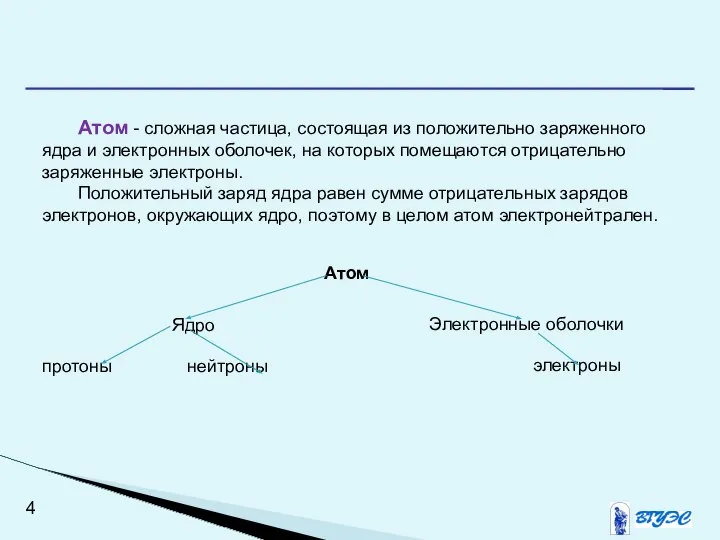
- 4. Атом - сложная частица, состоящая из положительно заряженного ядра и электронных оболочек, на которых помещаются отрицательно
- 6. Протоны, нейтроны и электроны называются элементарными частицами. Символы химических элементов представляются обычно в виде: где Х-символ
- 7. Изотопы-атомы одного химического элемента, имеющие одинаковое число протонов, но разные массовые числа (число нейтронов). Например, природный
- 8. Для строгого описания движения электронов вокруг атомного ядра необходимо использовать понятие корпускулярно- волнового дуализма электрона (электрон
- 9. Если l=0, то орбиталь называется s-орбиталь (движение электрона по сфере). При l=1 мы имеем р-орбиталь (гантелевидная
- 10. ml-магнитное квантовое число- характеризует проекцию магнитного момента электрона на внешнее магнитное поле, то есть определяет ориентацию
- 11. Атомная орбиталь- это совокупность положений электрона в атоме, характеризуемых определенными значениями главного, орбитального и магнитного квантовых
- 12. ms-спиновое квантовое число- определяет собственный момент вращения электрона. Это квантовое число вытекает не из решения уравнения
- 13. Если атом находится в основном состоянии (не обладает избыточной энергией), то его электроны занимают наиболее низкие
- 14. Графически правила Клечковского можно представить в виде:
- 15. Заполнение электронами орбиталей происходит в следующем порядке: 1s,2s,2p,3s,3p,4s,5s,4d,5p и т.д. Принцип Паули. В атоме не может
- 16. Максимальное число электронов на уровне N=2n2, где n-главное квантовое число. В связи с вышесказанным на первом
- 17. Правило Хунда. Внутри подуровня электроны заполняют орбитали таким образом, чтобы суммарному спиновое квантовое число было максимальным
- 18. Число электронов в атоме определяется порядковым номером элемента в периодической системе. Используя правила размещения электронов в
- 19. Если до полного или половинного заполнения d-подуровня (d5 или d10- конфигурации)не хватает одного электрона, то происходит
- 20. Электроны в атоме можно разделить на два типа: внутренние и внешние (валентные). Внутренние электроны занимают полностью
- 22. Скачать презентацию


















 Презентация по Химии "Увлекательные факты из жизни великого химика." - скачать смотреть бесплатно
Презентация по Химии "Увлекательные факты из жизни великого химика." - скачать смотреть бесплатно Полимеры в стоматологии. Ингредиенты полимерных стоматологических материалов
Полимеры в стоматологии. Ингредиенты полимерных стоматологических материалов :Химиялық реакциялардың кинетикалық жіктелуі.Ферментті катализ.Ферменттердің әсер ету ерекшеліктері
:Химиялық реакциялардың кинетикалық жіктелуі.Ферментті катализ.Ферменттердің әсер ету ерекшеліктері Плотность вещества
Плотность вещества Введение в химию галогенов
Введение в химию галогенов Презентация по Химии "Изучение химического состава кристаллов и синтезирование в лабораторных условиях" - скачать смотреть
Презентация по Химии "Изучение химического состава кристаллов и синтезирование в лабораторных условиях" - скачать смотреть  Жиры. Классификация жиров
Жиры. Классификация жиров Массообменные процессы
Массообменные процессы Урок - лекция с контролем в 10 классе
Урок - лекция с контролем в 10 классе 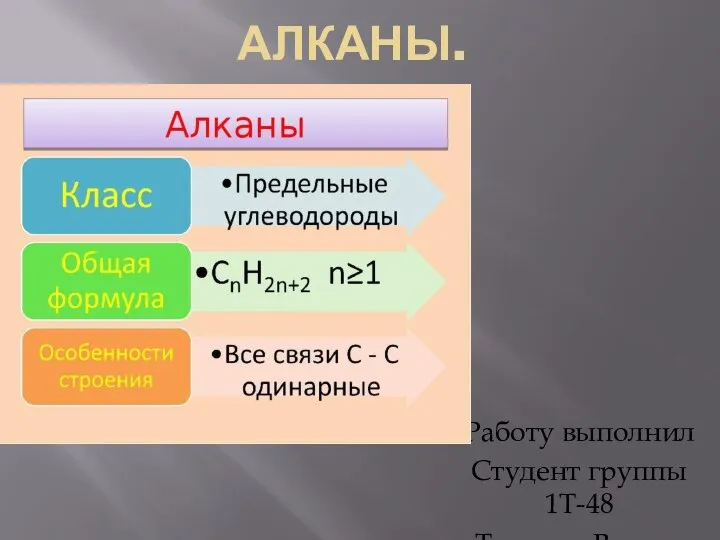 Алканы. Гомологический ряд и изомерия
Алканы. Гомологический ряд и изомерия Охорона довкілля від забруднення під час переробки нафти та кам’яного вугілля
Охорона довкілля від забруднення під час переробки нафти та кам’яного вугілля  Кинетика процессов твердофазного взаимодействия
Кинетика процессов твердофазного взаимодействия Роль Химии в жизни общества
Роль Химии в жизни общества Использование углеводородов в медицине
Использование углеводородов в медицине Виды присадок к моторным топливам
Виды присадок к моторным топливам Вебинар 1.05. Разбор заданий #стольник, #долюшка и #массовая
Вебинар 1.05. Разбор заданий #стольник, #долюшка и #массовая Отрицательное влияние азотных минеральных удобрений на почву
Отрицательное влияние азотных минеральных удобрений на почву МОУ «Каратунская СОШ с углубленным изучением отдельных предметов» Выполнила : учитель химии второй квалификационной категор
МОУ «Каратунская СОШ с углубленным изучением отдельных предметов» Выполнила : учитель химии второй квалификационной категор Химические свойства оксидов
Химические свойства оксидов Нафтопереробна промисловість України
Нафтопереробна промисловість України  Идеальный газ. Основное уравнение мкт
Идеальный газ. Основное уравнение мкт Силиактная промышленность Химия 9 класс Программа О.С. Габриэляна
Силиактная промышленность Химия 9 класс Программа О.С. Габриэляна Магматические породы и постмагматические процессы
Магматические породы и постмагматические процессы Присадки к маслам
Присадки к маслам Оборудование, инструмент и приспособления, белье для химической завивки
Оборудование, инструмент и приспособления, белье для химической завивки Презентация по Химии "Алкины" - скачать смотреть бесплатно
Презентация по Химии "Алкины" - скачать смотреть бесплатно Презентация по Химии "Всё о кремнии" - скачать смотреть
Презентация по Химии "Всё о кремнии" - скачать смотреть  Презентация по Химии "Синтетические высокомолекулярные соединения и полимеры на их основе" - скачать смотреть
Презентация по Химии "Синтетические высокомолекулярные соединения и полимеры на их основе" - скачать смотреть