Содержание
- 2. Лайфхак В каждой задаче подчеркивайте себе ключевые моменты (с чем реагировало вещество, какую порцию отобрали, какая
- 3. #стольник №34. Какую массу оксида серы (VI) следует добавить к 400 г 15 %-ного раствора серной
- 4. Написать все реакции, о которых идёт речь в задаче (после каждой реакции оставить немного места, чтобы
- 5. Шаг 2 Посчитать кол-во вещества тех веществ, у которых даны масса/объём и тд m1 (H2SO4)= =m1
- 6. 3. Внимательно посмотреть и подумать !!Замечание: если вводите неизвестные (х,y и тд), обязательно пишите что есть
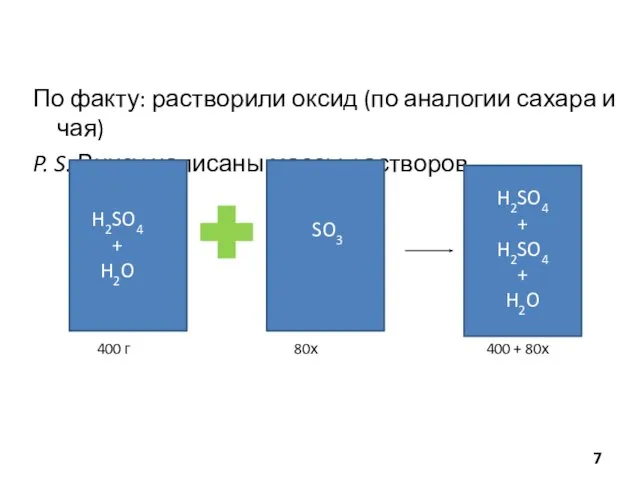
- 7. По факту: растворили оксид (по аналогии сахара и чая) P. S. Внизу написаны массы растворов SO3
- 8. 4. Составить уравнение w2 (H2SO4)= m2 (H2SO4)/m2 (p-pa H2SO4) = = 0,25 х=20/39=0,513= n (SO3) m
- 9. #стольник №35. При сгорании 4,68 г органического вещества получили 4,48 л углекислого газа (н. у.), 448
- 10. Алгоритм (обобщённый) 0. Перевести в СИ (г, л{газы} и тд) !!! Помним, что 1 л=1000 мл
- 11. t 0 2. Написать реакцию горения СхНуОzNt+aO₂ xCO₂+(y/2) H2O+(t/2)N₂
- 12. 3. Посчитать кол-ва веществ n(CO₂)=V(CO₂)/Vm=4,48 л/22,4 (л/моль)=0,2 моль = n(C в A) m(C)= n(C)*М(С)=0,2 моль*12 (г/моль)=2,4
- 13. ОБЯЗАТЕЛЬНАЯ ПРОВЕРКА m(O)=m(СхНуОzNt) - m(N) - m(C) - m(H)= 4,68 г - 0,44 г - 0,56
- 14. 4. Найти брутто-формулу В веществе СхНуОzNt : x:y:z:t= n(C): n(H): n(O): n(N)=0,2:0,44:0,08:0,04=5:11:2:1, то есть С5Н11О2N Один
- 15. 5. Нарисовать структурную формулу «При нагревании с соляной кислотой данное вещество подвергается гидролизу….» Гидролизуются только сложные
- 16. #массовая Задание 4. Электролиз 372,5 г 12%-го раствора KCl прекратили, когда на катоде выделилось 4,48 л
- 17. Алгоритм Шаг 1. Написать все уравнения реакций (катодно-анодные процессы обязательно расписывать!) К(-): 2Н2О +2е=2ОН(1-)+Н2 А(+): 2Сl(1-)-2e=Cl2
- 18. Шаг 2. Посчитать кол-ва веществ n(H2)= V(Н2)/ Vm= 4,48 л /22,4 (л/моль)=0,2 моль => По уравнению
- 19. #долюшка Задание 5. Для полного растворения смеси железа и оксида железа (II) потребовалось 511 г 5
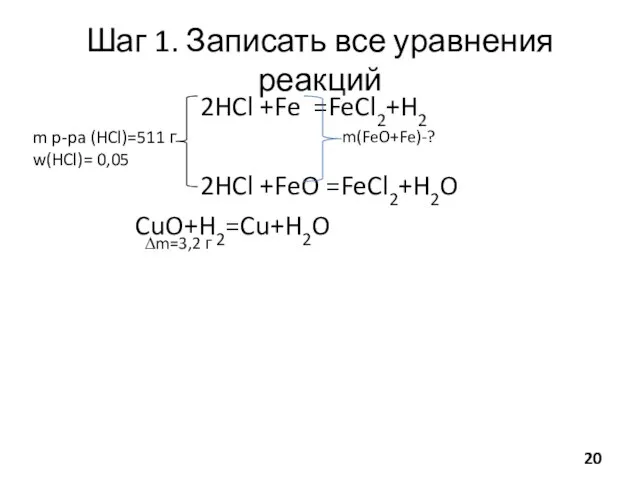
- 20. Шаг 1. Записать все уравнения реакций 2HCl +Fe =FeCl2+H2 2HCl +FeO =FeCl2+H2O CuO+H2=Cu+H2O m p-pa (HCl)=511
- 21. Шаг 2. Считать кол-ва веществ nобщ (HCl)=mобщ (HCI)/M(HCl) mобщ (HCl)= mобщ р-ра (HCI)*w(HCl)= =511г*0,05=25,55 г nобщ
- 22. CuO+H2=Cu+H2O Закон сохранения массы: m(CuO)+m(H2)=m(Cu)+m(H2O) H2 и H2O - ГАЗЫ, CuO и Cu - тв., то
- 23. Шаг 3. Внимательно посмотреть и подумать n(CuO)=n(H2)= 0,2 моль Водород был из реакции: 2HCl +Fe=FeCl2+H2 По
- 24. 2HCl +FeO=FeCl2+H2O По уравнению реакции: n(FeO)= n c FeО (HCl)/2= 0,15 моль m(FeO)= 0,15 моль*72 (г/моль)=10,8
- 25. #долюшка Задание 5. Электролиз 320 г 17%-го раствора хлорида цинка прекратили, когда на аноде выделилось 4,48
- 26. Напишем реакции: Цинк- металл средней активности, поэтому будет восстанавливаться металл и вода на катоде: К(-): 2Н2О
- 27. Немного подумаем… n(Cl₂)=V(Cl₂)/Vm=4,48 л/22,4 (л/моль)=0,2 моль По уравнению реакции: nпрор. (ZnCl2)= n(Cl₂)= 0,2 моль По условию:
- 28. mр-ра (после эл-за)=m р-ра(ZnСl2)-m(Н2)-m(Cl2)-m(Zn(ОН)2)-m(Zn) По уравнению реакции: n (Zn)= n(Zn(ОН)2)= n(Н2)= n(Cl₂)/2= 0,1 моль m(Zn)=65 (г/моль)
- 30. Скачать презентацию

























 Поверхностные явления и дисперсные системы (коллоидная химия)
Поверхностные явления и дисперсные системы (коллоидная химия) Нефть, классификация, применение, основные показатели ,особенности кодировки
Нефть, классификация, применение, основные показатели ,особенности кодировки Композиты на основе полибензоксазинов
Композиты на основе полибензоксазинов Презентация по Химии "Полімери" - скачать смотреть бесплатно
Презентация по Химии "Полімери" - скачать смотреть бесплатно Основні класи неорганічних речовин
Основні класи неорганічних речовин Химические формулы. Классы неорганических веществ. Урок №1
Химические формулы. Классы неорганических веществ. Урок №1 Методология, принципы и методы изучения МПИ
Методология, принципы и методы изучения МПИ Минералы и Близнецы
Минералы и Близнецы 8 класс
8 класс  Эмульсии и эмульгаторы
Эмульсии и эмульгаторы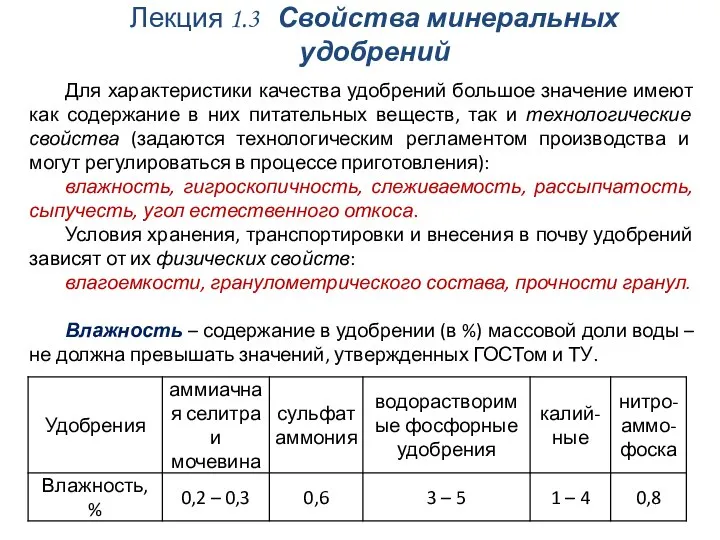 Свойства минеральных удобрений
Свойства минеральных удобрений Электрическая проводимость растворов
Электрическая проводимость растворов Презентация по Химии "Показатели воды: её жесткость и кислотность" - скачать смотреть
Презентация по Химии "Показатели воды: её жесткость и кислотность" - скачать смотреть  Вольфра́м — химический элемент с атомным номером 74 в Периодической системе химических элементов Д. И. Менделеева
Вольфра́м — химический элемент с атомным номером 74 в Периодической системе химических элементов Д. И. Менделеева Силикатная промышленность
Силикатная промышленность Кислотные дожди
Кислотные дожди Общая и неорганическая химия
Общая и неорганическая химия Білки. Функції білків в організмі
Білки. Функції білків в організмі Органические вещества
Органические вещества Безопасная пластмасса
Безопасная пластмасса Этиленовые, олефины, непредельные алкены
Этиленовые, олефины, непредельные алкены Методы диффузионной металлизации
Методы диффузионной металлизации Гипоксия
Гипоксия Презентация по Химии "Етери та естери" - скачать смотреть бесплатно
Презентация по Химии "Етери та естери" - скачать смотреть бесплатно Презентация по Химии "Миючі засоби в побуті. Мило. Првальні порошки" - скачать смотреть бесплатно
Презентация по Химии "Миючі засоби в побуті. Мило. Првальні порошки" - скачать смотреть бесплатно Химия в нашей жизни
Химия в нашей жизни Поверхностные явления. Лекция 15
Поверхностные явления. Лекция 15 Хімічні речовини у побуті підготували Стебко Марія, Бондар Аліна 11-Ф
Хімічні речовини у побуті підготували Стебко Марія, Бондар Аліна 11-Ф