Содержание
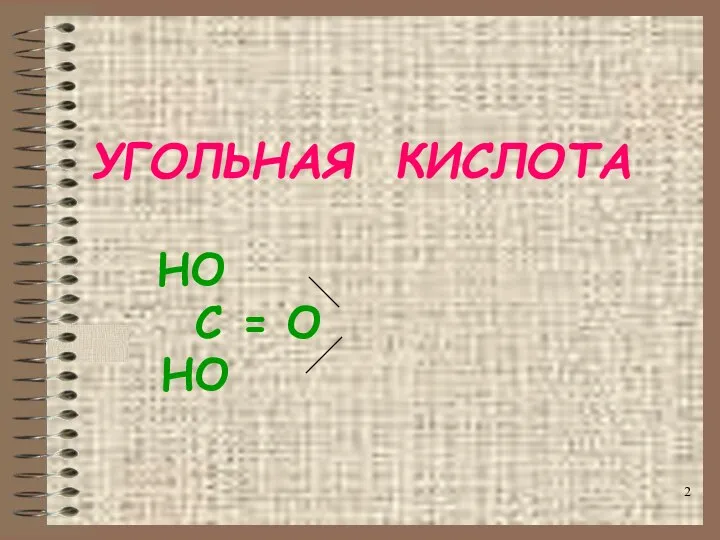
- 2. УГОЛЬНАЯ КИСЛОТА НО C = O НО
- 3. Гидроксимуравьиная (угольная) кислота и её производные
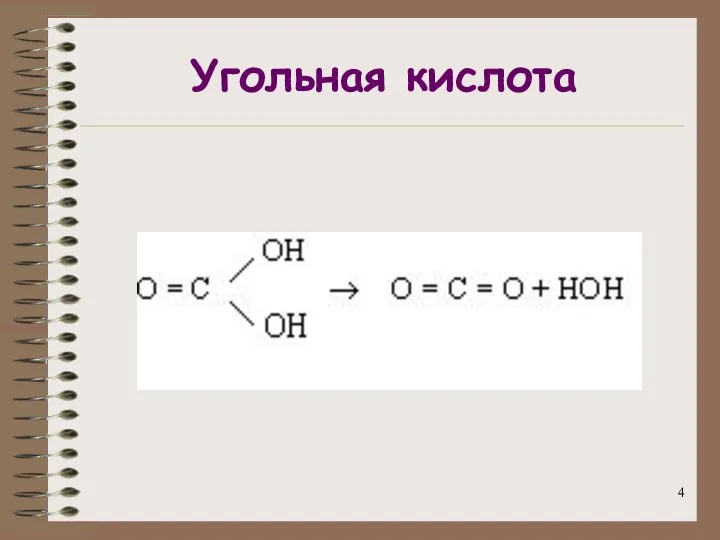
- 4. Угольная кислота
- 5. УГОЛЬНОЙ КИСЛОТЕ СООТВЕТСТВУЮТ: МОНОФУНКЦИОНАЛЬНЫЕ СОЕДИНЕНИЯ (неустойчивые и легко разлагаются, например HCO2Cl ) ДИФУНКЦИОНАЛЬНЫЕ СОЕДИНЕНИЯ (устойчивые и
- 6. Многие производные угольной кислоты имеют важное практическое значение Фосген (карбонилхлорид) COCl2 – полный хлорангидрид угольной кислоты,
- 7. Карбаминовая кислота H2N - COOH – неполный амид угольной кислоты. ОН О = С NН2 В
- 8. Эфиры карбаминовой кислоты получают при взаимодействии её хлорангидрида со спиртами Эфиры карбаминовой кислоты называются уретанами, их
- 9. Карбамид (мочевина)
- 10. КАРБАМИД (МОЧЕВИНА) Представляет собой полный амид угольной кислоты: Н2N C = O Н2N белое кристаллическое вещество,
- 11. Мочевина (карбамид) (NH2)2C=O – полный амид угольной кислоты, впервые получен Ф. Вёлером (1828 г.) при выпаривании
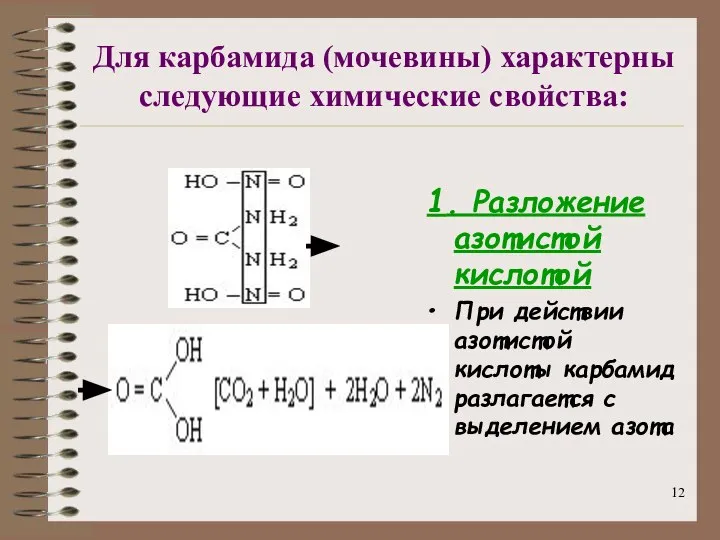
- 12. Для карбамида (мочевины) характерны следующие химические свойства: 1. Разложение азотистой кислотой При действии азотистой кислоты карбамид
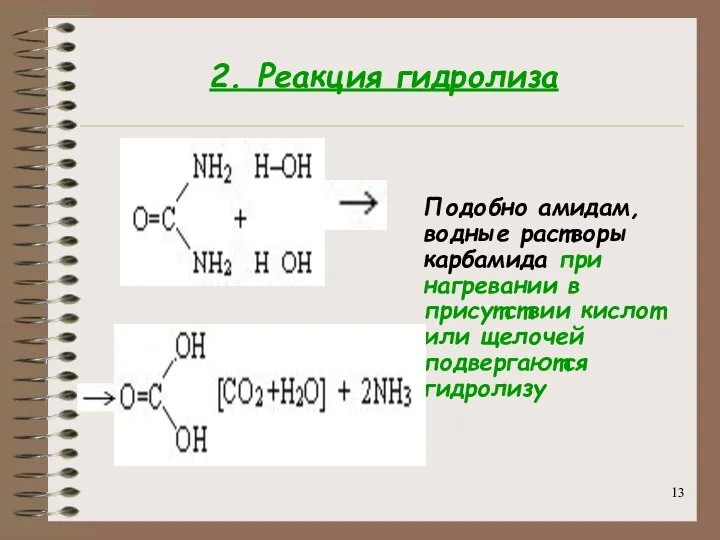
- 13. 2. Реакция гидролиза Подобно амидам, водные растворы карбамида при нагревании в присутствии кислот или щелочей подвергаются
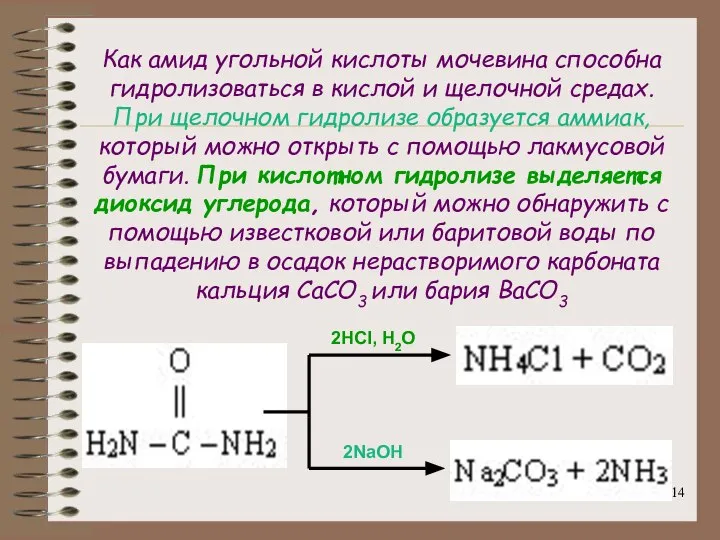
- 14. Как амид угольной кислоты мочевина способна гидролизоваться в кислой и щелочной средах. При щелочном гидролизе образуется
- 15. 3. Разложение при нагревании При нагревании выше температуры плавления карбамид плавится, а затем разлагается с выделением
- 16. 4. Образование солей. При взаимодействии с кислотами карбамид образует соли (с одним молем кислоты)
- 17. 5. Алкилирование карбамида. При алкилировании образуются алкильные производные карбамида N-метилкарбамид
- 18. 6. Ацилирование карбамида При взаимодействии карбамида с галогеногидридами и двухосновными кислотами образуются уреиды – ацильные производные
- 19. 7. Циклизация карбамида При нагревании (350-5000C) и давлении (10-40 МПа) шесьт молекул карбамида образуют циклическое соединение
- 20. * Вычислите массовую долю (%) азота в карбамиде (мочевине). *Почему карбамид может служить ценным азотистым удобрением!
- 21. Решение задачи: 1. Рассчитаем молярную массу карбамида – (NH2)2 CO: М = 2 (14 + 2)
- 22. Задание для самостоятельной проработки темы В каждом тестовом задании выберите только один правильный ответ. Время работы
- 23. «Ключик» для химического хамелеона Правильный ответ Д И М А Й Ы Н Л О П
- 24. «Ключик» для химического хамелеона Д И М А Й Ы Н Л О П Правильный ответ
- 26. Скачать презентацию


















 Химия в содружестве с другими науками
Химия в содружестве с другими науками Применение наноматериалов
Применение наноматериалов Химия - моя жизнь
Химия - моя жизнь Этиленгликоль. Физические свойства
Этиленгликоль. Физические свойства Қышқыл жаңбыр
Қышқыл жаңбыр Получение и свойства кислорода
Получение и свойства кислорода Презентация по Химии "Применение алюминия и его сплава" - скачать смотреть
Презентация по Химии "Применение алюминия и его сплава" - скачать смотреть  Полиэфирные волокна. Полиэстер
Полиэфирные волокна. Полиэстер Способы получения оксидов, оснований, кислот и солей. Урок №2
Способы получения оксидов, оснований, кислот и солей. Урок №2 Спирттер және фенолдар
Спирттер және фенолдар Thermal Energy, Chemical Energy
Thermal Energy, Chemical Energy Пластификаторы и пластификация полимеров
Пластификаторы и пластификация полимеров Химическая термодинамика
Химическая термодинамика EdExcel Unit C2 – Discovering Chemistry
EdExcel Unit C2 – Discovering Chemistry Никель қаптамаларын алу жолдары
Никель қаптамаларын алу жолдары Явище ізомерії. Структурна ізомерія. Близнюки органічного світу
Явище ізомерії. Структурна ізомерія. Близнюки органічного світу Влияние параметров технологического режима на удельную производительность и устойчивую работу реакторов
Влияние параметров технологического режима на удельную производительность и устойчивую работу реакторов Облучение. Радиационная окраска
Облучение. Радиационная окраска Тема Основание Гидроксид железа (II)
Тема Основание Гидроксид железа (II) Презентация Правила безопасности в кабинете химии
Презентация Правила безопасности в кабинете химии ДИТИНСТВО ТА ЖИТТЯ Д.І. МЕНДЕЛЄЄВА Підготував Учень 8-Б класу Воротинцев Артем
ДИТИНСТВО ТА ЖИТТЯ Д.І. МЕНДЕЛЄЄВА Підготував Учень 8-Б класу Воротинцев Артем  Химия s-элементов. Особенности свойств Mg и Be. Химия p-элементов. Общая характеристика элементов VIIA группы (галогены). Фтор
Химия s-элементов. Особенности свойств Mg и Be. Химия p-элементов. Общая характеристика элементов VIIA группы (галогены). Фтор Теория Бутлерова
Теория Бутлерова Количество вещества. Решение задач
Количество вещества. Решение задач Информационно-поисковый исследовательский проект: «Влияние пищевых добавок на здоровье человека».
Информационно-поисковый исследовательский проект: «Влияние пищевых добавок на здоровье человека».  Электронные конфигурации атомов
Электронные конфигурации атомов Альдегидтер және кетондар
Альдегидтер және кетондар Потенциометрия. Методы потенциометрии, и их применение в медицине. Плюсы и минусы методов ПТ
Потенциометрия. Методы потенциометрии, и их применение в медицине. Плюсы и минусы методов ПТ