Содержание
- 2. План лекции: I. Доструктурные теории: - витализм; - теория радикалов; - теория типов. II. Краткая справка
- 3. Йёнс Якоб Берцелиус
- 4. Фридрих Вёлер
- 5. Пьер Эжен Марселен Бертло
- 6. Жан Батист Дюма
- 7. Основные положения теории радикалов - в состав органических веществ входят радикалы, несущие на себе положительный заряд;
- 8. Значение теории радикалов - понятие «радикал» прочно вошло в химию; - верным оказалось утверждение о возможности
- 9. Шарль Фредерик Жерар Фридрих Август Кекуле
- 10. Сущность теории типов. в основу теории положена аналогия в реакциях между органическими и некоторыми неорганическими веществами,
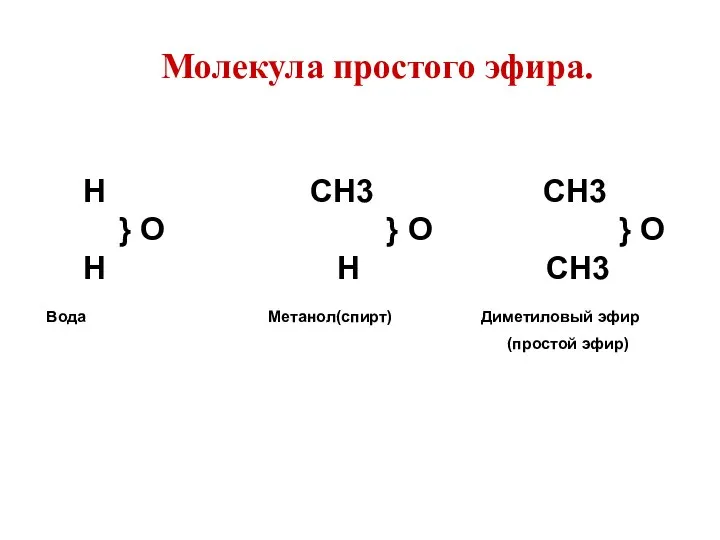
- 11. Молекула простого эфира. Н CH3 CH3 } O } O } O Н H CH3 Вода
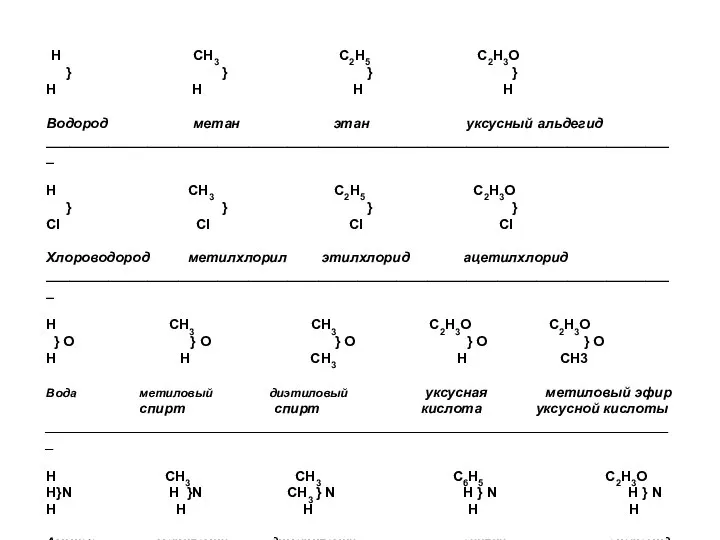
- 12. H CH3 C2H5 C2H3O } } } } H H H H Водород метан этан уксусный
- 13. - молекулы органических веществ представляют собой систему, состоящую из атомов, порядок соединения которых неизвестен; - невозможно
- 14. Роль теории типов в развитии органической химии - позволила предсказать и открыть ряд веществ; - оказала
- 15. Теория химического строения Теория химического строения
- 16. Александр Михайлович Бутлеров
- 17. Необходимость появления теории - возросли требования промышленности к органической химии. Невозможно было определить валентность углерода элементов
- 18. Основные предпосылки подготовившие почву для возникновения теории химического строения 1853г-Франкланд «Учение о валентности» - В 1858г.
- 19. Основные положения теории химического строения А.М. Бутлерова (1861г.)
- 20. Теория химического строения - дала возможность систематизировать органические вещества; - ответила на все вопросы, возникшие к
- 21. ТХС органических соединений А.М. Бутлерова внесла существенный вклад в создание общенаучной картины мира, способствовала диалектико –
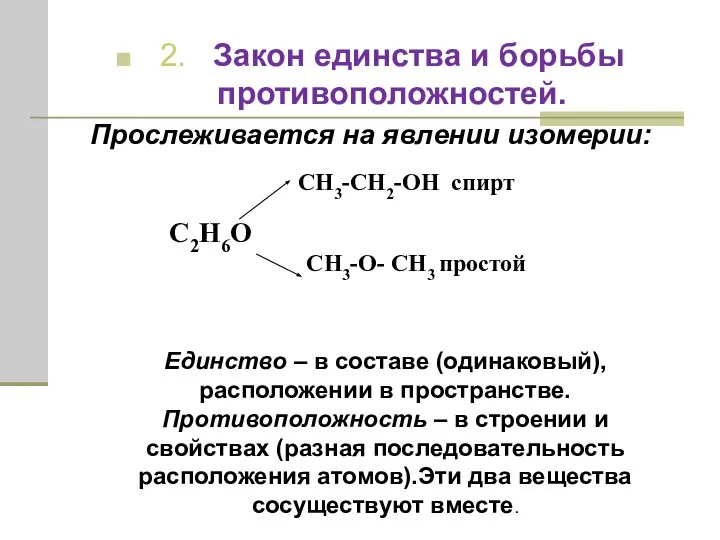
- 22. 2. Закон единства и борьбы противоположностей. Прослеживается на явлении изомерии: . CH3-CH2-OH спирт C2H6O CH3-O- CH3
- 23. Закон отрицания отрицания. Изомеры сосуществуя отрицают друг друга своим существованием.
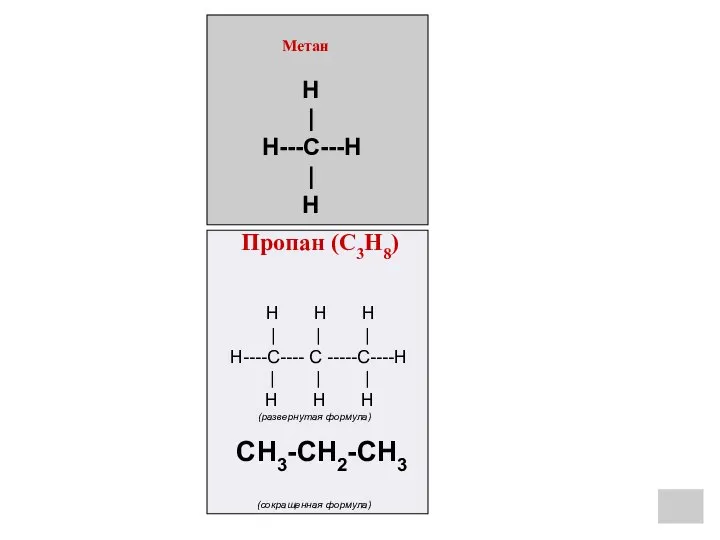
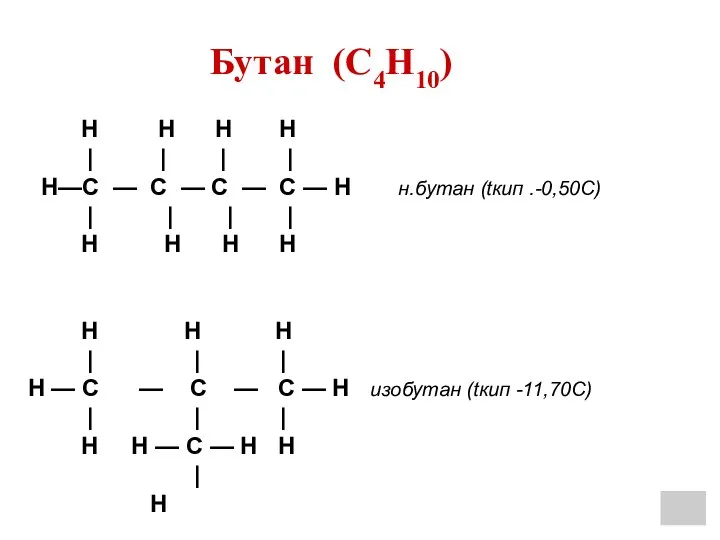
- 24. H H H | | | H----C---- C -----C----H | | | H H H (развернутая
- 25. Н Н Н Н | | | | Н—С — С — С — С —
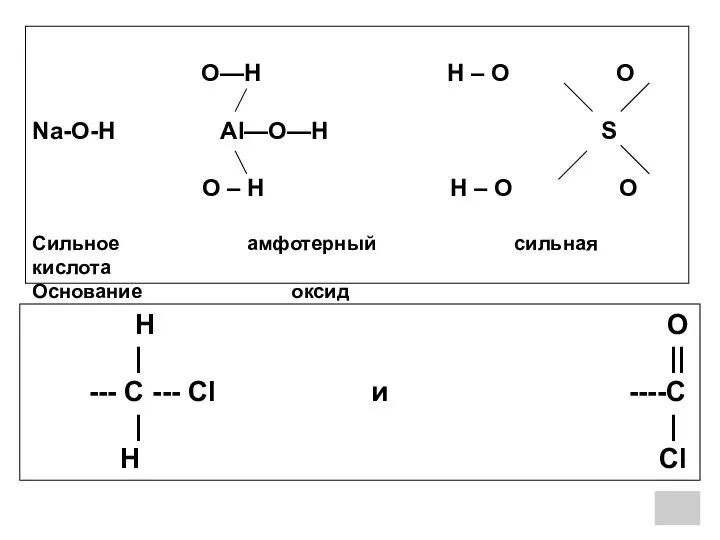
- 26. H O | || --- C --- Cl и ----C | | H Cl
- 28. Скачать презентацию



















 Физические и химические свойства меди
Физические и химические свойства меди Решаем задачи «Домашняя аптечка» Карпухина Ирина Степановна Учитель химии МБОУ СОШ № 32 Город Новосибирск
Решаем задачи «Домашняя аптечка» Карпухина Ирина Степановна Учитель химии МБОУ СОШ № 32 Город Новосибирск Природный и синтетический каучуки. Резина
Природный и синтетический каучуки. Резина Энергетика химических процессов. Основы термохимии
Энергетика химических процессов. Основы термохимии Аттестационная работа. Организация деятельности по изучению природных и искусственных красителей для пасхальных яиц
Аттестационная работа. Организация деятельности по изучению природных и искусственных красителей для пасхальных яиц Альдегиды
Альдегиды Неорганическая химия Сероводород
Неорганическая химия Сероводород Химико – математические проценты
Химико – математические проценты Оценка химической обстановки при авариях на химически опасных объектах
Оценка химической обстановки при авариях на химически опасных объектах Знаки химических элементов. Дополнение
Знаки химических элементов. Дополнение Диффузия золота и свинца
Диффузия золота и свинца Минеральные кислоты
Минеральные кислоты Хімічний склад і використання мінералів
Хімічний склад і використання мінералів Строение атома
Строение атома Геохимия природных процессов
Геохимия природных процессов Пәннiң мiндетi мен мақсаты. Термодинамика. Термохимия
Пәннiң мiндетi мен мақсаты. Термодинамика. Термохимия Биологическая коррозия и защита строительных материалов и конструкций от биоповреждений
Биологическая коррозия и защита строительных материалов и конструкций от биоповреждений Презентация по Химии "Хлор" - скачать смотреть
Презентация по Химии "Хлор" - скачать смотреть  Алканы. Практическое занятие 1
Алканы. Практическое занятие 1 Бытовая химия в нашей жизни
Бытовая химия в нашей жизни Драгоценные камни
Драгоценные камни Кислоты. Соли (8 класс)
Кислоты. Соли (8 класс) Уравнение состояния идеального газа
Уравнение состояния идеального газа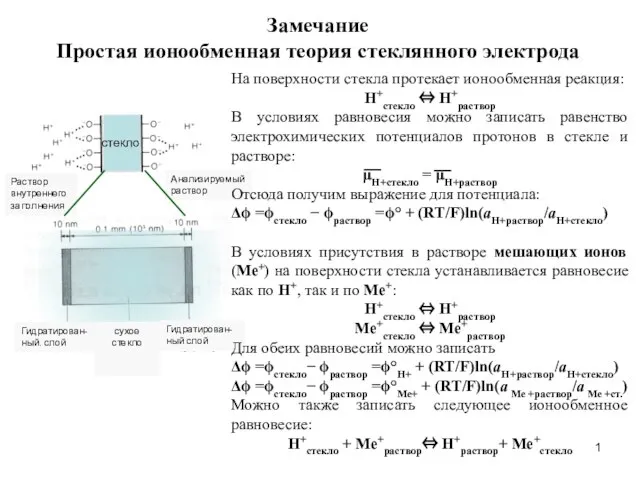 Простая ионообменная теория стеклянного электрода
Простая ионообменная теория стеклянного электрода Центрифугирование в почвоведении
Центрифугирование в почвоведении Расчеты равновесий в водных растворах рН, рОН
Расчеты равновесий в водных растворах рН, рОН Бейорганикалық қосылыстардың негізгі кластары
Бейорганикалық қосылыстардың негізгі кластары S,p,d,f-элементтері және олардың биологиялық маңызы
S,p,d,f-элементтері және олардың биологиялық маңызы