Содержание
- 2. Железо и его соединения Урок-проект в 9 классе подготовила Яскевич В.А. учитель химии МОУ «Кадетская школа
- 3. План изучения вещества Железо как химический элемент. Нахождение в природе. Получение. Физические свойства железа. Химические свойства
- 4. Визитная карточка железа Порядковый номер Период Группа Подгруппа Ar 26 4 VIII Побочная 56
- 5. Строение атома железа 2е; 8е; 14е; 2е. 1s2 2s2 2р6 3s2 3р6 3d6 4s2 26 p;
- 6. Степени окисления Для железа характерны две основные степени окисления: +2, +3. Fe0 –2e = Fe+2 Fe0
- 7. Распространенность в природе 4-е место среди элементов после O, Si, Al. 2-е место по количеству в
- 8. Железо – простое вещество Физические свойства железа Цвет Блеск Пластичность Магнитные свойства Температура плавления Твердость Серебристо-белый
- 9. Нахождение в природе Fe3O4 – магнитный железняк (72%) Fe2O3 – красный железняк (гематит) (65%) 2Fe2O3 *
- 10. Способы получения Домны. Кислородный конвертер. Генри Бессемер Электродуговые печи. Пьер Мартен
- 11. Биологическая роль железа В организме человека содержится около 5 г железа. Из них 57% приходится на
- 12. Биологическая роль железа Суточная норма потребности человека составляет около 15 мг железа. Много железа в сливовом
- 13. Химические свойства 1. Железо реагирует с неметаллами: 2 Fe+3Cl2 = 2FeCl3 Fe+S = FeS 3 Fe+
- 14. Генетические ряды железа Fe ? FeCl2 ? Fe(OH)2 ? FeO Fe ? FeCl3 ? Fe(OH)3 ?
- 15. Сплавы железа Сталь Чугун
- 16. Применение железа и его соединений Железный купорос, хлорное железо, оксиды железа используют для приготовления лекарств, катализаторов,
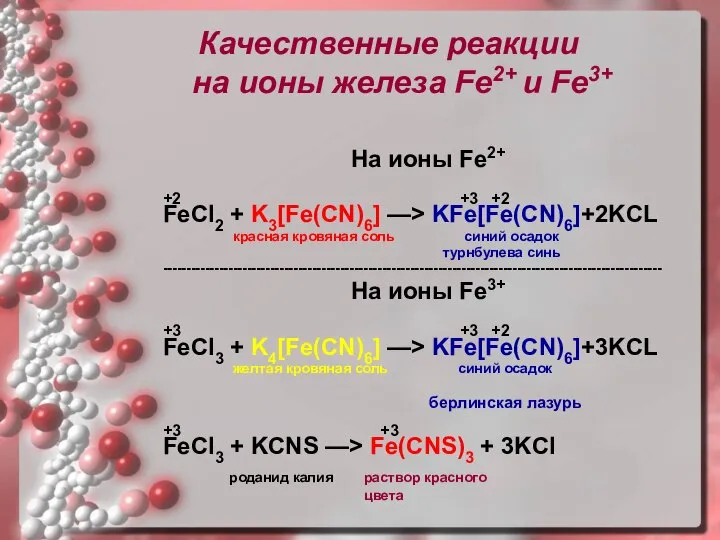
- 17. Качественные реакции на ионы железа Fe2+ и Fe3+ На ионы Fe2+ +2 +3 +2 FeCl2 +
- 18. Качественные реакции на ионы железа Fe2+ и Fe3+ Качественная реакция на ионы железа Fe2+: реактив –
- 19. «Определение содержания Fe3+ в воде, взятой из различных источников» Материалы: проб воды, взятые в разных местах,
- 20. Вывод Железо – жизненно необходимый элемент для всех живых организмов Железо – металл без которого невозможен
- 21. Железо не только основа всего мира, самый главный металл окружающей нас природы, оно – основа культуры
- 23. Скачать презентацию



















 Перечень практических навыков по общей химии для экзамена
Перечень практических навыков по общей химии для экзамена Химия вокруг нас
Химия вокруг нас Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Химическая реакция – превращение одних веществ в другие
Химическая реакция – превращение одних веществ в другие Минералдарды зерттеу әдістері
Минералдарды зерттеу әдістері Биохимия
Биохимия Эколого-геохимическая оценка состояния компонентов природной среды особо охраняемых территорий. Парк Смоленское Поозерье
Эколого-геохимическая оценка состояния компонентов природной среды особо охраняемых территорий. Парк Смоленское Поозерье Типы химических реакций
Типы химических реакций Петрология. Классификации магматических горных пород
Петрология. Классификации магматических горных пород Химия және денсаулық
Химия және денсаулық Атомная энергетика
Атомная энергетика Титан как элемент
Титан как элемент Алюминий. Сплавы алюминия. Учитель: Белозерова Татьяна Анатольевна Учени
Алюминий. Сплавы алюминия. Учитель: Белозерова Татьяна Анатольевна Учени Углеводороды и их природные источники. Гомологический ряд алканов. Строение алканов
Углеводороды и их природные источники. Гомологический ряд алканов. Строение алканов Каталитическая активность ферментов Работу выполнили: Кичаева Нина Иванькова Елена Ученицы 10 класса МОУ Сергиевской СОШ №1 «О
Каталитическая активность ферментов Работу выполнили: Кичаева Нина Иванькова Елена Ученицы 10 класса МОУ Сергиевской СОШ №1 «О Метаболизм - обмен веществ
Метаболизм - обмен веществ Химия актиноидов
Химия актиноидов Чистые вещества и смеси. Способы разделения смесей
Чистые вещества и смеси. Способы разделения смесей КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ
КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ  Лекция №6. Применение закона действующих масс к окислительно-восстановительным равновесиям
Лекция №6. Применение закона действующих масс к окислительно-восстановительным равновесиям Химиялық термодинамиканың негіздері. Негізгі түсініктері мен аңдары. Термохимиялық есептеулер
Химиялық термодинамиканың негіздері. Негізгі түсініктері мен аңдары. Термохимиялық есептеулер Кетоновые тела
Кетоновые тела Нанохимия, как наука
Нанохимия, как наука Autoionization of water Hydrolysis of salts
Autoionization of water Hydrolysis of salts Строение гетероциклических соединений
Строение гетероциклических соединений Применение s-, p-, d- элементов в медицине
Применение s-, p-, d- элементов в медицине Чипсы, вред или польза
Чипсы, вред или польза Бродильні мікроорганізми і бродіння. Лекція 5
Бродильні мікроорганізми і бродіння. Лекція 5