Содержание
- 2. Цель урока: Разобраться, что такое «степень окисления» Научиться находить степень окисления по формуле
- 3. Поваренная соль NaCl «Хлеб да соль» - пожелание добра «Надо вместе съесть пуд соли, чтобы узнать
- 4. Влияние Na на организм человека Хранят простое вещество «натрий» как Кощееву смерть. Как может повлиять натрий
- 5. Влияние Cl2 на организм человека Хлор – отравляющее вещество, применявшееся во время первой мировой войны
- 6. Образование сложного вещества Na0 +11 2е,8е,1е Cl0 +17 2e,8e,7e Какой вид связи может образоваться между этими
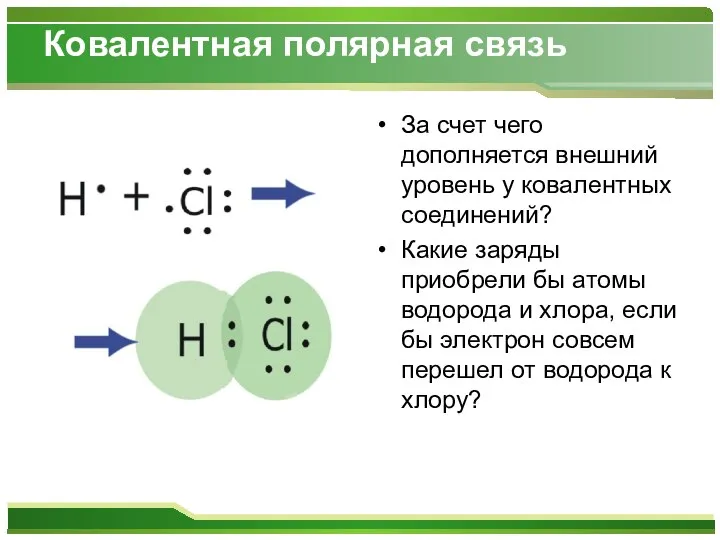
- 7. Ковалентная полярная связь За счет чего дополняется внешний уровень у ковалентных соединений? Какие заряды приобрели бы
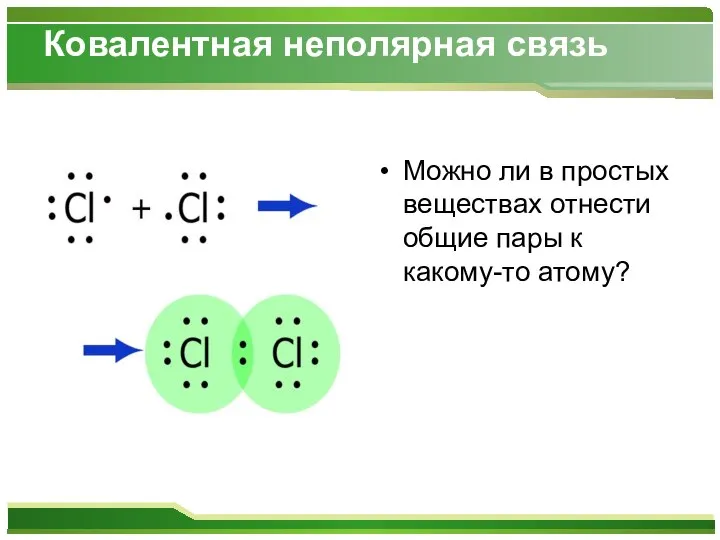
- 8. Ковалентная неполярная связь Можно ли в простых веществах отнести общие пары к какому-то атому?
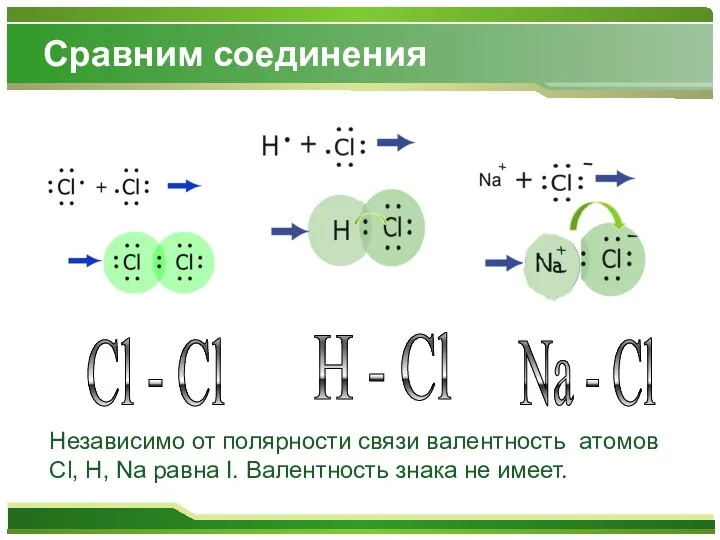
- 9. Сравним соединения H - Cl Cl - Cl Na - Cl Независимо от полярности связи валентность
- 10. Степень окисления – это условный заряд атомов химических элементов в соединении, вычисленный на основе предположения, что
- 11. Правила определения с.о. С.о. атомов в простых веществах = 0 С.о. фтора = -1 С.о. кислорода
- 12. Возможные с.о. Положительная «+» равна числу отданных электронов. Максимальная с.о. равна номеру группы Отрицательная «-» равна
- 13. Промежуточные с.о. Рассмотрим возможные с.о. серы – S Максимальная +6 SO3 Минимальная -2 H2S Сера может
- 14. Определение с.о. N2O3 На первом месте стоит элемент с «+» с.о., на втором с «-» У
- 15. Задание 1 Определите С.О. по формулам Cl2O7, NaH, Na2S, MgO, H3N, N2, Al2S3, Cu2O
- 17. Скачать презентацию











 Мир зеркал
Мир зеркал Углеводороды. Алканы
Углеводороды. Алканы Кристаллография и основы кристаллохимии. Лекция 5
Кристаллография и основы кристаллохимии. Лекция 5 Электролитическая диссоциация
Электролитическая диссоциация Сера
Сера Химия липидов
Химия липидов Вуглеводні. Насичені, ненасичені та ароматичні вуглеводні: їх склад, будова, фізичні та хімічні властивості.
Вуглеводні. Насичені, ненасичені та ароматичні вуглеводні: їх склад, будова, фізичні та хімічні властивості.  Твердое тело и его характеристики. Закон Гука. Плавление и кристаллизация. Лекция №26
Твердое тело и его характеристики. Закон Гука. Плавление и кристаллизация. Лекция №26 Алмази
Алмази  Презентация Алкены
Презентация Алкены Проведення електрофоретичного розділення ДНК в агарозному гелі
Проведення електрофоретичного розділення ДНК в агарозному гелі Фосфор и его основные соединения
Фосфор и его основные соединения Корозія металів Виконала учениця 10-А класу Новоград-Волинської ЗОШ №7 Бучинська Дарія
Корозія металів Виконала учениця 10-А класу Новоград-Волинської ЗОШ №7 Бучинська Дарія  Гидрирование альдегидов и кетонов
Гидрирование альдегидов и кетонов Исследование процесса диффузии на примере движения частиц в жидкостях и газах
Исследование процесса диффузии на примере движения частиц в жидкостях и газах Общая характеристика и источники сырья производств основного органического и нефтехимического синтеза. Лекция № 5-6
Общая характеристика и источники сырья производств основного органического и нефтехимического синтеза. Лекция № 5-6 Спирты: получение, свойства и применение
Спирты: получение, свойства и применение Периодический закон и периодическая система Д.И. Менделеева (Лекция 2)
Периодический закон и периодическая система Д.И. Менделеева (Лекция 2) Волокно капрон
Волокно капрон Презентация по Химии "Каучук" - скачать смотреть
Презентация по Химии "Каучук" - скачать смотреть  Предмет органической химии.
Предмет органической химии. Презентация по Химии "щелочные метал" - скачать смотреть бесплатно
Презентация по Химии "щелочные метал" - скачать смотреть бесплатно Фосфор
Фосфор Фазовое равновесие в насыщенном растворе малорастворимого электролита
Фазовое равновесие в насыщенном растворе малорастворимого электролита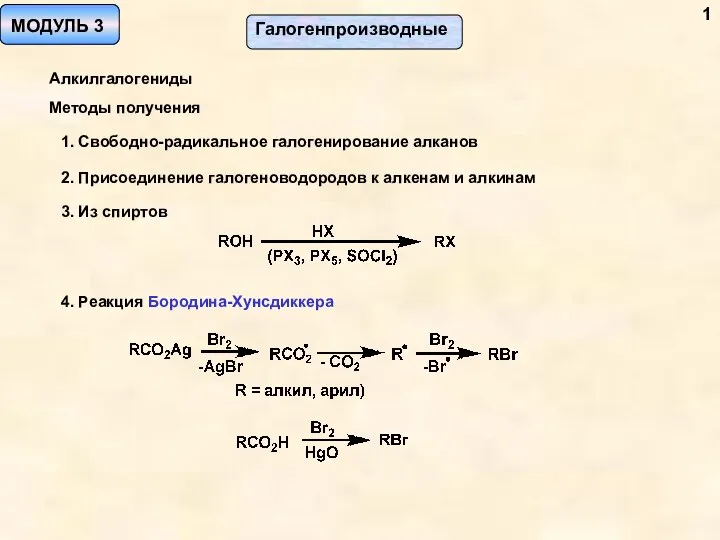 Галогенпроизводные. Алкилгалогениды. Методы получения. (Модуль 3)
Галогенпроизводные. Алкилгалогениды. Методы получения. (Модуль 3) Экспертные системы распознавания химических веществ
Экспертные системы распознавания химических веществ Теплота сгорания топлива
Теплота сгорания топлива Количество вещества
Количество вещества