Содержание
- 2. Углеводороды органические соединения, в состав которых входят только два элемента: углерод и водород. CH4, C2H6, C3H6,
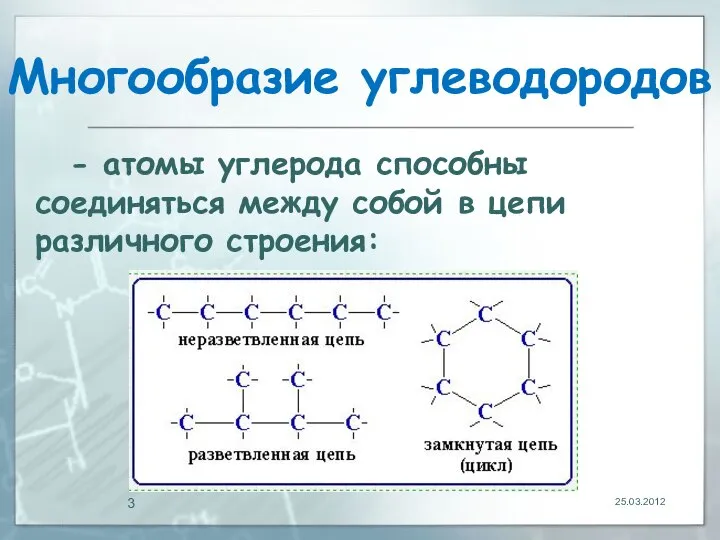
- 3. Многообразие углеводородов 25.03.2012 - атомы углерода способны соединяться между собой в цепи различного строения:
- 4. Многообразие углеводородов 25.03.2012 - даже при одинаковом количестве атомов углерода в молекулах углеводороды могут отличаться числом
- 5. Многообразие углеводородов 25.03.2012 - одному и тому же элементному составу молекул (одной молекулярной формуле) может соответствовать
- 6. Многообразие углеводородов 25.03.2012 Классификацию углеводородов проводят по следующим структурным признакам, определяющим свойства этих соединений: - строение
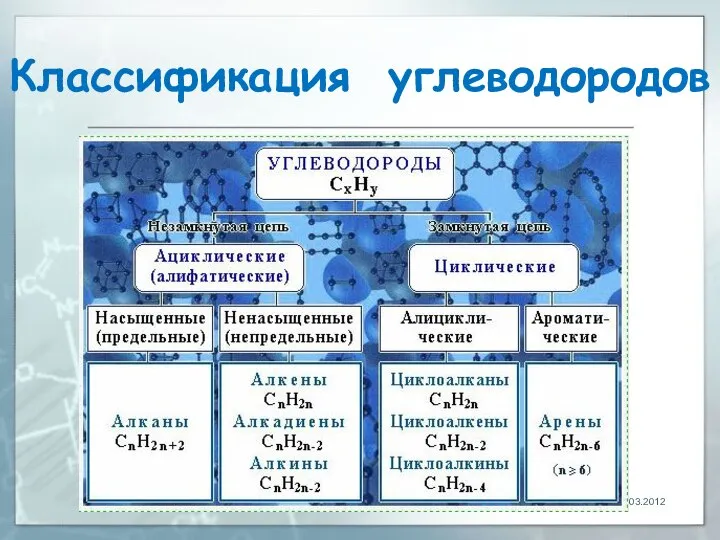
- 7. Классификация углеводородов 25.03.2012 1. В зависимости от строения углеродной цепи углеводороды подразделяют на две группы: -
- 8. Классификация углеводородов 25.03.2012
- 9. Классификация углеводородов 25.03.2012 Среди циклических углеводородов выделяют: - алициклические (т.е. алифатические циклические); - ароматические (арены). В
- 10. Классификация углеводородов 2. По степени насыщенности различают: насыщенные (предельные) углеводороды (алканы и циклоалканы); ненасыщенные (непредельные), содержащие
- 11. Алканы алифатические (ациклические) предельные углеводороды, в которых атомы углерода связаны между собой простыми (одинарными) связями в
- 12. Алканы Алканы – название предельных углеводородов по международной номенклатуре. Парафины – исторически сложившееся название, отражающее свойства
- 13. Алканы углеводороды, состав которых выражается общей формулой CnH2n+2, где n – число атомов углерода 25.03.2012
- 14. Гомологический ряд алканов Алканы, представляют собой ряд родственных соединений с однотипной структурой, в котором каждый последующий
- 15. Строение алканов в алканах имеются два типа химических связей: С–С и С–Н. Связь С–С является ковалентной
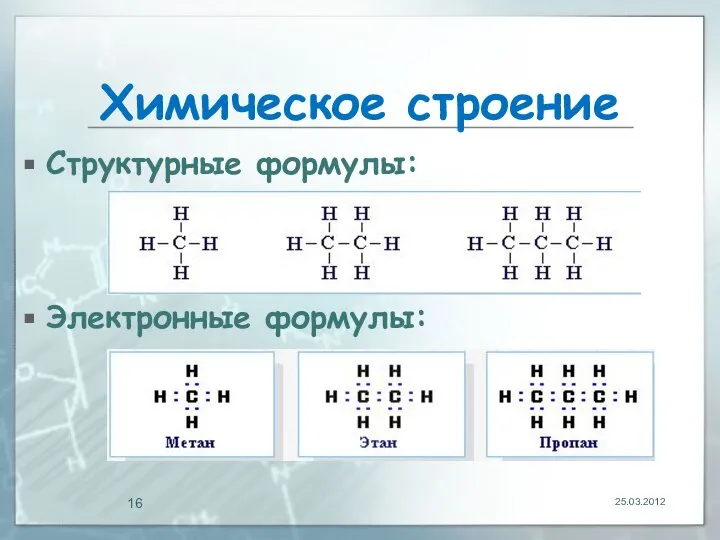
- 16. Химическое строение Структурные формулы: Электронные формулы: 25.03.2012
- 17. Пространственное строение 25.03.2012 sp3-гибридизация каждая из четырех sp3-гибридных АО углерода участвует в осевом (σ-) перекрывании с
- 18. Пространственное строение Четыре σ -связи углерода направлены в пространстве под тетраэдрическим углом 109о28'. Молекула метана СН4
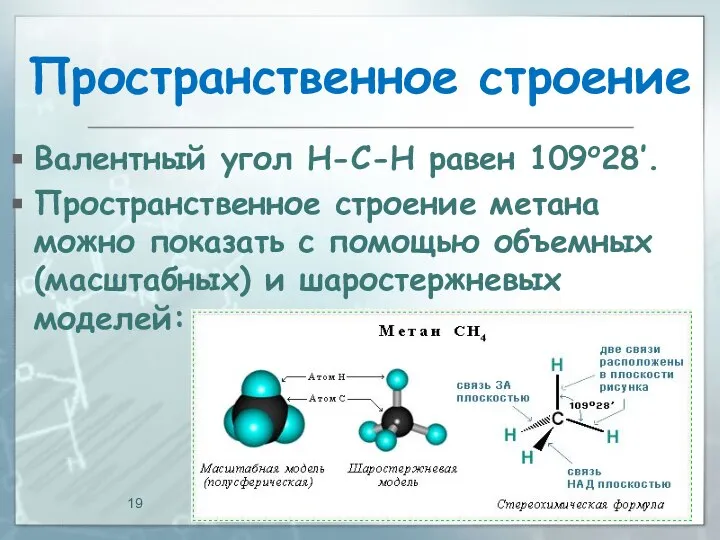
- 19. Пространственное строение Валентный угол Н-С-Н равен 109о28’. Пространственное строение метана можно показать с помощью объемных (масштабных)
- 20. Изомерия алканов явление существования соединений, которые имеют одинаковый состав (одинаковую молекулярную формулу), но разное строение. Такие
- 21. Структурная изомерия способность атомов углерода образовывать цепи различного строения: 25.03.2012 алкан С5Н12 – в виде трех
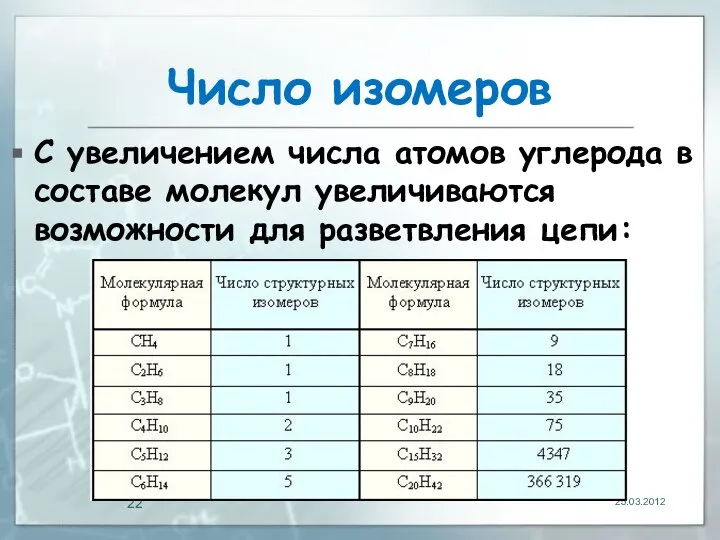
- 22. Число изомеров С увеличением числа атомов углерода в составе молекул увеличиваются возможности для разветвления цепи: 25.03.2012
- 23. Приемы построения структурных формул изомеров 1. Сначала изображаем молекулу линейного изомера (ее углеродный скелет) на примере
- 24. Приемы построения структурных формул изомеров 2. Затем цепь сокращаем на 1 атом углерода и этот атом
- 25. Приемы построения структурных формул изомеров 3. Когда все положения основной цепи исчерпаны, сокращаем цепь еще на
- 26. Приемы построения структурных формул изомеров 4. После построения углеродного скелета изомера необходимо дополнить все углеродные атомы
- 27. Зеркальная (оптическая) изомерия оптическими изомерами называются пространственные изомеры, молекулы которых относятся между собой как предмет и
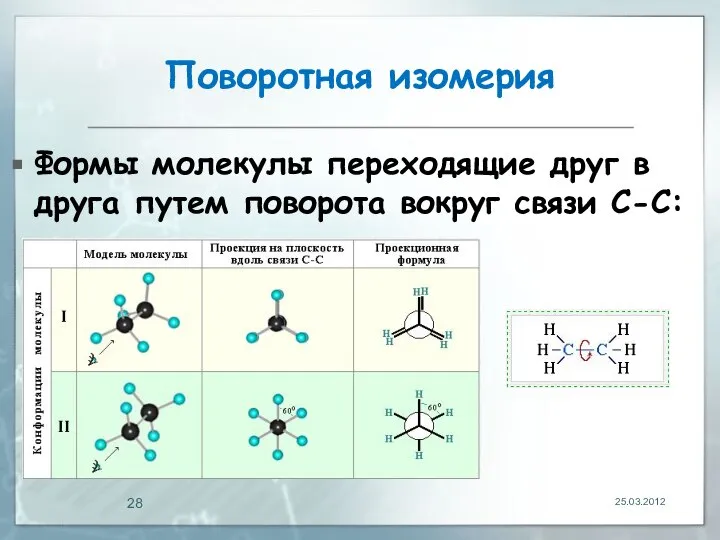
- 28. Поворотная изомерия Формы молекулы переходящие друг в друга путем поворота вокруг связи С-С: 25.03.2012
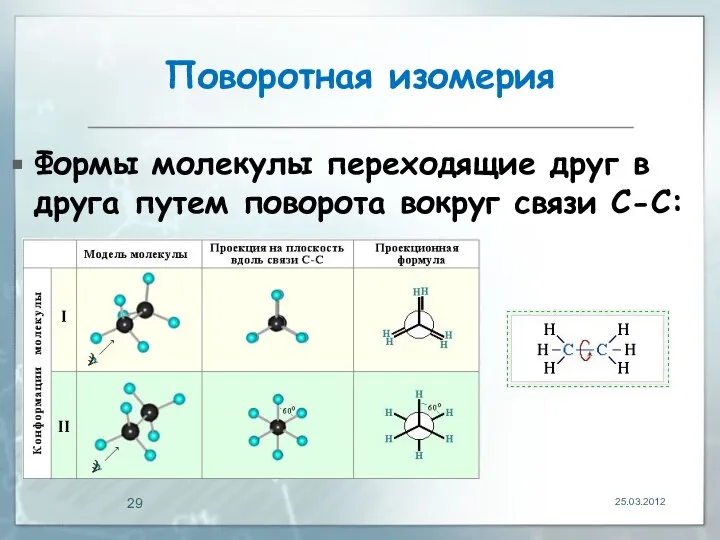
- 29. Поворотная изомерия Формы молекулы переходящие друг в друга путем поворота вокруг связи С-С: 25.03.2012
- 30. Номенклатура Номенклатура органических соединений – система правил, позволяющих дать однозначное название каждому индивидуальному веществу. В настоящее
- 31. Радикалы в ряду алканов Общее название одновалентных радикалов алканов – алкилы – обpазовано заменой суффикса -ан
- 32. Радикалы Радикалы подразделяются на первичные, вторичные и третичные: 25.03.2012
- 33. Правила построения названий 1. Для простейших алканов (С1-С4) приняты тpивиальные названия: метан, этан, пpопан, бутан, изобутан.
- 34. Правила построения названий 3.В основе названия разветвленного алкана лежит название входящего в его конструкцию нормального алкана
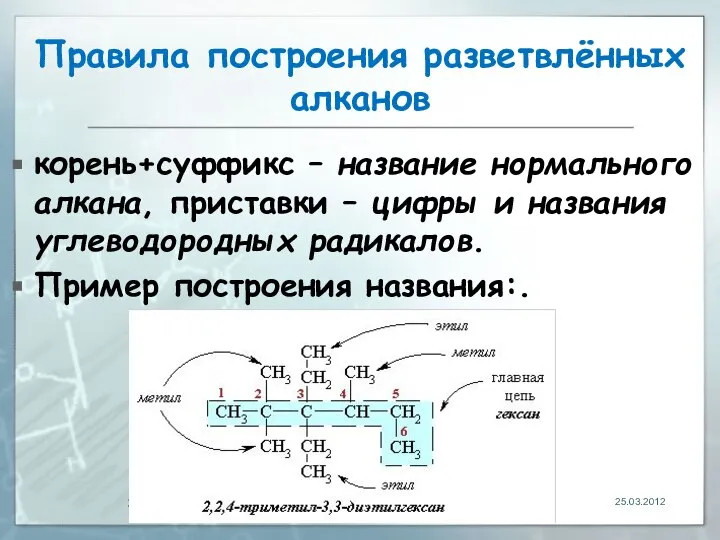
- 35. Правила построения разветвлённых алканов корень+суффикс – название нормального алкана, приставки – цифры и названия углеводородных радикалов.
- 36. 1.Контрольная работа 25.03.2012 1. Состав алканов отражает общая формула . . . а)CnH2n б) CnH2n+2 в)
- 37. 2. Контрольная работа 25.03.2012 Какие соединения относятся к гомологическому ряду метана: а) С2Н4 б) С3Н8 в)
- 38. 3.Контрольная работа 25.03.2012 Какие из представленных соединений являются структурными изомерами ?
- 39. 4. Контрольная работа 25.03.2012 Укажите названия углеводородных радикалов: Ответ 1: а - н-пропил; б - н-бутил;
- 40. 5. Контрольная работа Назовите по систематической номенклатуре "изооктан" (стандарт моторного топлива с октановым числом 100): 25.03.2012
- 42. Скачать презентацию































 Ауылшаруашылық дақылдарының тұқымдарын фунгецидтермен улау және химиялық қорғау тәсілдерінің биологиялық
Ауылшаруашылық дақылдарының тұқымдарын фунгецидтермен улау және химиялық қорғау тәсілдерінің биологиялық Исследование уравнения сжимаемости при высоких плотностях газов на примере аргона
Исследование уравнения сжимаемости при высоких плотностях газов на примере аргона Ցեմենտի արտադրություն
Ցեմենտի արտադրություն Фенолы. Классификация фенолов
Фенолы. Классификация фенолов Производство фенолформальдегидной смолы
Производство фенолформальдегидной смолы Презентація на тему: Твердість води Способи усунення твердості води
Презентація на тему: Твердість води Способи усунення твердості води  Микроорганизмы и важнейшие химические факторы среды обитания
Микроорганизмы и важнейшие химические факторы среды обитания Применение здм к кислотно-основным равновесиям и их роль в аналитической химии
Применение здм к кислотно-основным равновесиям и их роль в аналитической химии Презентация по Химии "Кислотные дожди" - скачать смотреть
Презентация по Химии "Кислотные дожди" - скачать смотреть  Алюминиевые сплавы
Алюминиевые сплавы Неон. Получение
Неон. Получение Биохимия крови. (Лекция 9)
Биохимия крови. (Лекция 9) Приготовление раствора сахара
Приготовление раствора сахара Сплавы
Сплавы Электронная формула атома магния
Электронная формула атома магния Периодический закон, периодическая система. Формулировка периодического закона Д.И. Менделеева
Периодический закон, периодическая система. Формулировка периодического закона Д.И. Менделеева КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ
КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ Мило. Мийні засоби
Мило. Мийні засоби  Домашняя химчистка рекомендует
Домашняя химчистка рекомендует Значення хімічних процесів у природі
Значення хімічних процесів у природі Биоорганическая химия
Биоорганическая химия Презентация по Химии "Основные классы неорганических соединений Соли" - скачать смотреть
Презентация по Химии "Основные классы неорганических соединений Соли" - скачать смотреть  Пластик и его применение в быту
Пластик и его применение в быту Комплексные соединения. Аммиакаты
Комплексные соединения. Аммиакаты Презентация по Химии "Круговорот углерода в природе" - скачать смотреть
Презентация по Химии "Круговорот углерода в природе" - скачать смотреть  Аккумуляторы и их устройство
Аккумуляторы и их устройство В менделеевской гостиной: А.А.Блок и Менделеевы
В менделеевской гостиной: А.А.Блок и Менделеевы Важнейшие классы бинарных соединений – оксиды и водородные соединения
Важнейшие классы бинарных соединений – оксиды и водородные соединения