Применение закона действующих масс к гетерогенным равновесиям. Ионное произведение растворимости. (Лекция 5)
Содержание
- 2. Гетерогенные равновесия в аналитической химии Гомогенная система – это система, состоящая только из одной фазы (жидкой,
- 4. В аналитической химии часто встречаются гетерогенные системы и равновесия двух типов: Осадок (твердая фаза) какого-либо вещества,
- 5. Произведение активностей В аналитической химии большое значение имеют гетерогенные системы "осадок - насыщенный раствор". Совершенно нерастворимых
- 6. [SO42-] и [Ba2+] – равновесные концентрации ионов в насыщенном растворе, их произведение представляет собой ПР концентрационную
- 7. Правило произведения растворимости Правило произведения растворимости (ПР) сформулировал В. Нернст (1889), применив закон действующих масс к
- 8. Правило произведения растворимости
- 9. ВА ⇄ В+ + А‾ Раствор, где [В+]∙[А‾] = ПР, называется насыщенным раствором. Раствор, в котором
- 10. ПР легко вычислить, зная растворимость соединения при данной температуре. Пример 1. Растворимость CaCO3 равна 0,0069 или
- 11. Зная величину ПР, можно в свою очередь вычислить растворимость вещества в моль/дм3 или г/л. Пример 2.
- 12. Если ионное произведение малорастворимого электролита превысит ПР, то произойдет образование осадка и концентрация ионов в растворе
- 13. Пример 4. В какой последовательности будут осаждаться галогениды при действии не смесь галогенидов нитрата серебра? При
- 14. Можно сравнивать значения ПР только однотипных электролитов. Если электролиты не однотипны, то для определения порядка осаждения
- 16. Скачать презентацию




![[SO42-] и [Ba2+] – равновесные концентрации ионов в насыщенном растворе, их](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1406785/slide-5.jpg)


![ВА ⇄ В+ + А‾ Раствор, где [В+]∙[А‾] = ПР, называется](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1406785/slide-8.jpg)





 Изомеризация легких парафиновых углеводородов. Термогидрокаталитические процессы. Гидроочистка нефтяного сырья
Изомеризация легких парафиновых углеводородов. Термогидрокаталитические процессы. Гидроочистка нефтяного сырья Кислородсодержащие органические соединения (К.О.С.)
Кислородсодержащие органические соединения (К.О.С.) Аттестационная работа. Методическая разработка по выполнению исследовательской работы «Тайны поваренной соли»
Аттестационная работа. Методическая разработка по выполнению исследовательской работы «Тайны поваренной соли» Циклоалканы
Циклоалканы Технология производства и свойства искусственных волокон
Технология производства и свойства искусственных волокон Изучение биохимических свойств микробов и их чувствительность к антибиотикам. Микробиологические исследования воды
Изучение биохимических свойств микробов и их чувствительность к антибиотикам. Микробиологические исследования воды Строение атома
Строение атома Пластмаси, синтетичні каучуки Виконала: Учениця 11 – А класу Твердохліб Анжеліка
Пластмаси, синтетичні каучуки Виконала: Учениця 11 – А класу Твердохліб Анжеліка  Коррозия металлов
Коррозия металлов Вода в природе. Свойства воды.
Вода в природе. Свойства воды. Медь. Химические свойства. Получение меди. Применение
Медь. Химические свойства. Получение меди. Применение Материя. Уровни организации материи
Материя. Уровни организации материи Неметаллы. Общая характеристика
Неметаллы. Общая характеристика Масс-спектрометрия (МС)
Масс-спектрометрия (МС) Продукты - рекордсмены по содержанию различных минеральных компонентов
Продукты - рекордсмены по содержанию различных минеральных компонентов Методика изучения периодического закона, периодической системы Д.И. Менделеева и строения атома
Методика изучения периодического закона, периодической системы Д.И. Менделеева и строения атома Кислотность органических соединений. Типы химических реакций
Кислотность органических соединений. Типы химических реакций Галогены
Галогены Теоретические аспекты
Теоретические аспекты Інгібіювання та регуляція ензимів
Інгібіювання та регуляція ензимів Получение и свойства кислорода. Практическая работа № 4
Получение и свойства кислорода. Практическая работа № 4 Типы химических реакции
Типы химических реакции В гостях у Хозяйки Медной горы. Покровская сельская библиотека
В гостях у Хозяйки Медной горы. Покровская сельская библиотека Оксиды. Классификация. Названия
Оксиды. Классификация. Названия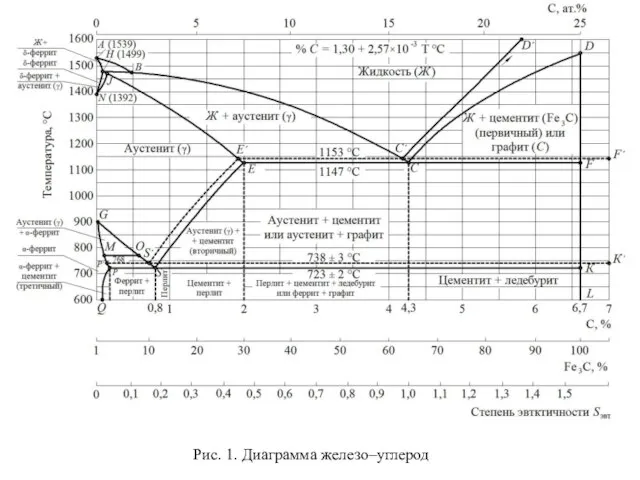 Чугуны и стали
Чугуны и стали Природный и попутный газ
Природный и попутный газ Оксиды (1 курс)
Оксиды (1 курс) Жиры и мыло
Жиры и мыло