Содержание
- 3. Химическая коррозия Химическая коррозия – процесс разрушения металла в результате протекания гетерогенных реакций без возникновения тока
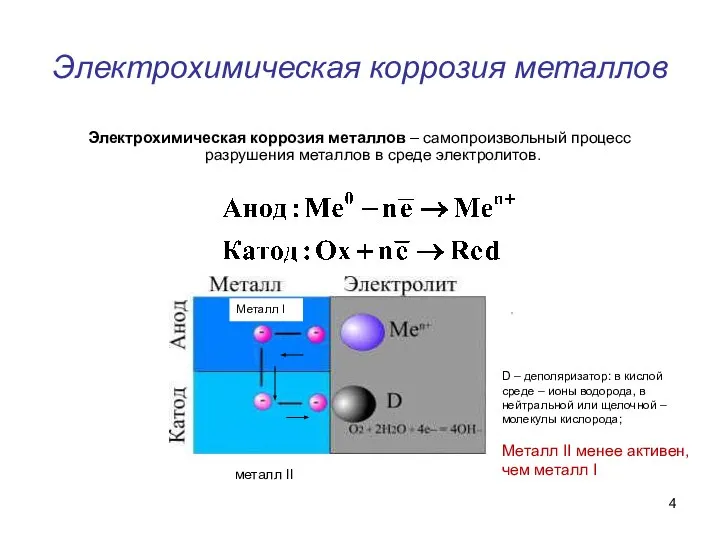
- 4. Электрохимическая коррозия металлов Электрохимическая коррозия металлов – самопроизвольный процесс разрушения металлов в среде электролитов. металл II
- 5. Катодные процессы при протекании коррозии по электрохимическому механизму
- 6. Причины электрохимической коррозии
- 7. Так как то контакт двух разных металлов приводит к тому, что разрушаться будет железо: Контакт двух
- 8. Образующийся гидроксид железа (II) подвергается последующему окислению: Контакт двух разных металлов (щелочная и нейтральная среды)
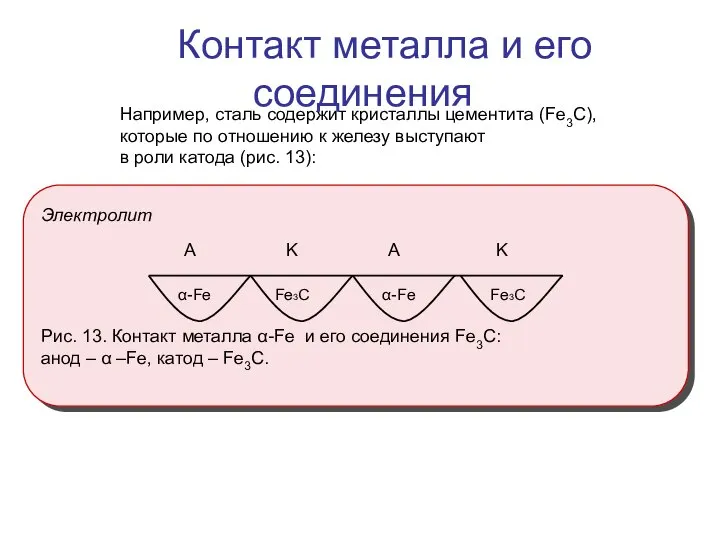
- 9. Например, сталь содержит кристаллы цементита (Fe3C), которые по отношению к железу выступают в роли катода (рис.
- 10. Электродный потенциал окисленного участка выше, чем неокисленного. Окисленные участки выполняют функцию катода. Так, например, если на
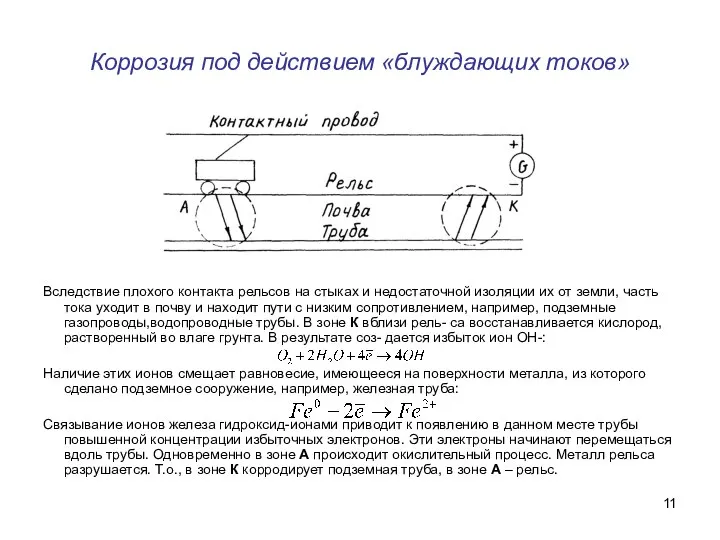
- 11. Коррозия под действием «блуждающих токов» Вследствие плохого контакта рельсов на стыках и недостаточной изоляции их от
- 12. Защита от коррозии
- 13. Все методы защиты металлов от коррозии условно делят на следующие группы: изоляция поверхности металла от окружающей
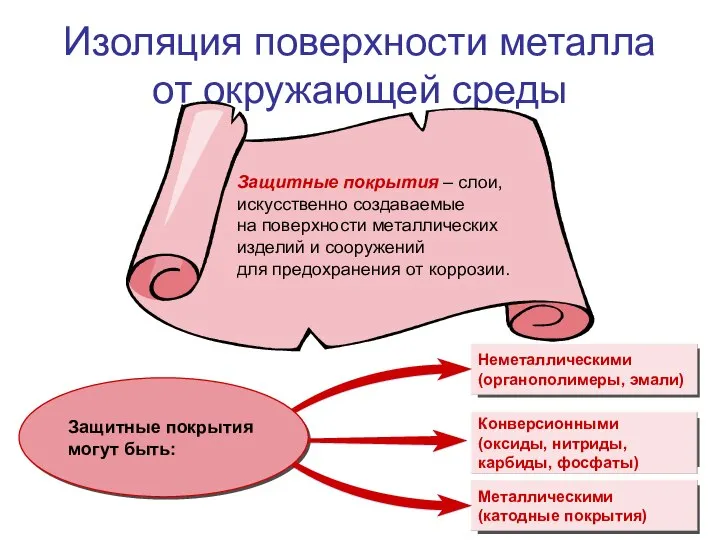
- 14. Изоляция поверхности металла от окружающей среды
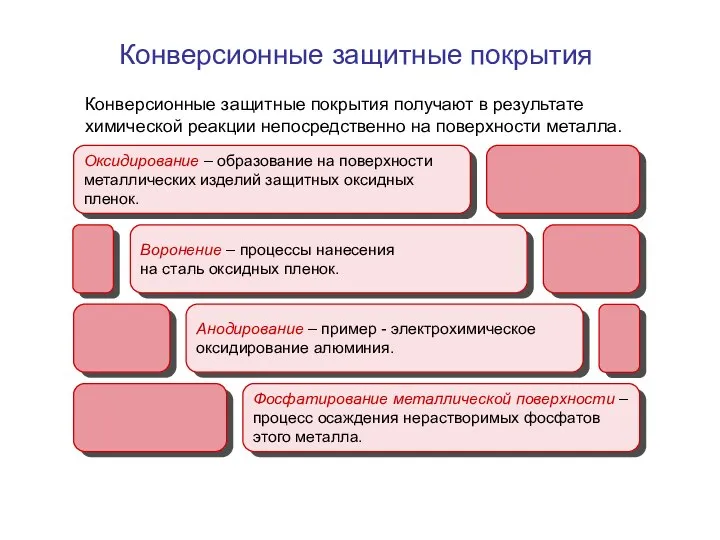
- 15. Конверсионные защитные покрытия получают в результате химической реакции непосредственно на поверхности металла. Конверсионные защитные покрытия
- 16. Металлические защитные покрытия. Катодные покрытия Катодные защитные покрытия – это покрытия металлом, электродный потенциал которого в
- 17. Электрохимическая защита. Анодные металлические покрытия
- 18. Протекторная защита Схема протекторной защиты Анод (Ме-протектор): Катод (Ме трубы) : ( среда – кислая )
- 21. Скачать презентацию













 Круговорот азота в природе
Круговорот азота в природе ЛР и ЛРС содержащие фитоэкдизоны
ЛР и ЛРС содержащие фитоэкдизоны Кислоты, их состав и название. Цель урока: 1. Сформировать понятия о кислотах. 2. Рассмотреть состав, название и классификацию ки
Кислоты, их состав и название. Цель урока: 1. Сформировать понятия о кислотах. 2. Рассмотреть состав, название и классификацию ки Координационные соединения
Координационные соединения Липиды. Общая характеристика липидов
Липиды. Общая характеристика липидов Соединения галогенов
Соединения галогенов Азот и фосфор
Азот и фосфор Химическая технология органических веществ
Химическая технология органических веществ Каталитикалық риформинг
Каталитикалық риформинг Аминокислоты
Аминокислоты Роботу виконав: Желєзний Влад
Роботу виконав: Желєзний Влад  Основания, их состав, номенклатура и основные представители
Основания, их состав, номенклатура и основные представители Элементный, фракционный и химический состав нефти. Классификация нефтей
Элементный, фракционный и химический состав нефти. Классификация нефтей Основные положения теории растворов электролитов, используемых в аналитической химии. (Лекция 3)
Основные положения теории растворов электролитов, используемых в аналитической химии. (Лекция 3) Минералы алюминия
Минералы алюминия Основания: классификация и свойства в свете ТЭД
Основания: классификация и свойства в свете ТЭД Ионная полимеризация. Катионная полимеризация
Ионная полимеризация. Катионная полимеризация Материаловедение. Основы металловедения
Материаловедение. Основы металловедения Изотермический процесс в реакционном объеме. (Тема 6.2)
Изотермический процесс в реакционном объеме. (Тема 6.2) Фенолы Простые эфиры
Фенолы Простые эфиры Альдегиды вокруг нас
Альдегиды вокруг нас Минералы. Определение минералов
Минералы. Определение минералов Курс хімії за 11 клас
Курс хімії за 11 клас Презентация по Химии "Атоми,молекули, йони, хімічні елементи, їхні назви й символи" - скачать смотреть бесплатно
Презентация по Химии "Атоми,молекули, йони, хімічні елементи, їхні назви й символи" - скачать смотреть бесплатно НАШ НЕБЕЗПЕЧНИЙ ПОБУТ Презентація на тему того,про що ми не думаємо у повсякденному житті.
НАШ НЕБЕЗПЕЧНИЙ ПОБУТ Презентація на тему того,про що ми не думаємо у повсякденному житті.  Функциональные производные с простой связью C-“Э”. Часть 4 …окси-производные
Функциональные производные с простой связью C-“Э”. Часть 4 …окси-производные Кремний и его соединения
Кремний и его соединения Презентация по Химии "Химия. Классификация химических реакций" - скачать смотреть бесплатно
Презентация по Химии "Химия. Классификация химических реакций" - скачать смотреть бесплатно