Содержание
- 2. Цели и задачи Цель: развитие знаний обучающихся о необратимых реакциях на примере реакций ионного обмена (РИО)
- 3. Основные понятия Реакция называется необратимой, если один из продуктов реакции является нерастворимым, газообразным или малодиссоциирующим веществом
- 4. Основные понятия Реакциями ионного обмена называются реакции, протекающие между ионами в растворах электролитов Сущность РИО заключается
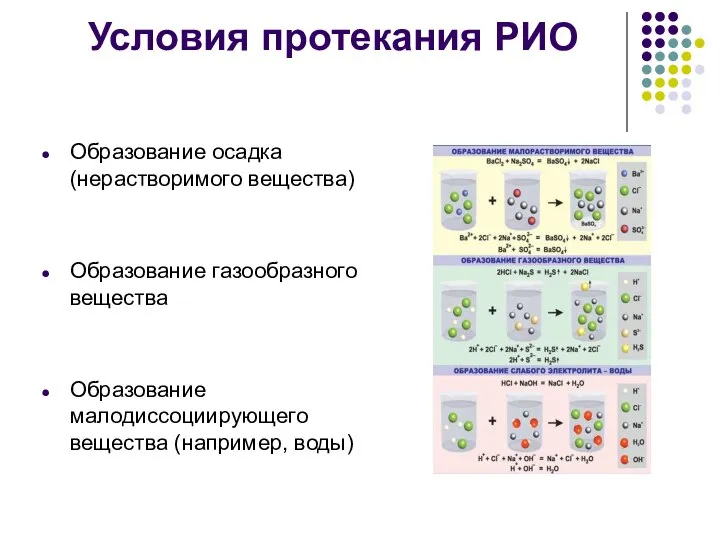
- 5. Условия протекания РИО Образование осадка (нерастворимого вещества) Образование газообразного вещества Образование малодиссоциирующего вещества (например, воды)
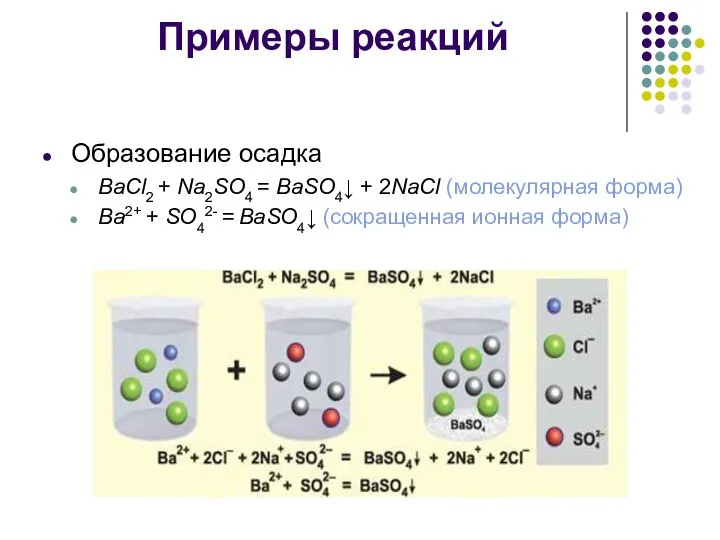
- 6. Примеры реакций Образование осадка BaCl2 + Na2SO4 = BaSO4↓ + 2NaCl (молекулярная форма) Ba2+ + SO42-
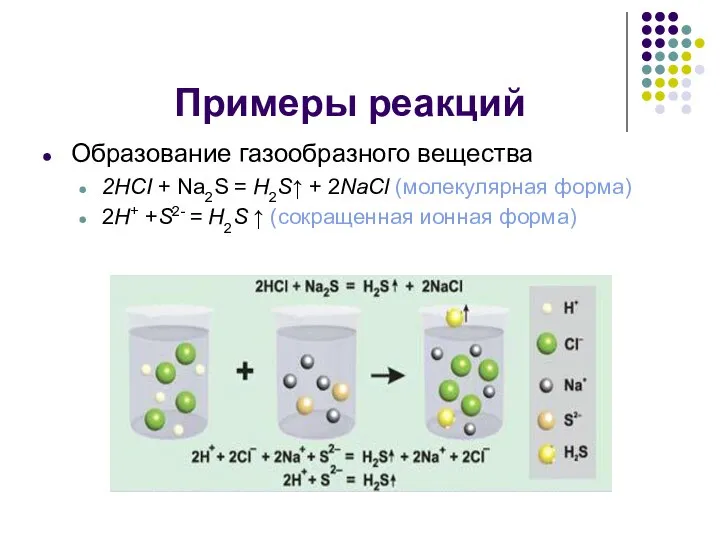
- 7. Примеры реакций Образование газообразного вещества 2HCI + Na2S = H2S↑ + 2NaCl (молекулярная форма) 2H+ +S2-
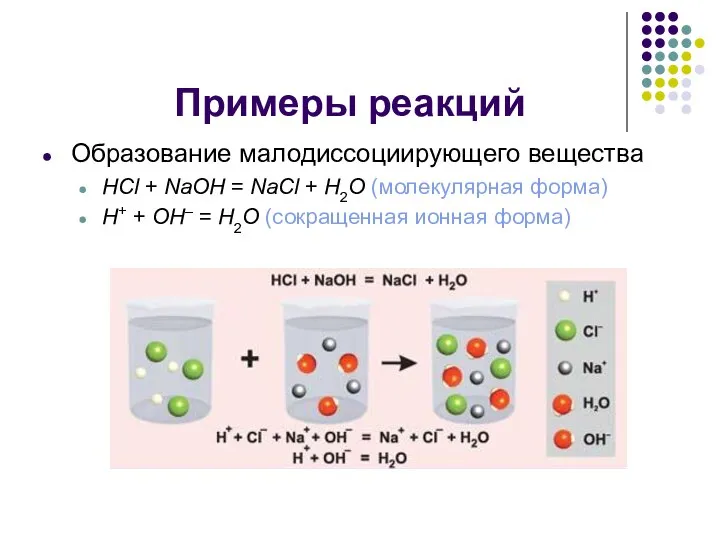
- 8. Примеры реакций Образование малодиссоциирующего вещества HCl + NaOH = NaCl + H2O (молекулярная форма) H+ +
- 9. Примеры заданий для самостоятельной работы Какие из перечисленных реакций относятся к РИО? Ответ обоснуйте AgNO3 +
- 10. Примеры заданий для самостоятельной работы По схемам сокращенных ионных уравнений составить молекулярные и полные ионные уравнения
- 11. Примерный перечень контрольных вопросов Какие реакции называются необратимыми и обратимыми? Какие реакции называются реакциями ионного обмена?
- 12. Примерный перечень контрольных вопросов Приведите примеры реакций ионного обмена в молекулярной и сокращенной ионной формах с
- 13. Рефлексия С какими новыми понятиями вы познакомились на уроке? Какие трудности усвоения материала по данной теме
- 15. Скачать презентацию








 Оксиды азота
Оксиды азота Презентация Лепиды
Презентация Лепиды  Химическая связь. Взаимное влияние атомов в молекуле. Классификация реакций и реагентов. Структура и функции биолекул
Химическая связь. Взаимное влияние атомов в молекуле. Классификация реакций и реагентов. Структура и функции биолекул Лимонная кислота
Лимонная кислота Дисахариды и полисахариды
Дисахариды и полисахариды Переработка гидроминерального сырья
Переработка гидроминерального сырья Підготувала: Учениця 10-Б класу Іщенко Інна
Підготувала: Учениця 10-Б класу Іщенко Інна  Екологічні продукти Знаки світу та України
Екологічні продукти Знаки світу та України  Липиды. Общая характеристика липидов
Липиды. Общая характеристика липидов Производство самодельного мыла: технология, экономика
Производство самодельного мыла: технология, экономика Вуглеводні. Насичені, ненасичені та ароматичні вуглеводні: їх склад, будова, фізичні та хімічні властивості
Вуглеводні. Насичені, ненасичені та ароматичні вуглеводні: їх склад, будова, фізичні та хімічні властивості Дифференциация магмы
Дифференциация магмы Электролиз водных растворов
Электролиз водных растворов Қышқыл жаңбыр
Қышқыл жаңбыр Елементи VІ групи головної підгрупи
Елементи VІ групи головної підгрупи Обобщение
Обобщение Стерилизация технологических потоков и оборудования
Стерилизация технологических потоков и оборудования Влияние этилового спирта на организм детей
Влияние этилового спирта на организм детей Условия осаждения и растворения. (Глава 4. § 19. Задача 11)
Условия осаждения и растворения. (Глава 4. § 19. Задача 11) Углеводы. Глюкоза-представитель моносахаридов
Углеводы. Глюкоза-представитель моносахаридов  Строение атома и химическая связь
Строение атома и химическая связь Все о лаках для волос
Все о лаках для волос Количественное определение лекарственных веществ
Количественное определение лекарственных веществ Пудра. Виды пудр. Процесс изготовления
Пудра. Виды пудр. Процесс изготовления Обменные реакции в растворах электролитов
Обменные реакции в растворах электролитов Вариации химического состава почек берез дендрария Санкт-Петербургской лесотехнической академии
Вариации химического состава почек берез дендрария Санкт-Петербургской лесотехнической академии Серебро. Химические свойства
Серебро. Химические свойства Мыс Cu – элементтердің периодтық жүйесінің І-тобындағы химиялық элемент
Мыс Cu – элементтердің периодтық жүйесінің І-тобындағы химиялық элемент