Содержание
- 2. Магическая кислота Магическая кислота получила своё название за исключительную способность растворять воск. Она является смесью пентафторида
- 3. При содержании SbF5 90% Н0 достигает значения −26,5 в результате дополнительной координации по уравнениям (12) и
- 4. Еще больше кислотность возрастает при растворении SbF5 во фтористом водороде. Уже 1% Уже 1% SbF5 изменяет
- 5. Эквимолярную смесь HSO3F и SbF5 называют «магической кислотой». Сверхкислотность обусловлена исключительной слабостью взаимодействия с протоном соответствующих
- 6. Как влияет вода на силу растворов кислот? 1) Рассмотрим, как протекает процесс растворения сильных электролитов: Растворение
- 7. 2) Некоторые аномалии водных растворов кислот Однако растворы кислот имеют показатели рН, отличные от показателей чистых
- 8. Так как соли, как и кислоты, являются сильными электролитами в воде, то вывод, сделанный Вальденом при
- 9. жидкий аммиак является дифференцирующим растворителем по отношению к сильным основаниям, но нивелирующим по отношению к кислотам
- 10. Влияние жидких метана и этана на силу растворенных кислот Сила кислот в растворителях зависит от диэлектрической
- 11. 2) Влияние диэлектрической проницаемости (ДП) растворителя на силу кислот Влияние диэлектрической проницаемости на силу электролитов достаточно
- 13. Скачать презентацию
Магическая кислота
Магическая кислота получила своё название за исключительную способность растворять воск. Она
Магическая кислота
Магическая кислота получила своё название за исключительную способность растворять воск. Она
Поводом для этого и для осмысления ее необычных свойств послужил забавный случай, когда во время рождественской вечеринки, происходившей в химической лаборатории, в “магическую кислоту” был помещен кусочек свечи, который довольно быстро растворился. Последующее исследование показало, что при этом происходят расщепление и изомеризация молекул длинноцепочечных парафинов, из которых состоит свеча. Тем самым одновременно была открыта и “суперкислотная” химия алканов. Изучение зависимости кислотности смесей HSO3F–SbF5 от их состава показало, что ее резкое повышение (примерно на −4 в шкале Н0) происходит уже при переходе от 100% HSO3F к раствору, содержащему ∼10% кислоты Льюиса, в результате взаимодействий:
HSO3F + SbF5 ⇌ HSbF5SO3F (10)
HSO3F + HSbF5SO3F ⇌ H2SO3F+(SbF5SO3F)− (11)
При содержании SbF5 90% Н0 достигает значения −26,5 в результате дополнительной
При содержании SbF5 90% Н0 достигает значения −26,5 в результате дополнительной
mSbF5 + HSO3F ⇌ HSbmF5mSO3F (12)
HSbnF5nSO3F + HSbmF5mSO3F ⇌ H2SbnF5nSO3F+(SbmF5mSO3F)− (13)
n, m = 1, 2, 3, n ≤ m. При содержании SbF5 50–70% преобладает (∼70%) анион SbF5SO3F− и присутствуют анионы Sb2F10SO3F−, SbF6− и SbF4(SO3F2). Два последних образуются в результате реакции диспропорционирования (14): 2SbF5SO3F− ⇌ SbF4(SO3F2)− + SbF6− (14). Строение комплексных анионов, образующихся в результате реализации равновесий (10)–(14), отображено на рисунке:
Еще больше кислотность возрастает при растворении SbF5 во фтористом водороде. Уже
Еще больше кислотность возрастает при растворении SbF5 во фтористом водороде. Уже
3HF + SbF5 ⇌ H3F2+SbF6− (15)
2HF + nSbF5 ⇌ H2F+SbnF5n + 1 (16)
Эквимолярную смесь HSO3F и SbF5 называют «магической кислотой».
Сверхкислотность обусловлена исключительной слабостью взаимодействия с
Эквимолярную смесь HSO3F и SbF5 называют «магической кислотой».
Сверхкислотность обусловлена исключительной слабостью взаимодействия с
Сильнейшей суперкислотной системой является гексафторсурьмяная кислота, смесь плавиковой кислоты и пентафторида сурьмы. В этой системе плавиковая кислота выделяет протон (H+), а сопряжённое основание (F−) изолируется координационной связью с пентафторидом сурьмы. Так образуется большой октаэдрический анион (SbF6−), являющийся очень слабым нуклеофилом и очень слабым основанием. Став «свободным», протон обусловливает сверхкислотность системы. Фторсурьмяная кислота в 2·1019 раз сильнее 100%-ой серной кислоты. Фторсурьмяная кислота образуется простым смешиванием пентафторида сурьмы и плавиковой кислоты в отношении 1:1.
Гексафторантимонат водорода в смеси с плавиковой кислотой образует самую сильную из известных кислот — гексафтороантимонат(V) фторония H2SbF7.
Как влияет вода на силу растворов кислот?
1) Рассмотрим, как протекает процесс
Как влияет вода на силу растворов кислот?
1) Рассмотрим, как протекает процесс
Растворение есть не только физический, но и химический процесс. Растворы образуются путем взаимодействия частиц растворенного вещества с частицами растворителя. Вода обладает способностью растворять многие вещества, т. е. давать с ними однородные физико-химические системы переменного состава (растворы).
В чем состоит механизм растворения? Молекулы воды в силу особенностей своего строения и возникающего из-за этого вокруг них силового поля обладают способностью притягивать молекулы других веществ. Процесс растворения заключается как раз во взаимодействии частиц растворяющего вещества с частицами воды. При соприкосновении с водой какого-нибудь сильного электролита (например, соли) ионы, образующие кристаллическую решетку, будут притягиваться противоположно заряженными частицами молекул воды. Например, при погружении в воду кристаллов галита ион натрия (катион) будет притягиваться отрицательным полюсом молекулы воды, а ион хлора (анион) — положительным.
В зависимости от природы вещества при его растворении обычно происходит выделение или поглощение тепла. Ионы растворенного вещества притягивают и удерживают вокруг себя определенное число молекул воды, которые образуют оболочку, называемую гидратной. Таким образом, в водном растворе ионы являются гидратированными, т. е. химически связанными с молекулами воды. Например, при растворении серной кислоты в воде раствор нагревается настолько сильно, что вода может закипеть
2) Некоторые аномалии водных растворов кислот
Однако растворы кислот имеют показатели
2) Некоторые аномалии водных растворов кислот
Однако растворы кислот имеют показатели
Данные аномалии объясняются тем, что вода принадлежит к типу нивелирующих растворителей.
Термин «нивелирующие растворители» был введен П.И. Вальденом при изучении диссоциации солей в различных растворителях.
Исследуя диссоциацию солей в разных растворителях, он установил, что в ряде растворителей (в том числе и в различающихся значениями диэлектрической проницаемости) многие соли одинаково хорошо диссоциируют. На основании этого, например, гидроксилсодержащие растворители с различными диэлектрическими проницаемостями (НОН, СН3ОН, С2Н5ОН, С3Н7ОН и т. д.), в которых соли примерно одинаково диссоциированы, Павел Иванович назвал нивелирующими, т. е. сглаживающими различия в силе электролитов. Типичным нивелирующим растворителем в отношении солей является вода. Как известно, почти все соли в воде независимо от их природы — сильные электролиты. Между тем в ряде растворителей с одинаковой диэлектрической проницаемостью степени диссоциации одних и тех же солей сильно различаются. Например, в метаноле (ε=31,5), ацетонитриле (ε=37,5), нитробензоле (ε=34,89) и нитрометане (ε=38,57) коэффициенты электропроводности одних и тех же солей резко различаются.
Так как соли, как и кислоты, являются сильными электролитами в воде,
Так как соли, как и кислоты, являются сильными электролитами в воде,
Это связано с тем, что водном растворе все кислоты с константами кислотности pKa < 0 имеют одинаковые свойства (например, рН растворов). А объясняется это тем, что для таких кислот равновесиев реакции взаимодействия с растворителем – водой практически нацело смещено в сторону образования иона гидроксония H3O+, который является единственной кислотой в растворе. По сути, ион гидроксония представляет собой самую сильную кислоту в водных растворах, поскольку все более сильные кислоты нацело превращаются в него и таким образом выравниваются по своей силе. Например, все кислоты с pKa < 0 (HCl, HBr, H2SO4) нацело диссоциированы в водных растворах.
Аналогичная ситуация наблюдается и в других растворителях: если pKa протонной кислоты в системе «кислота-растворитель» превосходит кислотность протонированного растворителя (его сопряженной кислоты), то происходит полный перенос протонов от кислоты к растворителю и единственной и наиболее сильной кислотой в растворе становятся катионы протонированного растворителя; кислотность раствора при этом определяется кислотностью сопряженной кислоты растворителя.
Из всего вышеизложенного можно сделать вывод, что при рассмотрении магической кислоты в водном растворе ее сила будет равна силе раствора серной кислоты, а значит, мы не сможем отличить две эти кислоты при сравнении их силы, хотя чистая магическая кислота во много раз сильнее читсой серной.
жидкий аммиак является дифференцирующим растворителем по отношению к сильным основаниям, но
жидкий аммиак является дифференцирующим растворителем по отношению к сильным основаниям, но
Влияние жидких метана и этана на силу растворенных кислот
Сила кислот в
Влияние жидких метана и этана на силу растворенных кислот
Сила кислот в
1) Почему алканы относятся к нивелирующим растворителям?
Алканы – химически малоактивные вещества, но суперкислоты, такие, как магическая кислота, протонируют алканы с образованием иона СН3+,который, как и ион гидроксония в воде, является сильнейшей кислотой в растворе и подавляет диссоциацию кислот. Поэтому алканы аналогично воде являются нивелирующими растворителями, и сила суперкислот в них сглаживается до силы иона СН3+.
2) Влияние диэлектрической проницаемости (ДП) растворителя на силу кислот
Влияние диэлектрической проницаемости
2) Влияние диэлектрической проницаемости (ДП) растворителя на силу кислот
Влияние диэлектрической проницаемости
В общем случае, чем больше дипольные моменты молекул растворителя, тем выше его ДП и тем больше его энергия ион-дипольного взаимодействия с молекулами растворенного вещества, а значит, тем больше молекул растворенного вещества диссоциирует на ионы. В неводных растворителях электролиты часто находятся в форме ионных пар. Собственный дипольный момент ионных пар, как правило, очень велик, соответственно, велика и энергия диполь-ди-польного взаимодействия между молекулами ионных пар, заставляющая их собираться в агрегаты, размеры и сложность которых увеличиваются с ростом этой энергии, т. е. с понижением ДП растворителя. Степень агрегации при этом нередко становится столь внушительной, что в растворе образуются микрокристаллы, которые, объединяясь в макрокристалл, выделяются в отдельную твердую фазу, выпадая из раствора.
В растворителях же с низкой диэлектрической проницаемостью, где «разрыв» на ионы происходит главным образом за счет химического взаимодействия, степень диссоциации зависит от индивидуальных химических свойств растворителя.
А поскольку алканы (метан и этан) имеют очень низкие значения ДП (ДП метана равно 1,000953), то распад кислоты на ионы в них ослабляется.
Вывод: в алканах суперкислоты ослабляются и нивелируются по силе, поэтому очевидно, раствор магической кислоты в метане или этане будет во много раз слабее , чем чистая магическая кислота.










 Скорость химических реакций. Факторы, влияющие на скорость химической реакции
Скорость химических реакций. Факторы, влияющие на скорость химической реакции Биологическое окисление-1.Лекция № 4
Биологическое окисление-1.Лекция № 4 Полимерные материалы и изделия. (Лекция 16)
Полимерные материалы и изделия. (Лекция 16) Исследовательская работа учащейся 10 «А» класса Акуловой Татьяны
Исследовательская работа учащейся 10 «А» класса Акуловой Татьяны Классы неорганических веществ
Классы неорганических веществ Опыты с хондроитин сульфатом
Опыты с хондроитин сульфатом Презентация по Химии "Презентация Пестициды" - скачать смотреть
Презентация по Химии "Презентация Пестициды" - скачать смотреть  Викторина по химии
Викторина по химии Химия в загадках
Химия в загадках Характеристика химического элемента S
Характеристика химического элемента S Углеводы: моносахариды, олигосахариды и полисахариды
Углеводы: моносахариды, олигосахариды и полисахариды Роль кварца в процессах зарождения и эволюция жизни
Роль кварца в процессах зарождения и эволюция жизни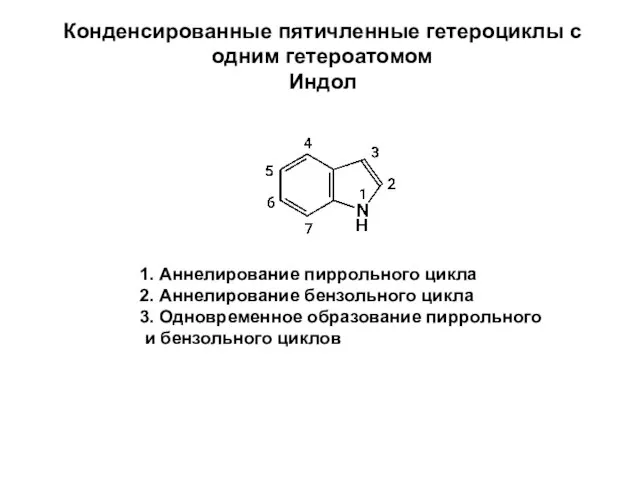 Конденсированные пятичленные гетероциклы с одним гетероатомом. Индол
Конденсированные пятичленные гетероциклы с одним гетероатомом. Индол Алюминий
Алюминий Дисперсные системы. Дисперсионная среда
Дисперсные системы. Дисперсионная среда Эврика – информационный канал
Эврика – информационный канал Ямр на ядрах 14n, 15n. 19f, 31p, лантаноїдні зсуваючі реагенти
Ямр на ядрах 14n, 15n. 19f, 31p, лантаноїдні зсуваючі реагенти Особенности ионообменных реакций с участием биологически активных веществ. Ионообменная сорбция пептидов и белков
Особенности ионообменных реакций с участием биологически активных веществ. Ионообменная сорбция пептидов и белков Органические соединения амины
Органические соединения амины Методы исследования и характеризации поверхностей. Поверхностное и межфазное натяжение. Тензиометрия и эллипсометрия
Методы исследования и характеризации поверхностей. Поверхностное и межфазное натяжение. Тензиометрия и эллипсометрия Задача №7. По щам! Команда Карбораны
Задача №7. По щам! Команда Карбораны Автор: Лисицкая Елена Владимировна учитель физики ГОУ ЦО «Школа здоровья»№ 628.
Автор: Лисицкая Елена Владимировна учитель физики ГОУ ЦО «Школа здоровья»№ 628.  Химия и сельское хозяйство
Химия и сельское хозяйство Карбоновые кислоты
Карбоновые кислоты Фосфориты. Добыча фосфоритов
Фосфориты. Добыча фосфоритов Современные проблемы геологии. Изотопный взгляд на проблему
Современные проблемы геологии. Изотопный взгляд на проблему Тест по неметаллам
Тест по неметаллам Презентация по Химии "Азотсодержащие органические соединения" - скачать смотреть
Презентация по Химии "Азотсодержащие органические соединения" - скачать смотреть