Содержание
- 2. Цели урока Охарактеризовать серу в свете трёх форм существования элемента: в форме атомов, простых веществ (аллотропия),
- 3. План изучения Положение серы в ПСХЭ Строение атома, возможные степени окисления Физические свойства серы Нахождение в
- 4. Положение серы в периодической системе химических элементов Д.И. Менделеева
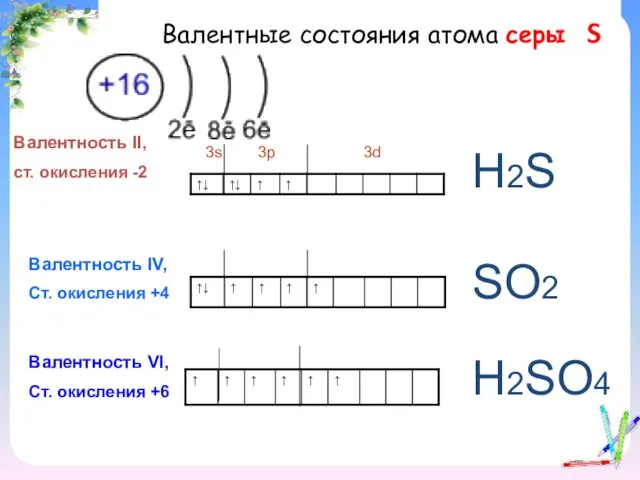
- 5. Валентные состояния атома серы S Валентность II, ст. окисления -2 3s 3p 3d Валентность IV, Ст.
- 6. Физические свойства серы Твёрдое кристаллическое вещество желтого цвета, без запаха Плохо проводит теплоту и не проводит
- 7. Нахождение серы в природе Сера является на 16-м месте по распространённости в земной коре. Встречается в
- 8. Сера также встречается в виде сульфатов - солей серной кислоты - мирабилит
- 9. Пирит – «огненный камень» (соединение серы в природе)
- 10. Сера входит в состав белков. Особенно много серы в белках волос, рогов, шерсти. Кроме этого сера
- 11. Серой богаты бобовые растения (горох, чечевица), овсяные хлопья, яйца
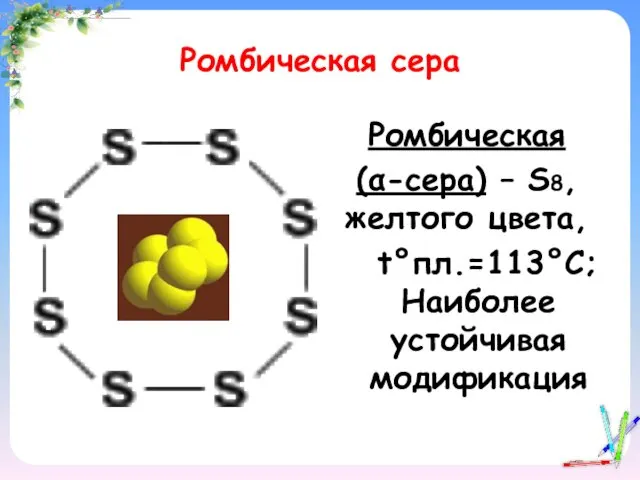
- 13. Ромбическая сера Ромбическая (α-сера) – S8, желтого цвета, t°пл.=113°C; Наиболее устойчивая модификация
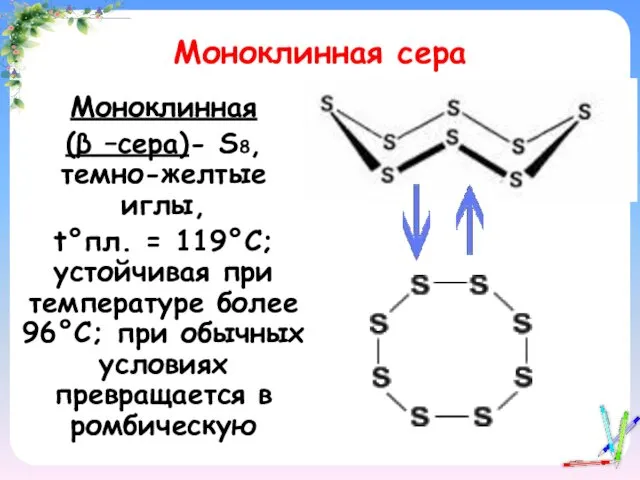
- 14. Моноклинная сера Моноклинная (β –сера)- S8, темно-желтые иглы, t°пл. = 119°C; устойчивая при температуре более 96°С;
- 15. Пластическая сера Пластическая сера- коричневая резиноподобная (аморфная) масса. Она неустойчива и через некоторое время становится хрупкой,
- 16. Химические свойства серы (восстановительные) Сера проявляет в реакциях с сильными окислителями: S - 2ē → S+2;
- 17. Химические свойства серы (окислительные) S0 + 2ē → S-2 4) Сера реагирует со щелочными металлами без
- 18. Применение серы Медицина Производство серной кислоты Сельское хозяйство Производство спичек Производство резины Производство взрывчатых веществ Красители
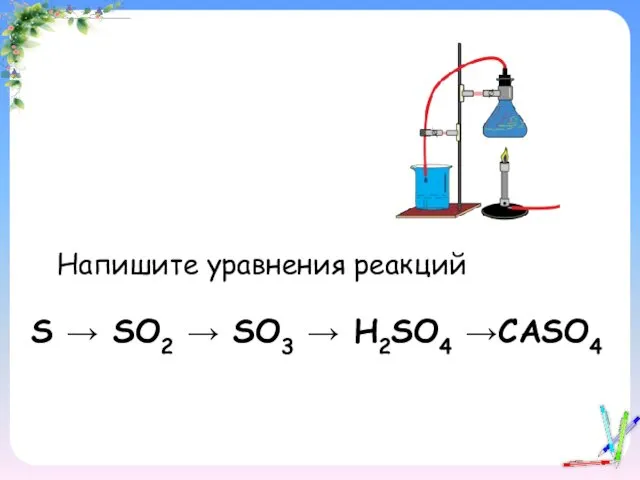
- 19. S → SO2 → SO3 → H2SO4 →CASO4 Напишите уравнения реакций
- 22. Скачать презентацию















 Альтернативная бытовая химия
Альтернативная бытовая химия Тепловой баланс котла
Тепловой баланс котла Полиэтилен высокого давления
Полиэтилен высокого давления Нефть. Состав нефти
Нефть. Состав нефти Диаграммы состояния сплавов, компоненты которых имеют полиморфное превращение
Диаграммы состояния сплавов, компоненты которых имеют полиморфное превращение Соединения химических элементов Степень окисления Составила учитель химии МБОУ «Октябрьская ООШ №2» Потапова Нина Ивановна
Соединения химических элементов Степень окисления Составила учитель химии МБОУ «Октябрьская ООШ №2» Потапова Нина Ивановна Антибиотики-аминогликозиды: получение, свойства, исследование и применение. Связь между химическим строением и действием
Антибиотики-аминогликозиды: получение, свойства, исследование и применение. Связь между химическим строением и действием Геология полезных ископаемых
Геология полезных ископаемых Классификация нефтей и нефтепродуктов
Классификация нефтей и нефтепродуктов Электрохимические процессы и явления
Электрохимические процессы и явления Производство серной кислоты
Производство серной кислоты Жиры. Классификация жиров
Жиры. Классификация жиров Кислород. Историческая справка
Кислород. Историческая справка Карбоновые кислоты
Карбоновые кислоты Презентация по Химии "Почему золото блестит?" - скачать смотреть
Презентация по Химии "Почему золото блестит?" - скачать смотреть  10 лекарств, которые изменили мир Ермуканова Закия 10 кл МОУ «СОШ №7 г.Соль –Илецка» Оренбургской области Рук. Сивожелезова Т.Г.
10 лекарств, которые изменили мир Ермуканова Закия 10 кл МОУ «СОШ №7 г.Соль –Илецка» Оренбургской области Рук. Сивожелезова Т.Г.  Физические и химические свойства алмаза. Алмазная промышленность в России
Физические и химические свойства алмаза. Алмазная промышленность в России Физико-химические методы анализа. Общая характеристика. Особенности и области применения
Физико-химические методы анализа. Общая характеристика. Особенности и области применения Оценка химической обстановки при авариях на химически опасных объектах
Оценка химической обстановки при авариях на химически опасных объектах Формування ВМ з заданою структурою
Формування ВМ з заданою структурою Типы химических связей
Типы химических связей Качественный анализ (часть 2)
Качественный анализ (часть 2) Информационно-поисковый исследовательский проект: «Влияние пищевых добавок на здоровье человека».
Информационно-поисковый исследовательский проект: «Влияние пищевых добавок на здоровье человека». Предельные углеводороды. (9 класс)
Предельные углеводороды. (9 класс) Применение муравьиного спирта
Применение муравьиного спирта Общая характеристика неметаллов
Общая характеристика неметаллов Термохимия. Расчетные задачи. (Лекция 4.2)
Термохимия. Расчетные задачи. (Лекция 4.2) Карбонильные соединения – альдегиды
Карбонильные соединения – альдегиды