Содержание
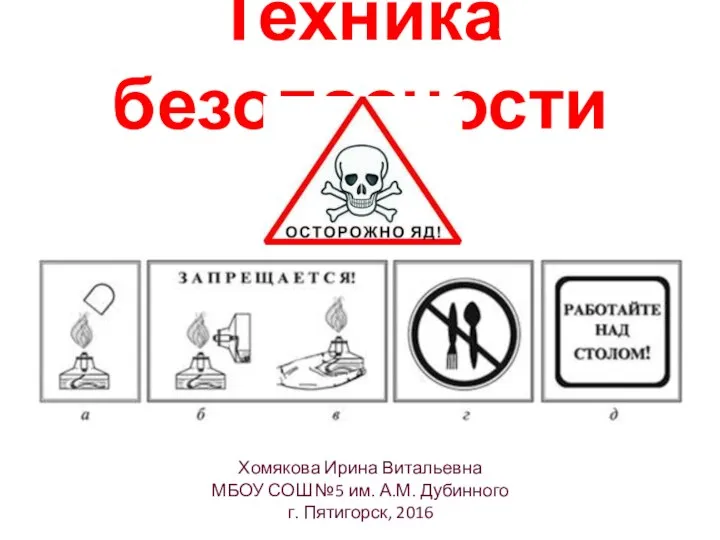
- 2. Техника безопасности Хомякова Ирина Витальевна МБОУ СОШ №5 им. А.М. Дубинного г. Пятигорск, 2016
- 3. Что такое качественный анализ? Качественный анализ – это идентификация (обнаружение) компонентов анализируемых веществ и материалов и
- 4. Аналитическая реакция – это реакция, которая сопровождается каким-либо внешним эффектом (образование или растворение осадка, выделение газа,
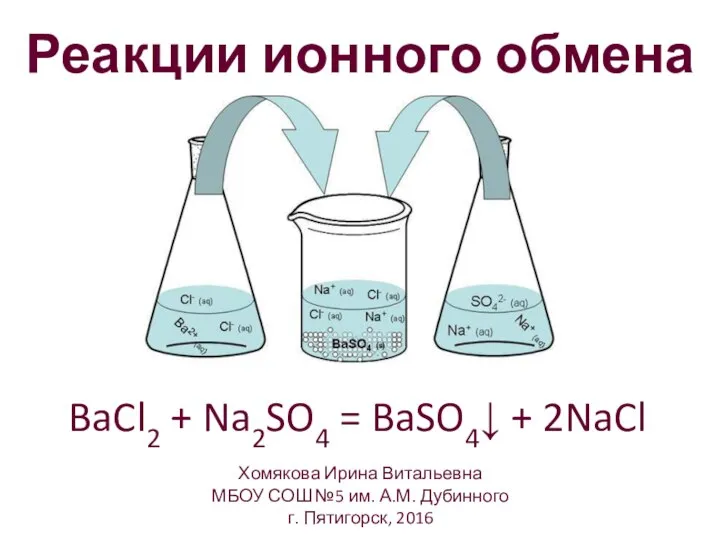
- 5. Реакции ионного обмена BaCl2 + Na2SO4 = BaSO4↓ + 2NaCl Хомякова Ирина Витальевна МБОУ СОШ №5
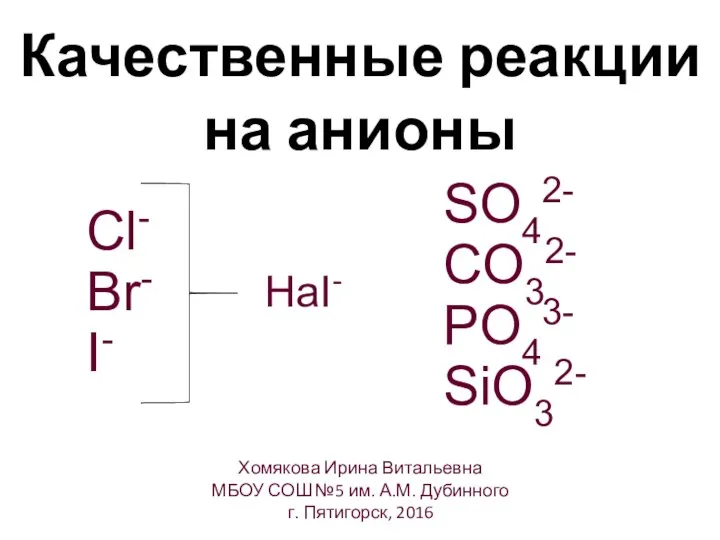
- 7. Качественные реакции на анионы Cl- Br- I- SO42- CO32- PO43- SiO32- HaI- Хомякова Ирина Витальевна МБОУ
- 8. Качественная реакция на Hal- Pb2+ + 2Cl- = PbCl2↓ Hg22+ + 2Cl- = Hg2Cl2↓ Pb2+ +
- 9. Качественная реакция на SO42- Pb2+ + 2Cl- = PbCl2↓ Hg22+ + 2Cl- = Hg2Cl2↓ Pb2+ +
- 10. Качественная реакция на CO32- Pb2+ + 2Cl- = PbCl2↓ Hg22+ + 2Cl- = Hg2Cl2↓ Pb2+ +
- 11. Качественная реакция на PO43- Pb2+ + 2Cl- = PbCl2↓ Hg22+ + 2Cl- = Hg2Cl2↓ Pb2+ +
- 12. Качественная реакция на SiO32- 2H+ + SiO32– = H2SO3↓ К анализируемому раствору добавить р-р сильной кислоты
- 14. Скачать презентацию








 Азотсодержащие соединения
Азотсодержащие соединения Химический состав молока
Химический состав молока Излучение и поглощение света атомами. Виды спектров, спектральный анализ
Излучение и поглощение света атомами. Виды спектров, спектральный анализ Аморфные тела
Аморфные тела Гетерофункциональные органические соединения и их производные – метаболиты и биорегуляторы
Гетерофункциональные органические соединения и их производные – метаболиты и биорегуляторы Личностно – ориентированный подход в обучении химии Талавир С.Е. Учитель химии МОУ СОШ№5
Личностно – ориентированный подход в обучении химии Талавир С.Е. Учитель химии МОУ СОШ№5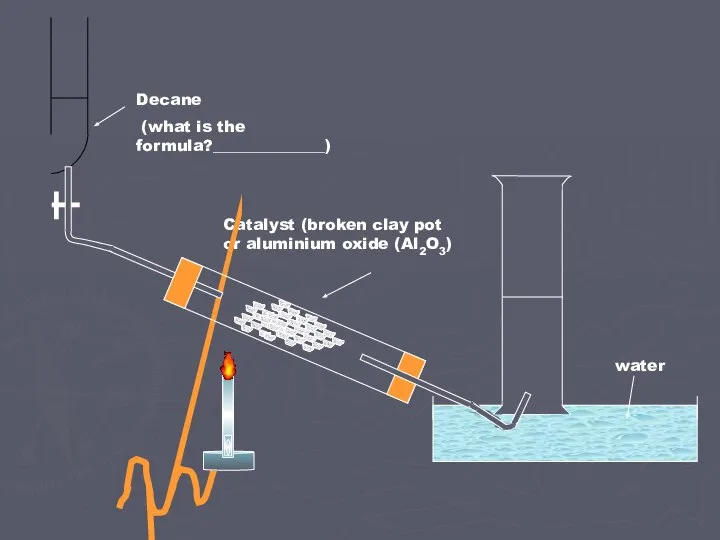 Addition reactions
Addition reactions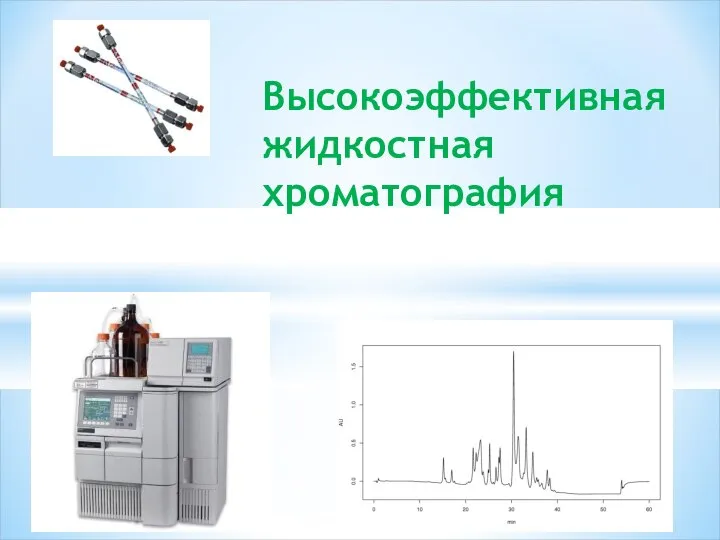 Высокоэффективная жидкостная хроматография (ВЭЖХ)
Высокоэффективная жидкостная хроматография (ВЭЖХ) Осадительное титрование
Осадительное титрование Белковые вещества
Белковые вещества Атомно-молекулярное учение. (Лекция 1)
Атомно-молекулярное учение. (Лекция 1) Застосування вуглеводів. Їх біологічна роль
Застосування вуглеводів. Їх біологічна роль Классификация неорганических веществ
Классификация неорганических веществ Щелочные металлы
Щелочные металлы Роль органической химии в жизни человека
Роль органической химии в жизни человека Занимательная игра по химии
Занимательная игра по химии Учение о растворах
Учение о растворах Человек и отходы «Человечество не погибнет в атомном кошмаре, оно захлебнется в собственных отходах» Нильс Бор. Автор: Георги
Человек и отходы «Человечество не погибнет в атомном кошмаре, оно захлебнется в собственных отходах» Нильс Бор. Автор: Георги Катаболизм пуриновых нуклеотидов
Катаболизм пуриновых нуклеотидов Функциональные производные с кратной связью C=“Э”. Часть 1. Карбонильные соединения и имины
Функциональные производные с кратной связью C=“Э”. Часть 1. Карбонильные соединения и имины Кислоты
Кислоты Классификация металлов в соответствии с ионным потенциалом и параметром мягкости
Классификация металлов в соответствии с ионным потенциалом и параметром мягкости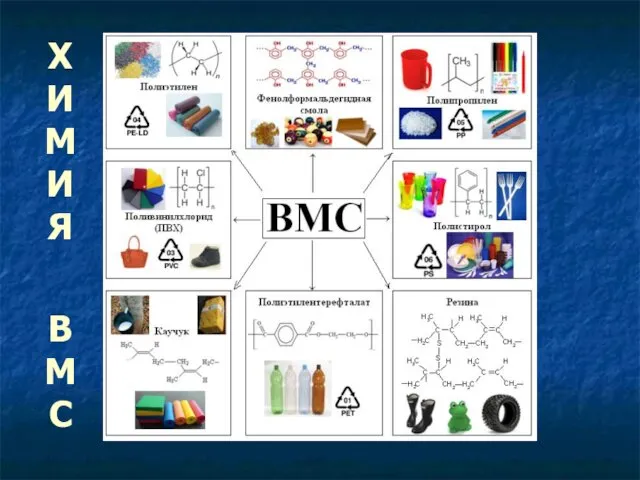 Химия высокомолекулярных соединений (ВМС)
Химия высокомолекулярных соединений (ВМС) Предельные углеводороды. Алканы
Предельные углеводороды. Алканы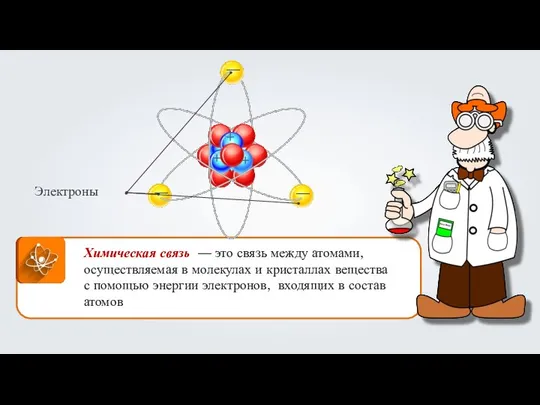 Взаимодействие атомов элементов-металлов и элементов-неметаллов между собой. Ионная связь. (Тема 10)
Взаимодействие атомов элементов-металлов и элементов-неметаллов между собой. Ионная связь. (Тема 10)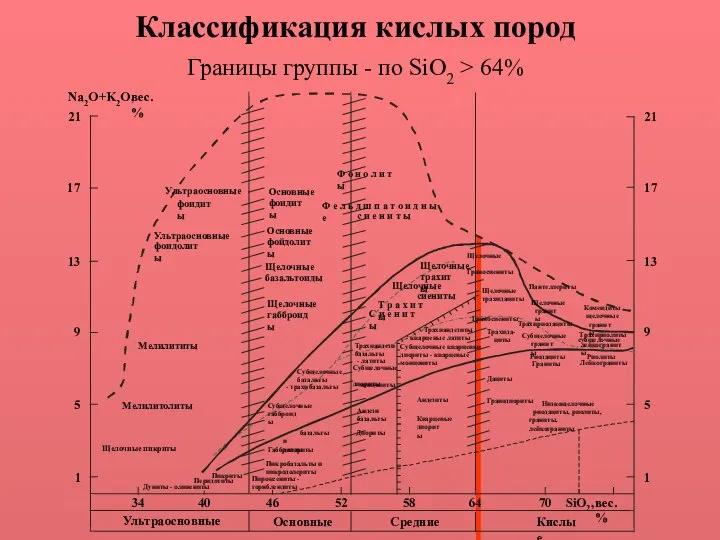 Классификация кислых пород
Классификация кислых пород Тренировочный тест. Уравнение состояния идеального газа
Тренировочный тест. Уравнение состояния идеального газа Химия - наука о веществах, их свойствах и превращениях. Понятие о химическом элементе и формах его существования
Химия - наука о веществах, их свойствах и превращениях. Понятие о химическом элементе и формах его существования