Содержание
- 2. Оксид серы (VI), серный ангидрид, триоксид серы Ковалентная полярная связь Молекулярная кристаллическая решетка
- 3. Физические свойства серного ангидрида Бесцветная, летучая, маслянистая жидкость, t° пл. = 17°C; t° кип. = 45°С;
- 4. Химические свойства I. - SO3 кислотный оксид 1)… 2)… 3)…
- 5. Химические свойства оксида серы (IV) 1. Кислотный оксид +Вода= Кислота SO3 + H2O = H2SO4 2.
- 6. Получение оксида серы (VI) 1. Окисление оксида серы (IV) …
- 7. Получение оксида серы (VI) SO2 + O2 = SO3 Оксид Оксид серы (IV) серы (VI)
- 8. H2SO4 серная кислота Дать классификацию серной кислоте.
- 9. По основности: двухосновная По наличию кислорода: кислородосодержащая По силе: сильный электролит H2SO4 классификация
- 10. Тяжелая маслянистая жидкость («купоросное масло») ρ = 1,84 г/см3 Нелетучая, очень хорошо растворима в воде –
- 11. Химические свойства H2SO4 С металлами (в ряду активности металлов до Н): H2SO4+Zn = … + …
- 12. Химические свойства H2SO4 С металлами (в ряду активности металлов до Н): H2SO4+Zn=ZnSO4 + H2 2. С
- 13. Качественная реакция на ион SO42- Реактивом на серную кислоту и ее соли является катион бария ,
- 14. Концентрированная серная кислота Серная кислота(конц) восстанавливается до (Н2S,S,SO2) в зависимости от активности металла и условий протекания
- 15. Автоцистерна для перевозки серной кислоты
- 16. Применение серной кислоты. 1. В производстве минеральных удобрений 2. Как электролит в свинцовых аккумуляторах 3. Для
- 18. Скачать презентацию















 Резина. Состав и применение резины
Резина. Состав и применение резины Теория теплового воспламенения газовых смесей
Теория теплового воспламенения газовых смесей Строение атома. 8 класс
Строение атома. 8 класс Строение молекулы воды
Строение молекулы воды Термодинамикалық тепе-теңдіктің заңдары
Термодинамикалық тепе-теңдіктің заңдары Химические связи
Химические связи Алкены. Свойства. 10 класс
Алкены. Свойства. 10 класс Индол. Методы синтеза. Химические свойства. Биологически активные производные. (Лекция 4)
Индол. Методы синтеза. Химические свойства. Биологически активные производные. (Лекция 4) Презентация по Химии "Изотопы" - скачать смотреть
Презентация по Химии "Изотопы" - скачать смотреть  Эндогенная серия. Магматическая группа
Эндогенная серия. Магматическая группа ХИМИЧЕСКАЯ СВЯЗЬ В КОМПЛЕКСНЫХ СОЕДИНЕНИЯХ 1. Метод валентных связей (ВС). 2. Теория кристаллического поля (ТКП). 3. Метод мо
ХИМИЧЕСКАЯ СВЯЗЬ В КОМПЛЕКСНЫХ СОЕДИНЕНИЯХ 1. Метод валентных связей (ВС). 2. Теория кристаллического поля (ТКП). 3. Метод мо Смесеобразование и сгорание топлива в цилиндрах дизеля
Смесеобразование и сгорание топлива в цилиндрах дизеля Промышленные аварии с выбросом опасных химических веществ
Промышленные аварии с выбросом опасных химических веществ Протолитические равновесия в растворах электролитов
Протолитические равновесия в растворах электролитов Коррозия металлов
Коррозия металлов Исследовательская работа по химии “Минеральные краски’’
Исследовательская работа по химии “Минеральные краски’’ История открытия стекла Выполняла работу: Заривная Виктория 10 - Л
История открытия стекла Выполняла работу: Заривная Виктория 10 - Л  Атомный уровень. Химия простых веществ. Молекулярный уровень. Химия соединений. Живое субклеточный уровень
Атомный уровень. Химия простых веществ. Молекулярный уровень. Химия соединений. Живое субклеточный уровень Индивидуальные задания для самостоятельной работы студентов нехимических специальностей
Индивидуальные задания для самостоятельной работы студентов нехимических специальностей Возобновляемое сырье органической химии
Возобновляемое сырье органической химии Дезактивація радіаційних речовин у зоні ядерного ураження
Дезактивація радіаційних речовин у зоні ядерного ураження КАРБАМІД
КАРБАМІД  Презентация по Химии "Синтетичні мийні засоби" - скачать смотреть бесплатно
Презентация по Химии "Синтетичні мийні засоби" - скачать смотреть бесплатно Кислоты
Кислоты Азотсодержащие органические соединения
Азотсодержащие органические соединения Презентация по Химии "Пищевые добавки. Е - коды" - скачать смотреть
Презентация по Химии "Пищевые добавки. Е - коды" - скачать смотреть 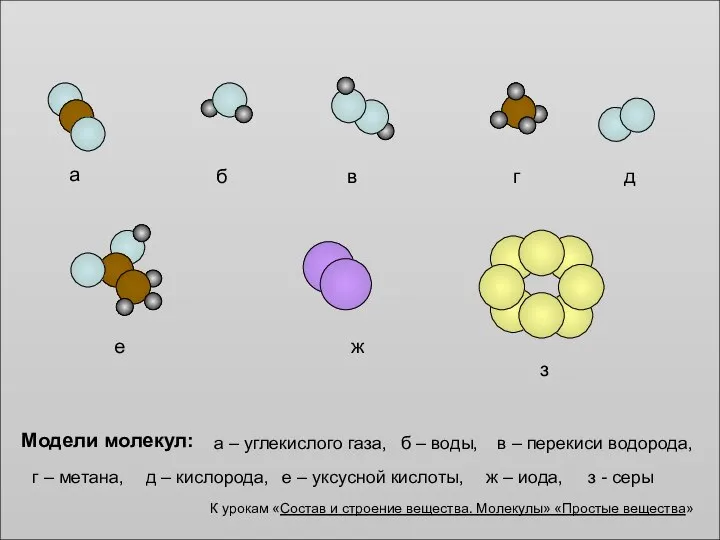 Состав и строение вещества. Молекулы
Состав и строение вещества. Молекулы Сложные эфиры
Сложные эфиры