Содержание
- 2. ЩЕЛОЧНОЗЕМЕЛЬНЫЕ МЕТАЛЛЫ
- 3. Положение в ПСХЭ Д.И. Менделеева и строение атомов 2 группа, А- подгруппа, на внешних уровнях по
- 4. СТРОЕНИЕ АТОМА КАЛЬЦИЯ
- 5. ФИЗИЧЕСКИЕ СВОЙСТВА Открыт в 1798 году французским химиком Луи Никола Вокленом, который назвал его глюцинием. Современное
- 6. Название элемента происходит от лат. calx (в родительном падеже calcis) — «известь», «мягкий камень». Оно было
- 7. НАХОЖДЕНИЕ В ПРИРОДЕ В земной коре содержится бериллия - 0,00053%, магния - 1,95%, кальция - 3,38%,
- 8. ХИМИЧЕСКИЕ СВОЙСТВА Очень реакционноспособны, сильные восстановители. Активность металлов и их восстановительная способность увеличивается в ряду: Be–Mg–Ca–Sr–Ba.
- 9. 3) Взаимодействие с неметаллами: Be + Cl2 → BeCl2 (галогениды) Ba + S → BaS (сульфиды)
- 10. ВАЖНЕЙШИЕ СОЕДИНЕНИЯ КАЛЬЦИЯ Окси́д ка́льция (окись кальция, негашёная и́звесть, «кипелка») формула CaO. Получение в промышленности Обжиг
- 11. ГИДРОКСИД КАЛЬЦИЯ (ГАШЕНАЯ ИЗВЕСТЬ, «ПУШОНКА» Получение: (гашение) CaO+H2O→ Ca(OH)2 (гашеная известь) ПРИМЕНЕНИЕ Гашёная известь — так
- 12. Л/о №10 Ознакомление со свойствами и превращениями карбонатов и гидрокарбонатов Написать уравнения реакций
- 14. ПРИМЕНЕНИЕ СОЛЕЙ КАЛЬЦИЯ В своей работе специалисты разных областей знаний не могут обойтись без соединений щелочноземельных
- 15. Хирург: гипс используем и мы, медики, для наложения фиксирующих гипсовых повязок. Сульфат магния, известный под названием
- 16. Стоматолог: а сколько соединений кальция в составе любой зубной пасты! Из зубной пасты доставляются кальций, фосфор
- 18. Скачать презентацию
ЩЕЛОЧНОЗЕМЕЛЬНЫЕ МЕТАЛЛЫ
ЩЕЛОЧНОЗЕМЕЛЬНЫЕ МЕТАЛЛЫ
Положение в ПСХЭ Д.И. Менделеева и строение атомов
2 группа, А- подгруппа,
Положение в ПСХЭ Д.И. Менделеева и строение атомов
2 группа, А- подгруппа,
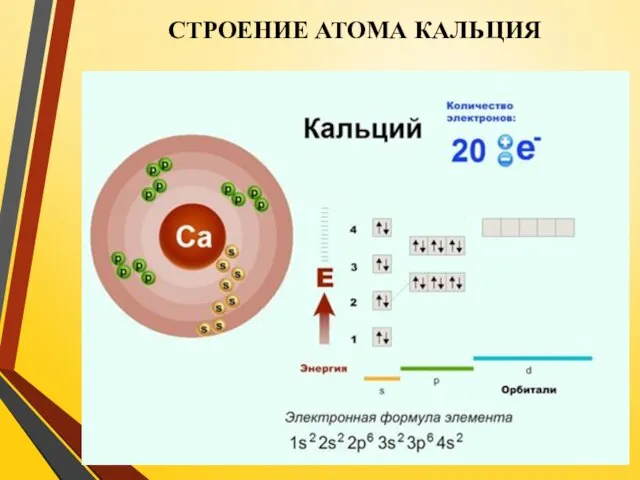
СТРОЕНИЕ АТОМА КАЛЬЦИЯ
СТРОЕНИЕ АТОМА КАЛЬЦИЯ
ФИЗИЧЕСКИЕ СВОЙСТВА
Открыт в 1798 году французским химиком Луи Никола Вокленом, который
ФИЗИЧЕСКИЕ СВОЙСТВА
Открыт в 1798 году французским химиком Луи Никола Вокленом, который
Бериллий — относительно твёрдый (5,5 баллов по Моосу), но хрупкий металл серебристо-белого цвета. Один из самых твёрдых металлов в чистом виде (уступает только иридию, осмию, вольфраму и урану). На воздухе активно покрывается стойкой оксидной плёнкой BeO. Плотность (при н. у.) 1,848 г/см³.Температура плавления 1278 °C, температура кипения 2970 °C.
В 1808 г. английский химик Гемфри Дэви с помощью электролиза увлажнённой смеси магнезии и оксида ртути получил амальгаму неизвестного металла, которому дал название «магнезиум», сохранившееся до сих пор во многих странах. В России с 1831 года принято название «магний». В 1829 г. французский химик А. Бюсси получил магний, восстанавливая его расплавленный хлорид металлическим калием. В 1830 г. М. Фарадей получил магний электролизом расплавленного хлорида магния.
Магний — металл серебристо-белого цвета, обладает металлическим блеском. При обычных условиях поверхность магния покрыта довольно прочной защитной плёнкой оксида магния MgO, которая разрушается при нагреве на воздухе до примерно 600 °C, после чего металл сгорает с ослепительно белым пламенем с образованием оксида и нитрида магния Mg3N2. На горящий магний желательно смотреть только через темные очки или стекло, так как в противном случае есть риск получить световой ожог сетчатки и на время ослепнуть. Плотность магния при 20 °C — 1,738 г/см³, температура плавления 650 °C, температура кипения 1090 °C. Магний высокой чистоты пластичен, хорошо прессуется, прокатывается и поддаётся обработке резанием.
Название элемента происходит от лат. calx (в родительном падеже calcis) —
Название элемента происходит от лат. calx (в родительном падеже calcis) —
Серебристый металл, плотность (при н. у.) 1,55 г/см3, температура плавления 838,85 °C, температура кипения 1483,85 °C.
Обнаружили в минерале стронцианите, найденном в 1764 году в свинцовом руднике близ шотландской деревни Стронти́ан[en] (англ. Strontian, гэльск. Sron an t-Sìthein), давшей впоследствии название новому элементу. Присутствие в этом минерале оксида нового металла было установлено в 1787 году Уильямом Крюйкшенком и Адером Кроуфордом. Выделен в чистом виде сэром Хемфри Дэви в 1808 году.
Стронций — мягкий серебристо-белый металл, обладает ковкостью и пластичностью, легко режется ножом. Температура плавления: 768 °С, температура кипения: 1390 °С.
Барий был открыт в виде оксида BaO в 1774 г. Карлом Шееле и Юханом Ганом. В 1808 году английский химик Гемфри Дэви электролизом выделил металлический барий.
Барий — серебристо-белый ковкий металл. При резком ударе раскалывается. Плотность 3,5 г/см³.
НАХОЖДЕНИЕ В ПРИРОДЕ
В земной коре содержится бериллия - 0,00053%, магния -
НАХОЖДЕНИЕ В ПРИРОДЕ
В земной коре содержится бериллия - 0,00053%, магния -
Встречаются в природе только в виде соединений - силикатов, алюмосиликатов, карбонатов, фосфатов, сульфатов и т.д.
Be
3BeO • Al2O3 • 6SiO2 или Al2[Be3(Si6O18)] – берилл
Mg
MgCO3 – магнезит, CaCO3 • MgCO3 – доломит
KCl • MgSO4 • 3H2O – каинит, KCl • MgCl2 • 6H2O – карналлит, MgCl2•6H2O - бишофит
ХИМИЧЕСКИЕ СВОЙСТВА
Очень реакционноспособны, сильные восстановители.
Активность металлов и их восстановительная способность
ХИМИЧЕСКИЕ СВОЙСТВА
Очень реакционноспособны, сильные восстановители.
Активность металлов и их восстановительная способность
1) Взаимодействие с водой.
В обычных условиях поверхность Be и Mg покрыты инертной оксидной пленкой, поэтому они устойчивы по отношению к воде. В отличие от них Ca, Sr и Ba растворяются в воде с образованием гидроксидов, которые являются сильными основаниями:
Ве + H2O → ВеO+ H2↑
Ca + 2H2O → Ca(OH)2 + H2↑
2) Взаимодействие с кислородом.
Все металлы образуют оксиды МеO, барий образует пероксид – BaO2:
2Mg + O2 → 2MgO
Ba + O2 → BaO2
ПОЛУЧЕНИЕ- ЭЛЕКТРОЛИЗ СОЛЕЙ
3) Взаимодействие с неметаллами:
Be + Cl2 → BeCl2 (галогениды) Ba + S → BaS (сульфиды)
3Mg + N2 → Mg3N2 (нитриды) Ca + H2 → CaH2 (гидриды)
Ca + 2C → CaC2 (карбиды) 3Ba + 2P → Ba3P2 (фосфиды)
Бериллий и магний
3) Взаимодействие с неметаллами:
Be + Cl2 → BeCl2 (галогениды) Ba + S → BaS (сульфиды)
3Mg + N2 → Mg3N2 (нитриды) Ca + H2 → CaH2 (гидриды)
Ca + 2C → CaC2 (карбиды) 3Ba + 2P → Ba3P2 (фосфиды)
Бериллий и магний
4) Взаимодействие с кислотами:
Ca + 2HCl → CaCl2 + H2
Mg + H2SO4(разб.) → MgSO4 + H2
Бериллий также растворяется в водных растворах щелочей (амфотерные свойства):
Be + 2NaOH + 2H2O → Na2[Be(OH)4] + H2
Качественная реакция на катионы щелочноземельных металлов – окрашивание пламени в следующие цвета:
Ca2+ - темно-оранжевый Sr2+- темно-красный Ba2+ - светло-зеленый
Катион Ba2+ обычно открывают обменной реакцией с серной кислотой или ее солями: BaCl2 + H2SO4 → BaSO4↓ + 2HCl
Ba2+ + SO42- → BaSO4↓
Сульфат бария – белый осадок, нерастворимый в минеральных
кислотах.
ВАЖНЕЙШИЕ СОЕДИНЕНИЯ КАЛЬЦИЯ
Окси́д ка́льция (окись кальция, негашёная и́звесть, «кипелка») формула CaO.
ВАЖНЕЙШИЕ СОЕДИНЕНИЯ КАЛЬЦИЯ
Окси́д ка́льция (окись кальция, негашёная и́звесть, «кипелка») формула CaO.
Получение в промышленности
Обжиг известняка:
CaCO3 t˚C→ CaO + CO2
Химические свойства
Типичный основный оксид. Реагирует с водой, кислотными оксидами и кислотами:
СаO + H2O → Са(OH)2 + Q; (гашение извести)
СаО + SO3 → CaSO4;
СаО + 2HCI → CaCI2 + H2O.
Физические свойства
Тугоплавкое вещество белого цвета, температура плавления 2570°С.
ГИДРОКСИД КАЛЬЦИЯ (ГАШЕНАЯ ИЗВЕСТЬ, «ПУШОНКА»
Получение: (гашение)
CaO+H2O→ Ca(OH)2 (гашеная известь)
ПРИМЕНЕНИЕ
Гашёная известь — так как
ГИДРОКСИД КАЛЬЦИЯ (ГАШЕНАЯ ИЗВЕСТЬ, «ПУШОНКА»
Получение: (гашение)
CaO+H2O→ Ca(OH)2 (гашеная известь)
ПРИМЕНЕНИЕ
Гашёная известь — так как
Известковое молоко — взвесь (суспензия), образуемая при смешивании избытка гашёной извести с водой. Похожа на молоко. (получение хлорной извести, производство сахара, для борьбы с болезнями растений)
Известковая вода — прозрачный раствор гидроксида кальция, получаемый при фильтровании известкового молока. (для обнаружения углекислого газа)
Белый (иногда серый) порошок, мало растворимый в воде, растворимость падает с ростом температуры.
ХИМИЧЕСКИЕ СВОЙСТВА
Реакции с кислотными оксидами: Ca(OH)2 + СO2 → CaСO3↓ + H2O
Л/о №10 Ознакомление со свойствами и превращениями карбонатов и гидрокарбонатов
Написать уравнения
Л/о №10 Ознакомление со свойствами и превращениями карбонатов и гидрокарбонатов
Написать уравнения
ПРИМЕНЕНИЕ СОЛЕЙ КАЛЬЦИЯ
В своей работе специалисты разных областей знаний не могут
ПРИМЕНЕНИЕ СОЛЕЙ КАЛЬЦИЯ
В своей работе специалисты разных областей знаний не могут
Строитель: самый важный из минералов – известняк (карбонат кальция), без которого не обходится ни одно строительство. Во-первых, он сам является прекрасным строительным камнем. Во-вторых, это сырьё для получения цемента, гашёной и негашёной извести, стекла и др. Известковой щебёнкой укрепляют дороги. Природный мел представляет собой остатки раковин древних животных. Мел применяют для побелки, а также и в школе – школьный мел.
Агроном: среднего содержания кальция в почвах (1,37%) вполне достаточно для обеспечения физиологических потребностей растений. Тем не менее, соединения кальция вносят в почвы для химической мелиорации: известковым порошком уменьшают кислотность почв, гипсованием устраняют избыточную щёлочность. Нитрат и фосфаты кальция используются как азотные удобрения.
Скульптор: минерал скульпторов – мрамор (карбонат кальция). Из него создавал свои прекрасные творения Микеланджело. Сульфат кальция встречается в природе в виде минерала гипса. Его используют для получения слепков. Для этого применяют полуводный гипс – алебастр.
Хирург: гипс используем и мы, медики, для наложения фиксирующих гипсовых повязок.
Хирург: гипс используем и мы, медики, для наложения фиксирующих гипсовых повязок.
Стоматолог: а сколько соединений кальция в составе любой зубной пасты! Из
Стоматолог: а сколько соединений кальция в составе любой зубной пасты! Из
Биолог: соединения кальция входят в состав скелетов и зубов позвоночных животных. Такие скелеты называются внутренними, и образованы они фосфатом кальция. На долю кальция приходится более 1,5% массы тела человека, 98% кальция содержится в костях.













 Химия в содружестве с другими науками
Химия в содружестве с другими науками Применение наноматериалов
Применение наноматериалов Химия - моя жизнь
Химия - моя жизнь Этиленгликоль. Физические свойства
Этиленгликоль. Физические свойства Қышқыл жаңбыр
Қышқыл жаңбыр Получение и свойства кислорода
Получение и свойства кислорода Презентация по Химии "Применение алюминия и его сплава" - скачать смотреть
Презентация по Химии "Применение алюминия и его сплава" - скачать смотреть  Полиэфирные волокна. Полиэстер
Полиэфирные волокна. Полиэстер Способы получения оксидов, оснований, кислот и солей. Урок №2
Способы получения оксидов, оснований, кислот и солей. Урок №2 Спирттер және фенолдар
Спирттер және фенолдар Thermal Energy, Chemical Energy
Thermal Energy, Chemical Energy Пластификаторы и пластификация полимеров
Пластификаторы и пластификация полимеров Химическая термодинамика
Химическая термодинамика EdExcel Unit C2 – Discovering Chemistry
EdExcel Unit C2 – Discovering Chemistry Никель қаптамаларын алу жолдары
Никель қаптамаларын алу жолдары Явище ізомерії. Структурна ізомерія. Близнюки органічного світу
Явище ізомерії. Структурна ізомерія. Близнюки органічного світу Влияние параметров технологического режима на удельную производительность и устойчивую работу реакторов
Влияние параметров технологического режима на удельную производительность и устойчивую работу реакторов Облучение. Радиационная окраска
Облучение. Радиационная окраска Тема Основание Гидроксид железа (II)
Тема Основание Гидроксид железа (II) Презентация Правила безопасности в кабинете химии
Презентация Правила безопасности в кабинете химии ДИТИНСТВО ТА ЖИТТЯ Д.І. МЕНДЕЛЄЄВА Підготував Учень 8-Б класу Воротинцев Артем
ДИТИНСТВО ТА ЖИТТЯ Д.І. МЕНДЕЛЄЄВА Підготував Учень 8-Б класу Воротинцев Артем  Химия s-элементов. Особенности свойств Mg и Be. Химия p-элементов. Общая характеристика элементов VIIA группы (галогены). Фтор
Химия s-элементов. Особенности свойств Mg и Be. Химия p-элементов. Общая характеристика элементов VIIA группы (галогены). Фтор Теория Бутлерова
Теория Бутлерова Количество вещества. Решение задач
Количество вещества. Решение задач Информационно-поисковый исследовательский проект: «Влияние пищевых добавок на здоровье человека».
Информационно-поисковый исследовательский проект: «Влияние пищевых добавок на здоровье человека».  Электронные конфигурации атомов
Электронные конфигурации атомов Альдегидтер және кетондар
Альдегидтер және кетондар Потенциометрия. Методы потенциометрии, и их применение в медицине. Плюсы и минусы методов ПТ
Потенциометрия. Методы потенциометрии, и их применение в медицине. Плюсы и минусы методов ПТ