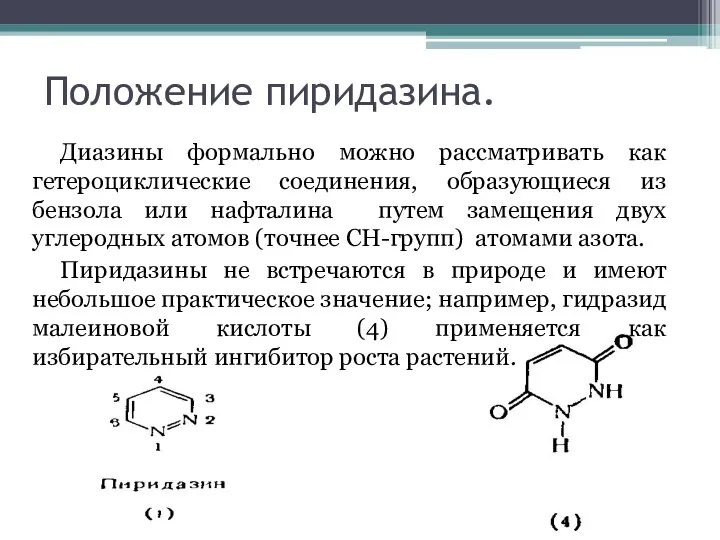
Химические свойства пиридазинов.
Пиридазин является более слабым основанием (pKB=2,33), чем пиридин (pKB=5,23), вследствие электроноакцепторного
влияния второго атома азота. Обычно протонируется только один атом азота молекулы пиридазина, второй атом азота может протонироваться только в концентрированных растворах кислот.
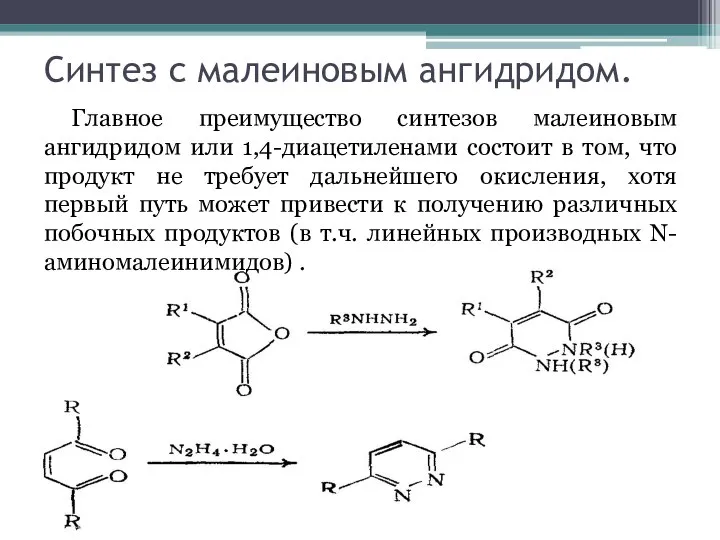
В реакции электрофильного замещения пиридазин вступает с большим трудом, в реакции нитрования, сульфирования, галогенирования и ацилирования практически не вступает. С алкилгалогенидами образует соответствующие N-соли.
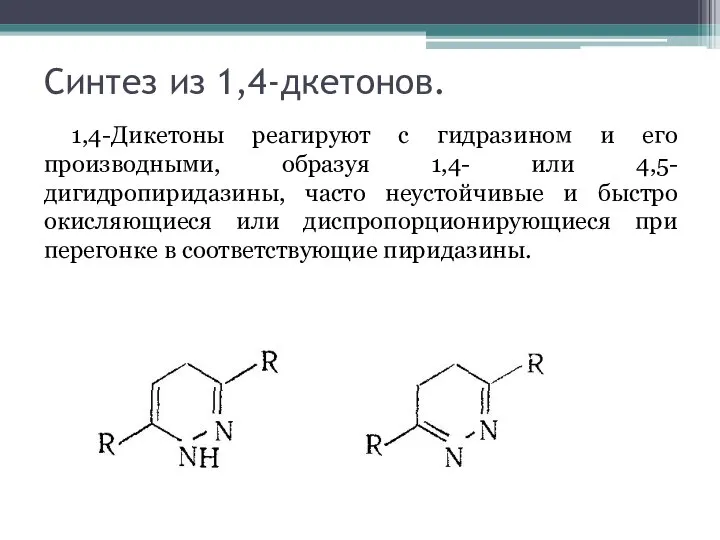
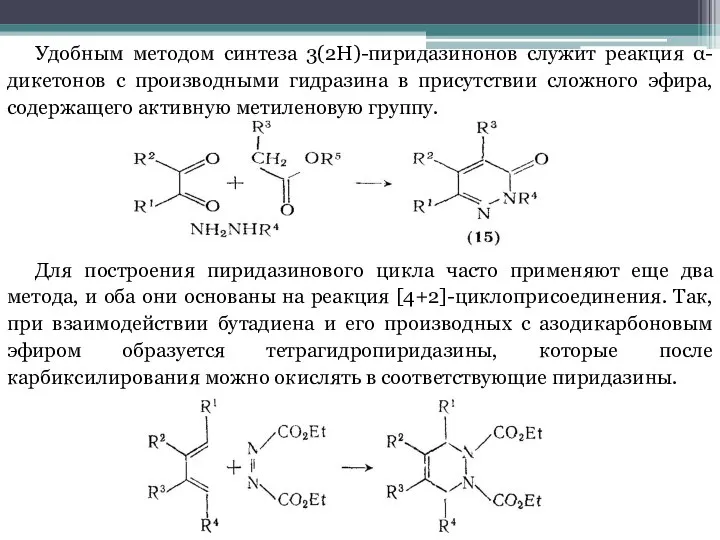
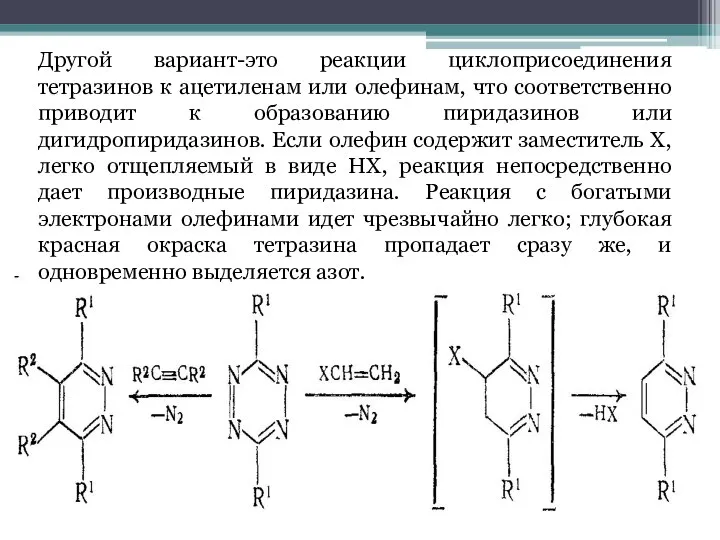
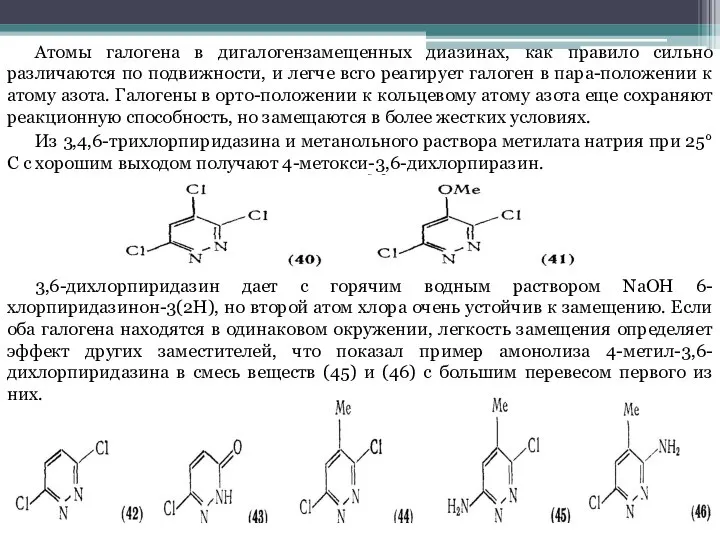
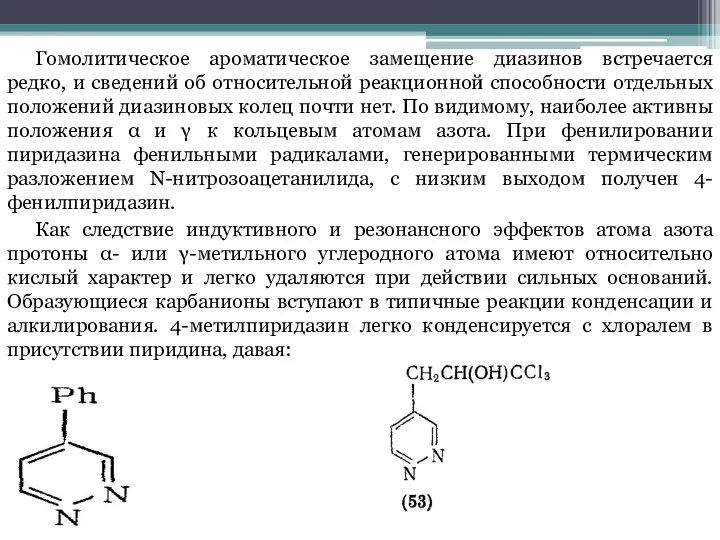
В большинстве случаев нуклеофильного замещения диазинов входящая группа вытесняет не водород, а какой-либо из заместителей кольца, чаще всего атом галогена. Это объясняется доступностью галогендиазинов из соответствующих оксодиазинов, которые с в свою очередь легко получить прямым синтезом. Реакционная способность атомов галогена, связанных с кольцом диазина, в значительной степени зависит от природы галогена, положения в кольце, о нуклеофила и вляния других заместителей.



 Нуклеофилы и электрофилы. Лекция 2
Нуклеофилы и электрофилы. Лекция 2 «Влияние талой воды на прорастание семян» Учащаяся 10 класса Гончарова Евгения Руководитель Григенча Т
«Влияние талой воды на прорастание семян» Учащаяся 10 класса Гончарова Евгения Руководитель Григенча Т Необычные минералы
Необычные минералы Атомно-емісійна спектрометрія з індуктивно-зв’язаною плазмою та рентгенофлуоресцентний аналіз
Атомно-емісійна спектрометрія з індуктивно-зв’язаною плазмою та рентгенофлуоресцентний аналіз Строение, свойства и многообразие функций белков
Строение, свойства и многообразие функций белков Apa în natură. Resursele de apă
Apa în natură. Resursele de apă Засоби побутової хімії – небезпечні джерела шкідливих для здоров’я людини речовин.
Засоби побутової хімії – небезпечні джерела шкідливих для здоров’я людини речовин.  Воздух, его состав и значение
Воздух, его состав и значение Содержание аскорбиновой кислоты в плодах шиповника, разных видов консервации
Содержание аскорбиновой кислоты в плодах шиповника, разных видов консервации Титан и его сплавы
Титан и его сплавы Полимеризация циклов. Сополимеризация
Полимеризация циклов. Сополимеризация Обмен простых белков. Дезаминирование и трансаминирование аминокислот
Обмен простых белков. Дезаминирование и трансаминирование аминокислот Изучение биохимических свойств микробов и их чувствительность к антибиотикам. Микробиологические исследования воды
Изучение биохимических свойств микробов и их чувствительность к антибиотикам. Микробиологические исследования воды Строение вещества
Строение вещества Składniki odżywcze
Składniki odżywcze Аллотропные модификации. Углерод
Аллотропные модификации. Углерод Презентация по Химии "Растворимость веществ в воде" - скачать смотреть
Презентация по Химии "Растворимость веществ в воде" - скачать смотреть  Растворы ВМС
Растворы ВМС Свойства химических элементов I и II А подгрупп периодической системы Д.И. Менделеева
Свойства химических элементов I и II А подгрупп периодической системы Д.И. Менделеева Основания, кислоты, соли в свете ТЭД
Основания, кислоты, соли в свете ТЭД КУБАНСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ КУБАНСКИЙ МЕДИЦИНСКИЙ ИНСТИТУТ КАФЕДРА ФУНДАМЕНТАЛЬНОЙ И КЛИНИЧЕСКОЙ БИОХИМ
КУБАНСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ КУБАНСКИЙ МЕДИЦИНСКИЙ ИНСТИТУТ КАФЕДРА ФУНДАМЕНТАЛЬНОЙ И КЛИНИЧЕСКОЙ БИОХИМ Классификация методов аналитической химии
Классификация методов аналитической химии Модифицированные природные полимеры. Их свойства
Модифицированные природные полимеры. Их свойства Кремний. Химические свойства
Кремний. Химические свойства Важнейшие классы бинарных соединений. Оксиды, гидриды и летучие водородные соединения
Важнейшие классы бинарных соединений. Оксиды, гидриды и летучие водородные соединения КАЛЬЦИЙ учитель: Дерюжина Алеся Владимировна Alesya2312@nextmail.ru МОУ «Гимназия №4» г.о. Электросталь, МО Ca 9 класс
КАЛЬЦИЙ учитель: Дерюжина Алеся Владимировна Alesya2312@nextmail.ru МОУ «Гимназия №4» г.о. Электросталь, МО Ca 9 класс  Количество вещества. Молярная масса. Задачи
Количество вещества. Молярная масса. Задачи Важнейшие химические понятия и законы
Важнейшие химические понятия и законы