Содержание
- 2. Я, Кузьмина Ирина Викторовна, кандидат технических наук с большим опытом преподавания в высшей школе и на
- 3. Вернуться к содержанию Для выхода из программы нажмите «Esc» на клавиатуре Переход к тому действию, о
- 4. Содержание Инструкция по использованию интерфейса Скорость химических реакций. Основные постулаты формальной химической кинетики. Зависимость скорости реакции
- 5. Скорость химических реакций Механизм и скорость реакций изучает химическая кинетика . Средняя скорость гомогенной химической реакции
- 6. При изучении химических реакций формальная химическая кинетика основывается на двух основных положениях-постулатах. Первый из них –
- 7. Физический смысл константы скорости реакции состоит в том, что она равна скорости химической реакции при концентрациях
- 8. Второй постулат химической кинетики – закон независимости протекания химических реакции. В случае сложной химической реакции все
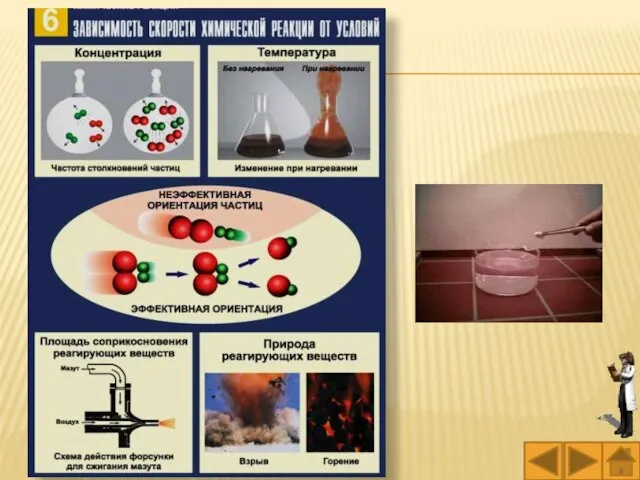
- 9. Зависимость скорости реакции от различных факторов Скорость реакции зависит от многих факторов. На нее влияют: природа
- 11. Влияние концентрации на скорость реакций Вааге Петер – норвежский физико-химик и минералог Гульдберг Като Максимилиан –
- 12. Закон действующих масс. Основным законом химической кинетики является открытый в 1864–1867 гг. Гульдбергом и Вааге (Норвегия)
- 13. Рассмотрим в общем виде одностадийную обратимую реакцию, протекающую в гомогенной среде А + В ⇔ АВ
- 14. Выражение зависимости скорости реакции от концентрации называют кинетическим уравнением. Как только образуются молекулы АВ, начнется обратная
- 15. Якоб Хендрик Вант-Гофф (в 1901 г. стал первым лауреатом Нобелевской премии по химии) Влияние температуры на
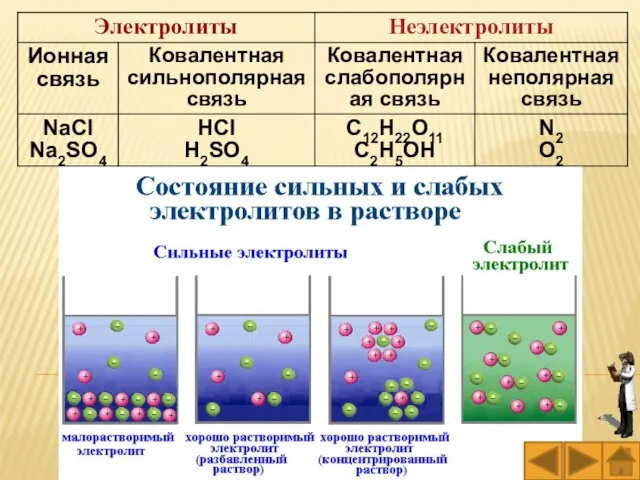
- 16. Влияние природы реагирующих веществ на скорость химических реакций Вещества с ионной и сильно полярной связью взаимодействуют
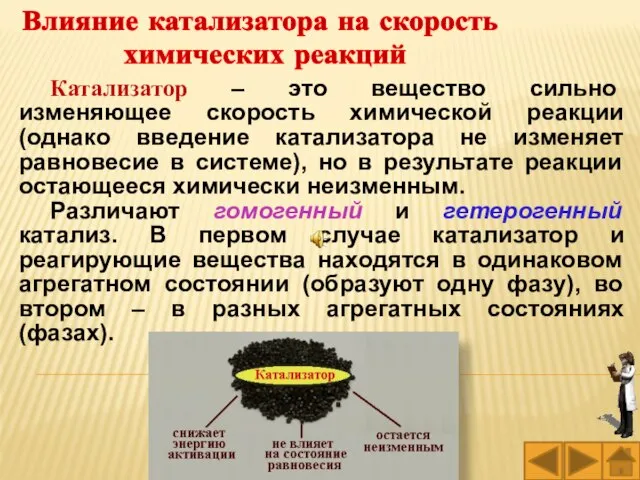
- 18. Катализатор – это вещество сильно изменяющее скорость химической реакции (однако введение катализатора не изменяет равновесие в
- 19. Пример гомогенного катализа Для объяснения каталитического действия при гомогенном катализе выдвинута гипотеза об образовании промежуточных продуктов
- 20. При гетерогенном катализе согласно адсорбционной теории катализа реагирующие вещества адсорбируются на поверхности катализатора, в результате чего
- 21. Установка для изучения кинетики инверсии сахарозы Приборы для демонстрации и изучения зависимости скорости химических реакций от
- 22. Прибор позволяет выявить влияние на скорость химической реакции следующих факторов: природы реагирующих веществ; концентрации; площади соприкосновения
- 23. Принцип работы прибора для демонстрации зависимости скорости химических реакций от различных условий Принцип работы прибора состоит
- 24. Прибор состоит из двух сосудов Ландольта (1), связанных с поворотным устройством (2), двух силиконовых трубок (3)
- 25. Проводим в одинаковых условиях реакции цинка с растворами серной кислоты различной концентрации. Скорость реакции определяем по
- 26. Проведем в одинаковых условиях реакции с цинком двух разных кислот: уксусной и серной. Газ интенсивнее выделяется
- 27. Проведем в одинаковых условиях две одинаковые реакции цинка с раствором серной кислоты. Отличаться реакции будут только
- 28. Пероксид водорода медленно разлагается на кислород и воду. По объему выделившегося кислорода можно судить о скорости
- 29. Определение скорости движения молекул и распределение Максвела-Больцмана С помощью данного прибора можно изучать: кинетическую теорию газов;
- 30. Химическое равновесие Большинство химических реакций обратимы, т. к. они протекают в прямом и обратном направлениях: Н2(газ)
- 31. В ходе процесса скорость прямой реакции уменьшается, а скорость обратной – увеличивается до тех пор, пока
- 32. Поскольку при равновесии скорости прямой и обратной реакции равны, ωпр= ωобр , то и k1×[H2]×[I2] =
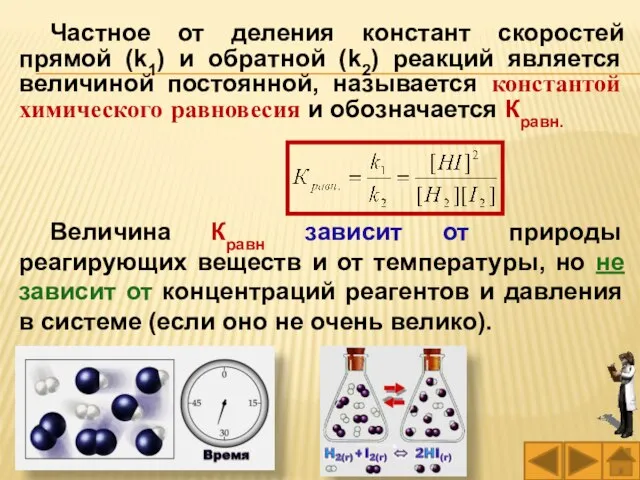
- 33. Частное от деления констант скоростей прямой (k1) и обратной (k2) реакций является величиной постоянной, называется константой
- 34. Смещение химического равновесия при изменении внешних условий Под смещением химического равновесия понимают такой процесс, который изменяет
- 35. При увеличении температуры равновесие смещается в сторону эндотермической реакции и, наоборот, при уменьшении температуры – в
- 36. При увеличении концентрации исходных веществ равновесие системы смещается вправо, в сторону образования конечных продуктов, а при
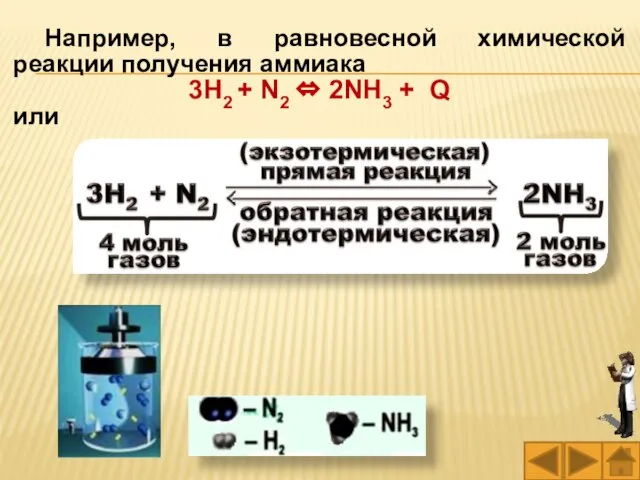
- 37. Например, в равновесной химической реакции получения аммиака 3Н2 + N2 ⇔ 2NH3 + Q или
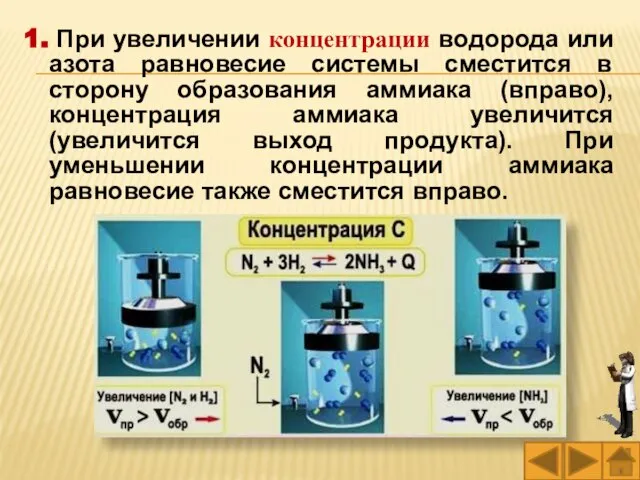
- 38. 1. При увеличении концентрации водорода или азота равновесие системы сместится в сторону образования аммиака (вправо), концентрация
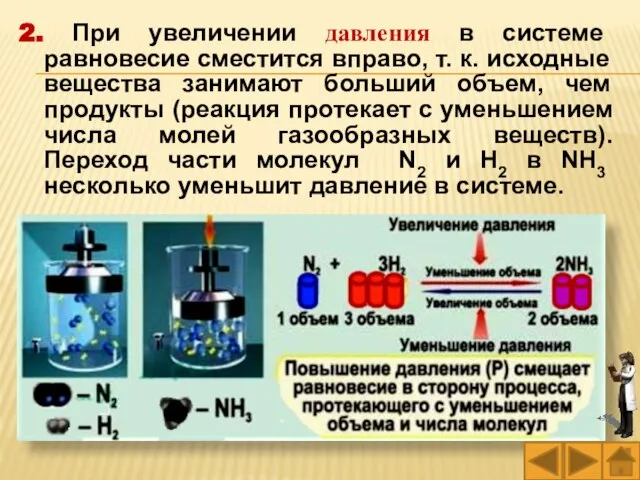
- 39. 2. При увеличении давления в системе равновесие сместится вправо, т. к. исходные вещества занимают больший объем,
- 40. 3. При увеличении температуры в этой же равновесной системе происходит смещение равновесия влево. Процесс разложения аммиака
- 41. Практическая (лабораторная) работа 6 «Изучение скорости взаимодействия металлов и их соединений с кислотами»
- 42. Цель – познакомиться с закономерностями взаимодействия металлов с кислотами. Приборы и реактивы: химическая посуда, цинк, алюминий,
- 43. Опыт 1. Взаимодействие металлов с кислотами. Налейте в две пробирки немого разбавленной серной кислоты H2SO4. В
- 44. 2Al0 + 3H+2SO4 → Al+32(SO4)3 + 3H02↑ серная сульфат кислота алюминия H2SO4 Al H2
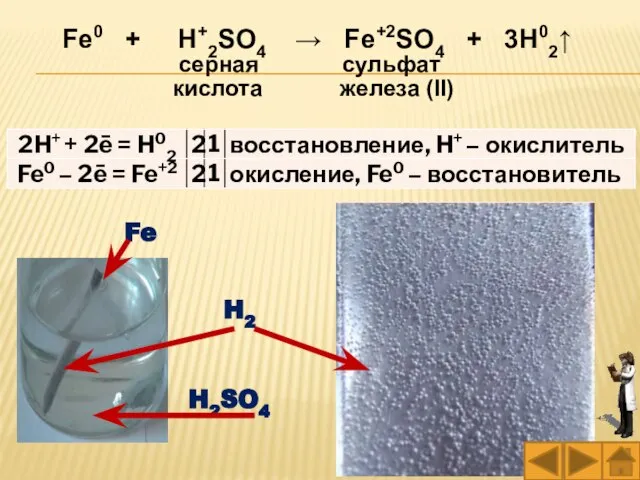
- 45. Fe0 + H+2SO4 → Fe+2SO4 + 3H02↑ серная сульфат кислота железа (II) Fe H2SO4 H2
- 46. Наблюдаемый эффект: выделился газ (при нагревании интенсивность выделения газа больше, чем при комнатной температуре). Признак реакции
- 47. а б в Взаимодействие металлов с кислотами: а – алюминий; б – цинк; в – никель
- 48. Задача 1. В процессе химической реакции 2NO(г)+ O2(г) = 2NO2(г) концентрация оксида азота (II) за 10
- 49. Скорость реакции, измеренную по NO можно определить следующим образом: В процессе этой реакции 0,2 моль NO
- 50. Задача 2. Во сколько раз изменится скорость прямой реакции А(г)+2В(г) ⇔ АВ2(г) при увеличении давления в
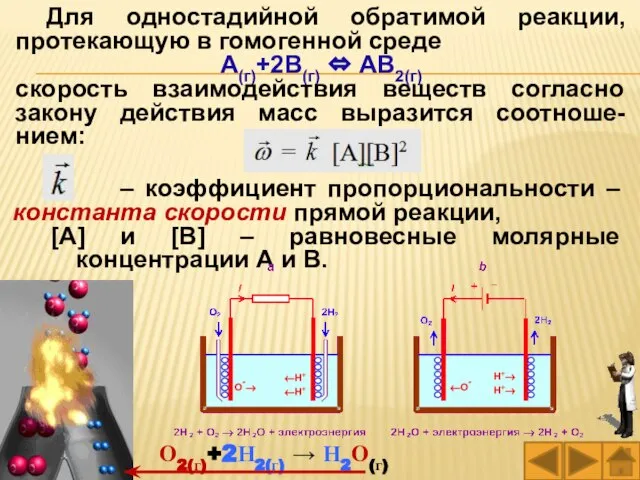
- 51. Для одностадийной обратимой реакции, протекающую в гомогенной среде А(г)+2В(г) ⇔ АВ2(г) скорость взаимодействия веществ согласно закону
- 53. Ответ: в замкнутой системе при постоянной температуре при увеличении давления в 2 раза скорости прямой реакции
- 54. Задача 3. Окисление серы и его диоксида протекают по уравнениям: а) S(к) + O2(г)= SO2(г); б)
- 55. Ответ: при уменьшении объема в 4 раза концентрация кислорода увеличивается в 4 раза.
- 56. б) 2SO2 (г) + O2 (г)= 2SO3(г) До сжатия реакционной системы скорость этой реакции: SO3
- 57. Ответ: при уменьшении объема в 4 раза концентрация кислорода увеличивается в 64 раза.
- 58. Задача 4. Вычислить во сколько раз уменьшится скорость реакции, протекающей в газовой фазе, если понизить температуру
- 59. Задача 5. Вычислить значение температурного коэффициента скорости реакции, если при повышении температуры на 30 оС скорость
- 60. Задача 6. Реакция при температуре 40 оС протекает за три минуты. Температурный коэффициент реакции равен трем.
- 61. Проверим, как Вы поняли и запомнили пройденный материал 1. Закон действующих масс: скорость элемен-тарной реакции… 1)
- 62. 2. Для реакции aА + bВ ⇔ cАВ скорость прямой реакции равна … 1) ωпр =
- 63. 4. Правило Вант-Гоффа: при повышении температуры на каждые 10о скорость реакции увеличивается в … 1) 1
- 64. 6. Катализатор – это вещество… 1) сильно изменяющее скорость химичес-кой реакции, 2) не изменяющее скорость химической
- 65. 7. В присутствии катализатора реакция проходит через следующие стадии: а) А + К = АК; б)
- 66. 9. Принцип Ле–Шателье: если на систему, находящуюся в равновесии, оказывается внешнее воздействие (изменяется …), … 1)
- 67. 1. Закон действующих масс: скорость элемен-тарной реакции… 1) пропорциональна произведению кон-центраций реагирующих веществ в степенях… 2)
- 68. 2. Для реакции aА + bВ ⇔ cАВ скорость прямой реакции равна … 1) ωпр =
- 69. 4. Правило Вант-Гоффа: при повышении температуры на каждые 10о скорость реакции увеличивается в … 1) 1
- 70. 6. Катализатор – это вещество… 1) сильно изменяющее скорость химичес-кой реакции, 2) не изменяющее скорость химической
- 71. 7. В присутствии катализатора реакция проходит через следующие стадии: а) А + К = АК; б)
- 72. 9. Принцип Ле–Шателье: если на систему, находящуюся в равновесии, оказывается внешнее воздействие (изменяется …), … 1)
- 73. Габриелян О. С., Остроумов И. Г. Химия для профессий и специальностей технического профиля: учебник для студ.
- 74. Новошннский И. И., Новошинская Н. С. Химия: учебник для 8 класса общеобразовательных учреждений/И. И. Новошинский, Н.
- 75. http://interneturok.ru/chemistry/9-klass/bhimicheskaya-svyaz-elektroliticheskaya-dissociaciyab/skorost-himicheskih-reaktsiy-osnovnoy-urok http://s-konda.ru/exam/chemistry_9-30.htm https://www.google.ru/search?q=скорость+химических+реакций https://ru.wikipedia.org/wiki/Химическое_равновесие http://www.hemi.nsu.ru/ucheb217.htm http://files.school-collection.edu.ru/dlrstore/bd0d808e-db78-f3d2-e3b2-5388709d7222/1011619A.htm http://alhimikov.net/reaktion/Page-1.html http://orgchem.ru/chem1/P6_14.htm http://prosto-o-slognom.ru/chimia/20_chim_ravnovesie.html https://www.google.ru/search?q=химическое+равновесие Использованные источники
- 77. Скачать презентацию
































































 Классификация методов аналитической химии
Классификация методов аналитической химии Обмен нуклеопротеинов
Обмен нуклеопротеинов Нуклеин қышқылдары. ДНҚ репликациясы
Нуклеин қышқылдары. ДНҚ репликациясы Некрохмалисті полісахариди
Некрохмалисті полісахариди Физический этап развития периодического закона
Физический этап развития периодического закона Хімічні явища в побуті
Хімічні явища в побуті Көмірсу. Көмірсулардың қасиеттері. Көмірсудың метаболизмі
Көмірсу. Көмірсулардың қасиеттері. Көмірсудың метаболизмі Основы теории плавления и отвердевания металлов
Основы теории плавления и отвердевания металлов Экологический проект Тема: Лабораторное исследование химического состава чипсов Работу выполнила Купавцева Татьяна
Экологический проект Тема: Лабораторное исследование химического состава чипсов Работу выполнила Купавцева Татьяна  Строение атома
Строение атома Непредельные углеводороды
Непредельные углеводороды Строение атома и периодическая система элементов Д. И. Менделеева
Строение атома и периодическая система элементов Д. И. Менделеева Органические и неорганические полимеры
Органические и неорганические полимеры Классификация химических реакций
Классификация химических реакций Определение активной реакции воды (рН)
Определение активной реакции воды (рН)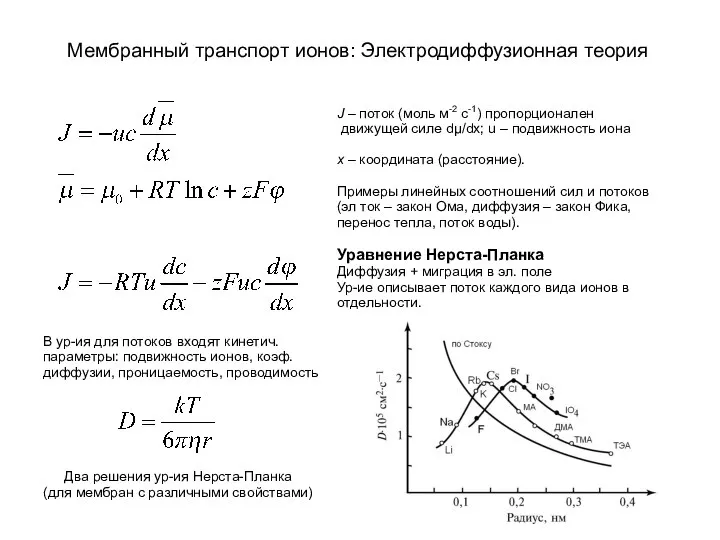 Мембранный транспорт ионов: электродиффузионная теория
Мембранный транспорт ионов: электродиффузионная теория Нефть. Состав. Свойства. Переработка
Нефть. Состав. Свойства. Переработка КЛАССИФИКАЦИЯ ХИМИЧЕСКИХ РЕАКЦИЙ
КЛАССИФИКАЦИЯ ХИМИЧЕСКИХ РЕАКЦИЙ Аттестационная работа. Программа элективного курса по химии «экологическая химия»
Аттестационная работа. Программа элективного курса по химии «экологическая химия» Спиртзавод ОАО «Петровский»
Спиртзавод ОАО «Петровский» Гидролиз солей.
Гидролиз солей.  Прогнозування хімічної обстановки під час застосування хімічної зброї
Прогнозування хімічної обстановки під час застосування хімічної зброї Fiber-Sludge-Sulfur-Beton (FiSHSB)
Fiber-Sludge-Sulfur-Beton (FiSHSB) Сероводород
Сероводород Композиционные или композитные материалы
Композиционные или композитные материалы Углеводороды и их природные источники. Гомологический ряд алканов. Строение алканов
Углеводороды и их природные источники. Гомологический ряд алканов. Строение алканов Хімія та їжа
Хімія та їжа Одорант природный
Одорант природный