Содержание
- 2. ОТВЕТЫ: 1 ВАРИАНТ 1. Cu2O + C = 2Cu + CO Cu2O + CO = 2Cu
- 3. Соединения металлов. Оксиды и гидроксиды.
- 4. Металлы I и II групп ПСХЭ III группы ПСХЭ 1 – 2 ē 3 ē Оксиды
- 5. Различные соединения хрома CrO – основной оксид Cr2O3 – амфотерный оксид CrO3 – кислотный оксид +2
- 6. Соединения металлов и их свойства Основные оксиды Образованы металлами со с.о. +1, +2 Na2O, CaO, MgO,
- 7. Соединения металлов и их свойства Амфотерные оксиды Образованы металлами со с.о. +2, +3 Al2O3, ZnO, BeO,
- 8. Соединения металлов и их свойства Кислотные оксиды Образованы металлами побочных подгрупп с высшими с.о. (больше +3)
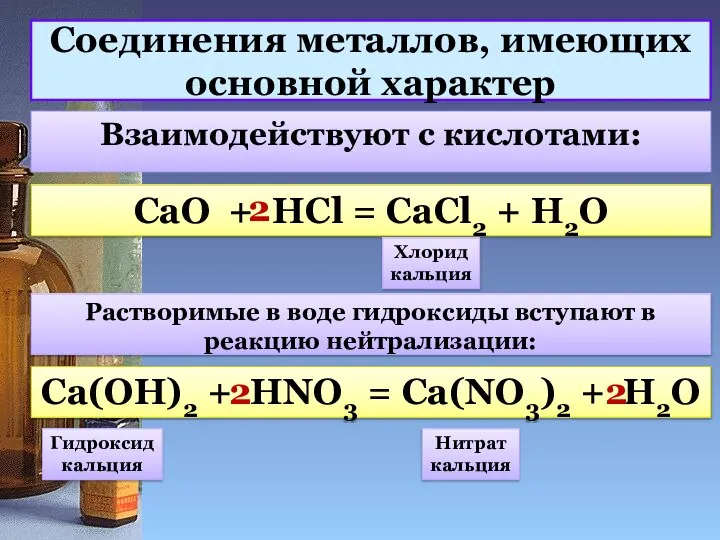
- 9. Соединения металлов, имеющих основной характер Взаимодействуют с кислотами: CaO + HCl = CaCl2 + H2O 2
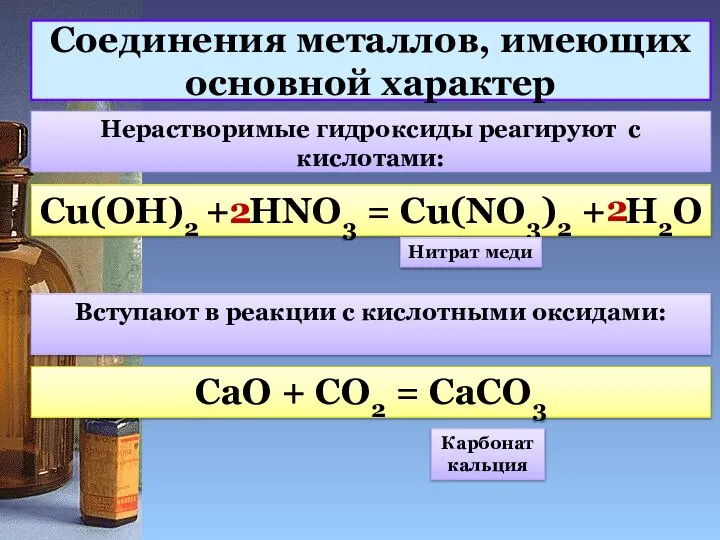
- 10. Соединения металлов, имеющих основной характер Нерастворимые гидроксиды реагируют с кислотами: Cu(OH)2 + HNO3 = Cu(NO3)2 +
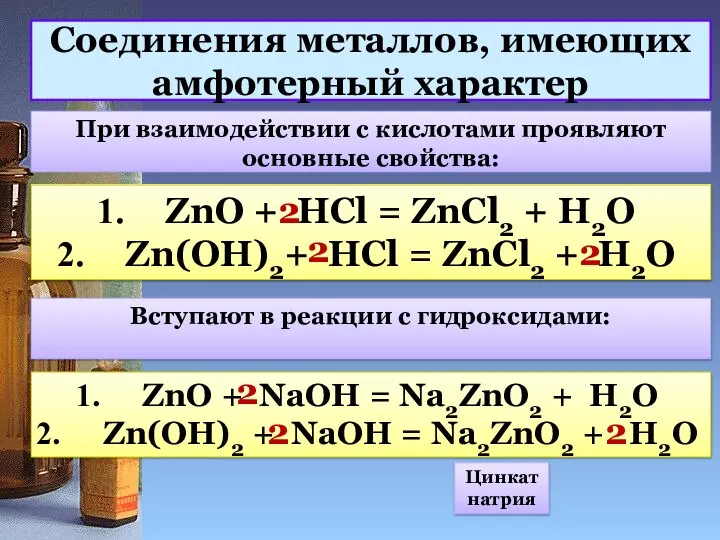
- 11. Соединения металлов, имеющих амфотерный характер При взаимодействии с кислотами проявляют основные свойства: ZnO + HCl =
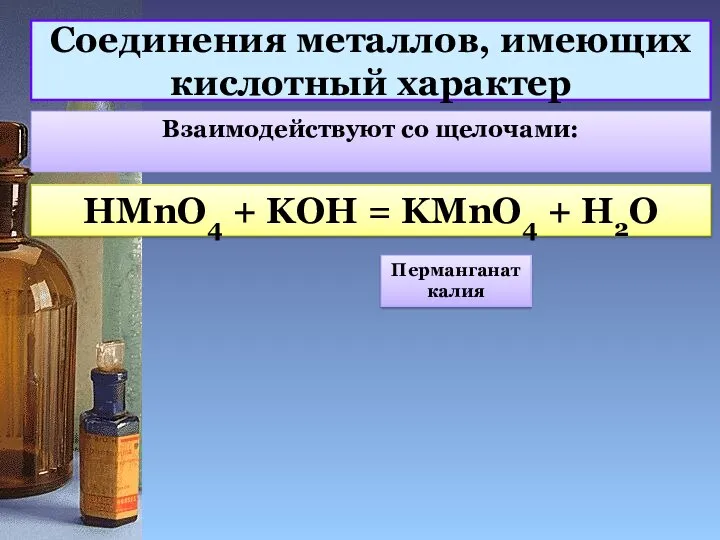
- 12. Соединения металлов, имеющих кислотный характер Взаимодействуют со щелочами: HMnO4 + KOH = KMnO4 + H2O Перманганат
- 14. Скачать презентацию







 Інгібіювання та регуляція ензимів
Інгібіювання та регуляція ензимів Температурная зависимость времени спин-решеточной релаксации протонов в H2La2Ti3O10
Температурная зависимость времени спин-решеточной релаксации протонов в H2La2Ti3O10 Презентация по Химии "Презентация Коррозия металлов" - скачать смотреть
Презентация по Химии "Презентация Коррозия металлов" - скачать смотреть  Аттестационная работа. Разработка урока химии в 9 классе Исследовательская деятельность при решении экспериментальных задач
Аттестационная работа. Разработка урока химии в 9 классе Исследовательская деятельность при решении экспериментальных задач Полимерлену. Полимерлердің түзілу әдістері
Полимерлену. Полимерлердің түзілу әдістері Химические свойства воды (домашнее задание)
Химические свойства воды (домашнее задание) Химическая спартакиада
Химическая спартакиада Теория Электролитической Диссоциации
Теория Электролитической Диссоциации Electron configuration and periodicity
Electron configuration and periodicity Аттестационная работа. Групповой урочный проект Кислородсодержащие органические вещества
Аттестационная работа. Групповой урочный проект Кислородсодержащие органические вещества Правила работы и основные методы исследований в химической лаборатории
Правила работы и основные методы исследований в химической лаборатории Хроматографические методы в радиохимии
Хроматографические методы в радиохимии Водород, нахождение в природе. Получение водорода и его физические свойства
Водород, нахождение в природе. Получение водорода и его физические свойства Химическая термодинамика
Химическая термодинамика Альдегиды
Альдегиды Химия - моя жизнь
Химия - моя жизнь Реакции ионного обмена
Реакции ионного обмена Учитель высшей категории ГОУ СОШ №26 с углубленным изучением французского языка г. Санкт-Петербурга Литвиненко Галина Андреевна
Учитель высшей категории ГОУ СОШ №26 с углубленным изучением французского языка г. Санкт-Петербурга Литвиненко Галина Андреевна КОЛЕКЦІЯ ВОЛОКОН
КОЛЕКЦІЯ ВОЛОКОН  ХИМИЧЕСКИЕ СВОЙСТВА АЛКАНОВ Презентацию составила учитель МОУ «Ягринская гимназия» г.Северодвинска Шапошникова Т.С.
ХИМИЧЕСКИЕ СВОЙСТВА АЛКАНОВ Презентацию составила учитель МОУ «Ягринская гимназия» г.Северодвинска Шапошникова Т.С.  Задачи на смеси (задание № 33)
Задачи на смеси (задание № 33) Цемент. (9 класс)
Цемент. (9 класс) 10 смыслов картины Черный квадрат
10 смыслов картины Черный квадрат  Классификация неорганических веществ. Оксиды. Автор: Калитина Тамара Михайловна Место работы: МОУ СОШ №3 с.Александров-Гай
Классификация неорганических веществ. Оксиды. Автор: Калитина Тамара Михайловна Место работы: МОУ СОШ №3 с.Александров-Гай  Физические и химические явления. Химические реакции
Физические и химические явления. Химические реакции Нептуний
Нептуний Цепные химические реакции
Цепные химические реакции Семинар на тему Природные источники углеводородов и их переработка
Семинар на тему Природные источники углеводородов и их переработка