Содержание
- 2. Охарактеризуйте Fe как химический элемент, составив предложения со словами и словосочетаниями: Порядковый номер, номер периода ,
- 3. Проверьте ошибки и коэффициенты Fe + S→ Fe S 3Fe + 2O2 → Fe3O4 2Fe +3СI₂
- 4. Проверьте ошибки и коэффициенты Fe + 2HCI → FeCI₂ + H₂ Fe + H₂SO₄ → FeSO₄
- 5. СЕГОДНЯ НА УРОКЕ: 1. Оксиды и гидроксиды железа +2 и +3, их характер 2. Получение гидроксидов
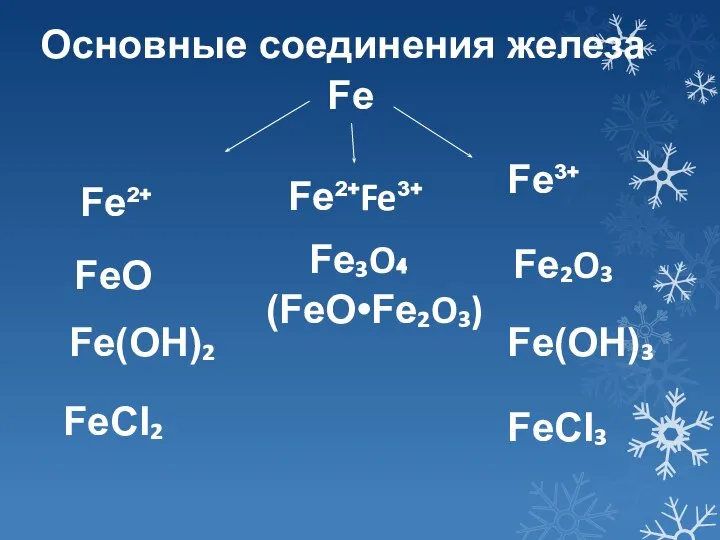
- 6. Fe Fe²⁺ Fe³⁺ FeO Fe(OH)₂ FeCI₂ Fe₂O₃ Fe(OH)₃ FeCI₃ Основные соединения железа Fe²⁺Fe³⁺ Fe₃O₄ (FeO•Fe₂O₃)
- 7. Экспериментальная Соблюдайте ПТБ!
- 8. Получение гидроксидов железа FeCI₂ + 2NaOH = Fe(OH)₂↓ +2NaCI FeCI₃ + 3NaOH = Fe(OH)₃↓ + 3NaCI
- 9. Качественные реакции на ионы Fe²⁺ и Fe³⁺ Fe³⁺ реактив – роданид калия KSCN Fe³⁺ реактив –
- 10. Нахождение в природе В свободном виде в метеоритах В живых организмах
- 11. Биологическая Железо входит в состав гемоглобина, миоглобина, различных ферментов и других сложных железо -белковых комплексов, которые
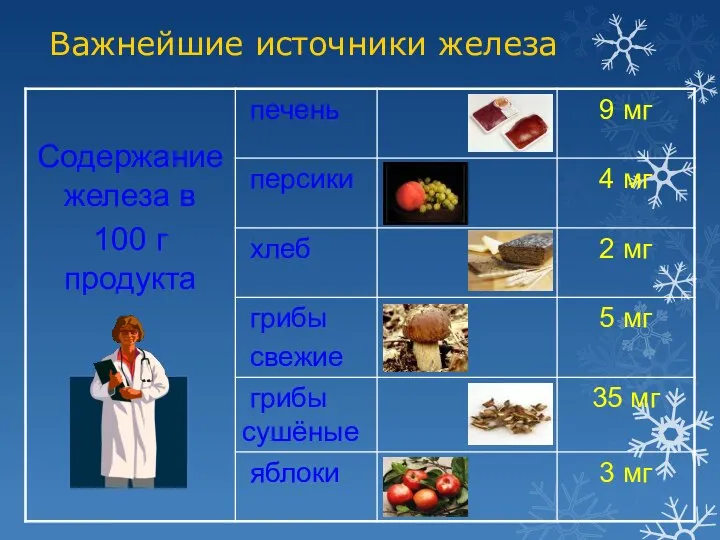
- 12. Важнейшие источники железа
- 13. Токсичность железа Избыточная доза железа – 200мг и выше может вызвать отравление Железо занимает 5 –е
- 14. Генетические связи Fe ПРОЙДИТЕ, СОСТАВИВ СООТВЕТСТВУЮЩУЮ СХЕМУ РЕАКЦИЙ, ОТ ОДНОГО УКАЗАННОГО В ЗАДАНИИ ВЕЩЕСТВА К ДРУГОМУ:
- 15. СЕГОДНЯ Я УЗНАЛ… Я УДИВИЛСЯ… ТЕПЕРЬ Я УМЕЮ… Я ХОТЕЛ БЫ…
- 16. Домашнее задание § 14, упражнение 4 стр. 82 Задача 6 стр. 83 (по желанию)
- 18. Скачать презентацию













 Открытие кремния
Открытие кремния История мыловарения. Мыло своими руками
История мыловарения. Мыло своими руками Вода – основа жизни на Земле
Вода – основа жизни на Земле Классификация полимеров
Классификация полимеров Генетическая связь неорганических соединений. 8 класс
Генетическая связь неорганических соединений. 8 класс Происхождение нефти
Происхождение нефти Хімія у створенні нових матеріалів та побуті
Хімія у створенні нових матеріалів та побуті Гигиенические нормативы. Химические факторы окружающей среды
Гигиенические нормативы. Химические факторы окружающей среды Кислоты и их свойства
Кислоты и их свойства Отдаленные последствия токсического воздействия. Гигиена труда в с/х при работе с ядохимикатами
Отдаленные последствия токсического воздействия. Гигиена труда в с/х при работе с ядохимикатами Пластмассы
Пластмассы 6 классов ферментов и тривиальные названия некоторых основных групп
6 классов ферментов и тривиальные названия некоторых основных групп Петрография некоторых распространенных метаморфических пород
Петрография некоторых распространенных метаморфических пород Презентация Дисахариды
Презентация Дисахариды Викторина «Своя игра» в рамках декады по биологии, географии и химии
Викторина «Своя игра» в рамках декады по биологии, географии и химии  Периодическая система элементов Д.И. Менделеева
Периодическая система элементов Д.И. Менделеева Криптонит для растений
Криптонит для растений Физико-химия дисперсных систем
Физико-химия дисперсных систем Алюминий и его сплавы
Алюминий и его сплавы Буферные системы. Классификация буферных растворов
Буферные системы. Классификация буферных растворов Хлор
Хлор Спирты и фенолы
Спирты и фенолы Серебро. Химические свойства
Серебро. Химические свойства Классификация органических веществ. Автор: Русакова А.В. учитель химии МОУ «Гимназия № 19» г. Омска.
Классификация органических веществ. Автор: Русакова А.В. учитель химии МОУ «Гимназия № 19» г. Омска.  Аттестационная работа. Образовательная программа внеурочной деятельности «Химия и физика с детства». (1-4 класс)
Аттестационная работа. Образовательная программа внеурочной деятельности «Химия и физика с детства». (1-4 класс) Степень окисления веществ. Задачи
Степень окисления веществ. Задачи Люминесцентный анализ
Люминесцентный анализ Органічна хімія
Органічна хімія