Содержание
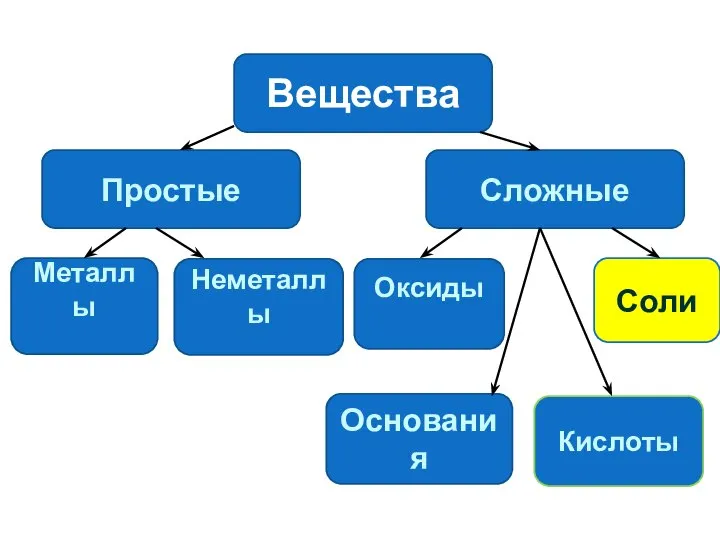
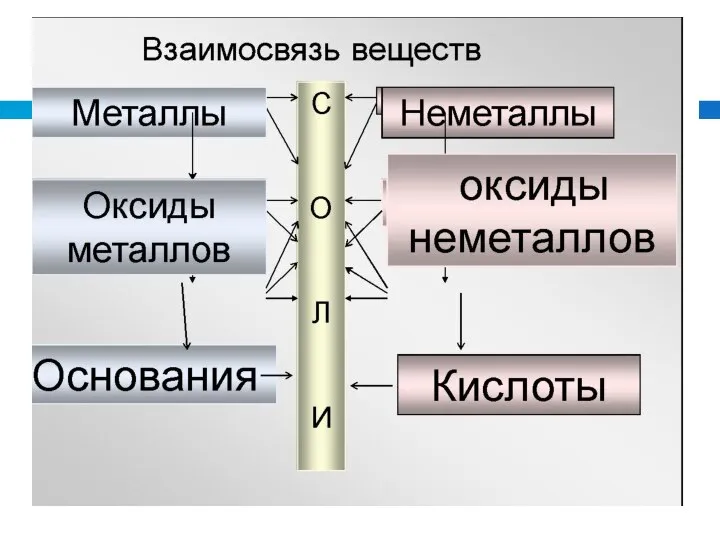
- 2. Вещества Простые Сложные Металлы Неметаллы Оксиды Основания Соли Кислоты
- 3. NO HNO NaOH HNO 2 3 К какому классу соединений относятся вещества, дать им названия
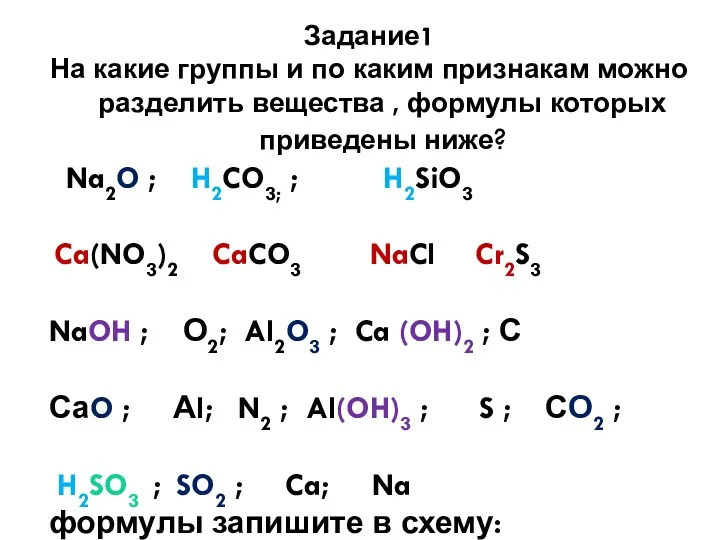
- 4. Задание1 На какие группы и по каким признакам можно разделить вещества , формулы которых приведены ниже?
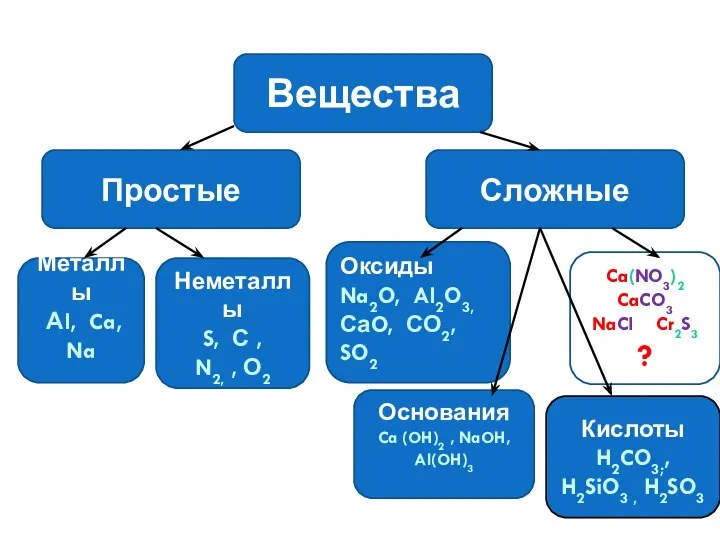
- 5. Вещества Простые Сложные Металлы Аl, Ca, Na Неметаллы S, С , N2, , О2 Оксиды Na2O,
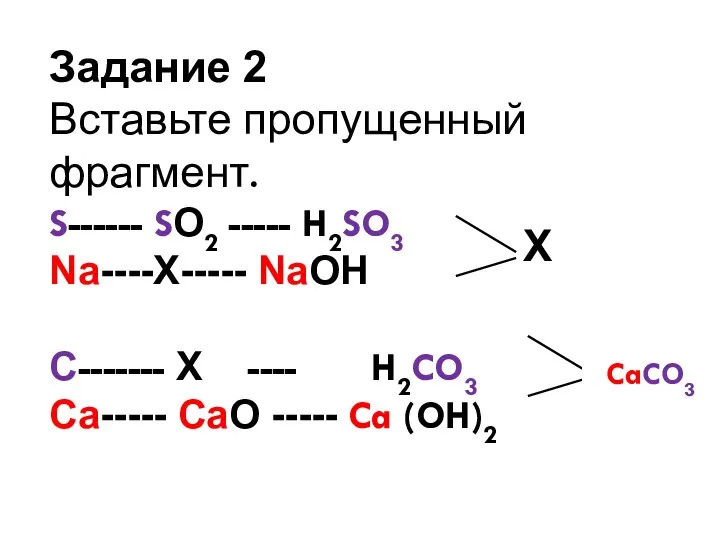
- 6. Задание 2 Вставьте пропущенный фрагмент. S------ SО2 ----- H2SO3 Na----Х----- NaОН С------- Х ---- H2CO3 Ca-----
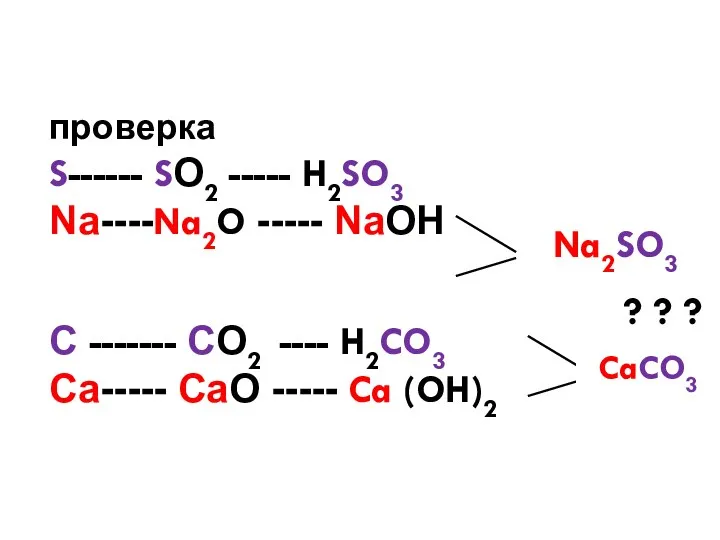
- 7. проверка S------ SО2 ----- H2SO3 Na----Na2O ----- NaОН ? ? ? С ------- СО2 ---- H2CO3
- 9. СОЛИ , как производные кислот и оснований. Их состав и номенклатура (название).
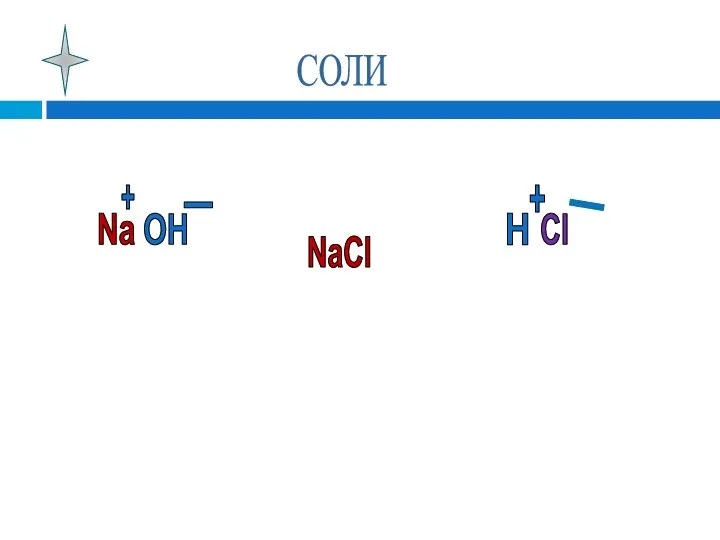
- 10. СОЛИ Na OH H Cl NaCl + - + _
- 11. Соли - это сложные вещества, которые состоят из ионов металла и кислотного остатка.
- 12. Задание. Определить : почему у солей разное количество кислотных остатков Дайте обоснованный ответ. NaNO3 Ca (NO3
- 13. 3адание. Na+1 Ca+2 Al+3 Имеют разную степень окисления. (см. таблицу растворимости)
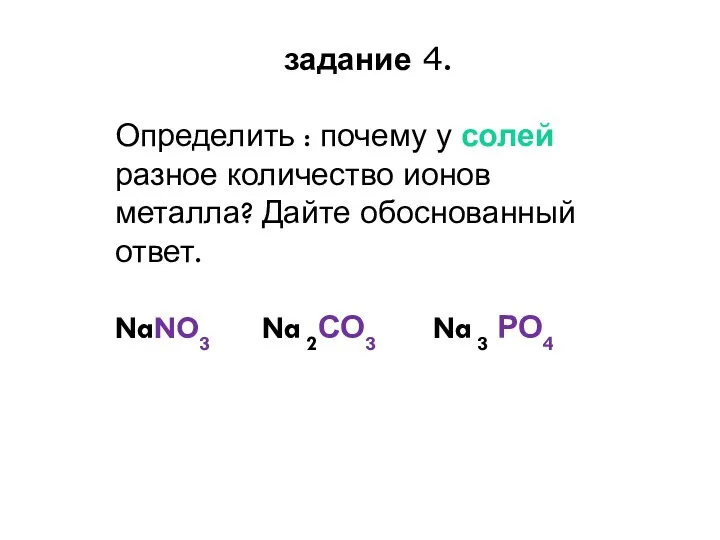
- 14. задание 4. Определить : почему у солей разное количество ионов металла? Дайте обоснованный ответ. NaNO3 Na
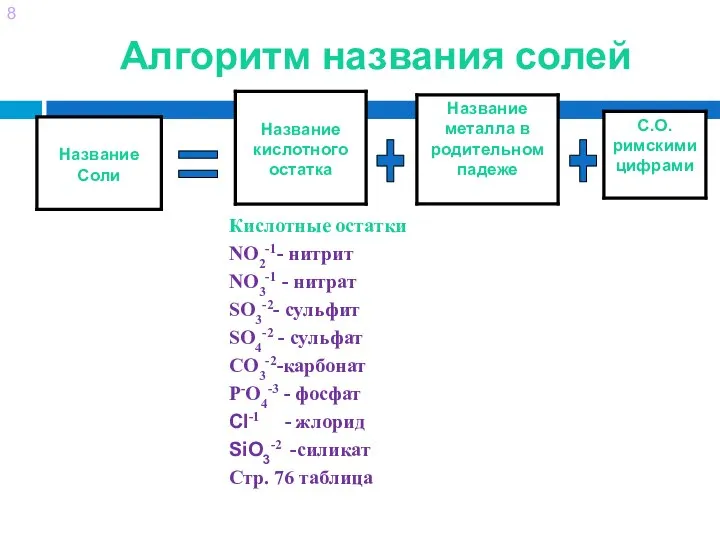
- 15. Так как кислотные остатки имеют свою степень окисления: (см. таблицу растворимости) NO2-1- нитрит NO3-1 – нитрат
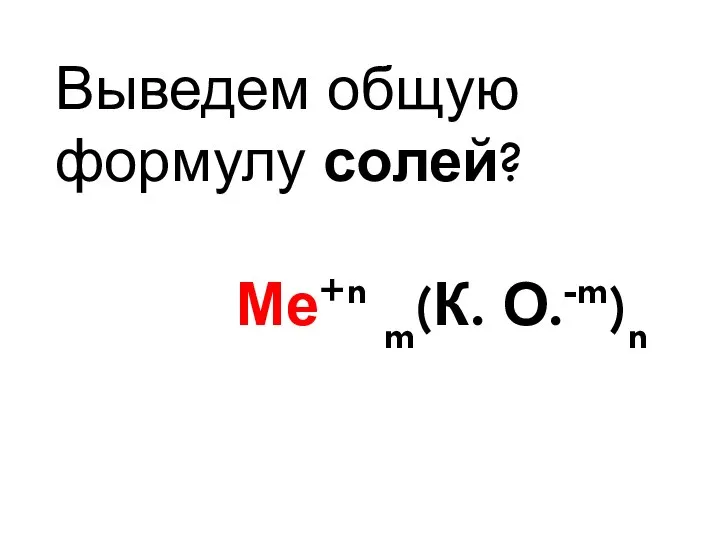
- 16. Выведем общую формулу солей? Ме+n m(К. О.-m)n
- 17. Алгоритм названия солей + + =
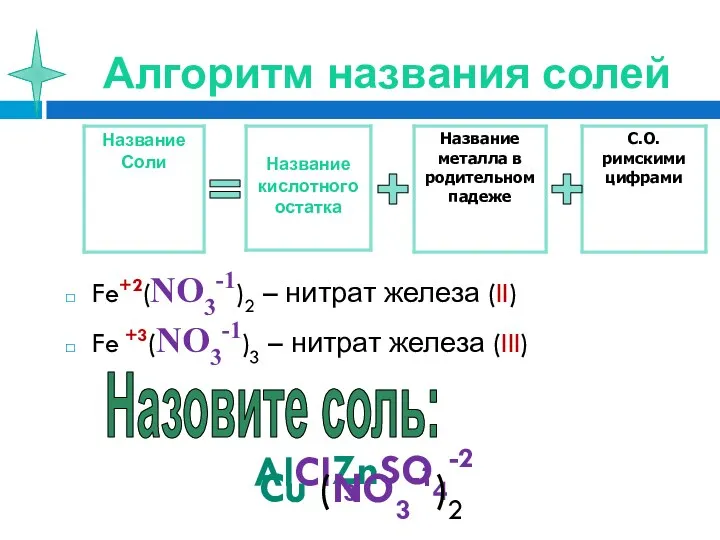
- 18. Алгоритм названия солей Fe+2(NO3-1)2 – нитрат железа (II) Fe +3(NO3-1)3 – нитрат железа (III) = +
- 19. задание 5. НАЗОВИТЕ СОЛИ NaCl Fe +2SO4 Al3(PO4)3 Ca(NO3)2 Cu+2CO3 Cr2+3S3 Na2SO4 Ba(NO3 )2
- 20. задание 5. НАЗОВИТЕ СОЛИ NaCl - хлорид натрия Fe +2SO4 - сульфат железа (II) Al3(PO4)3 –
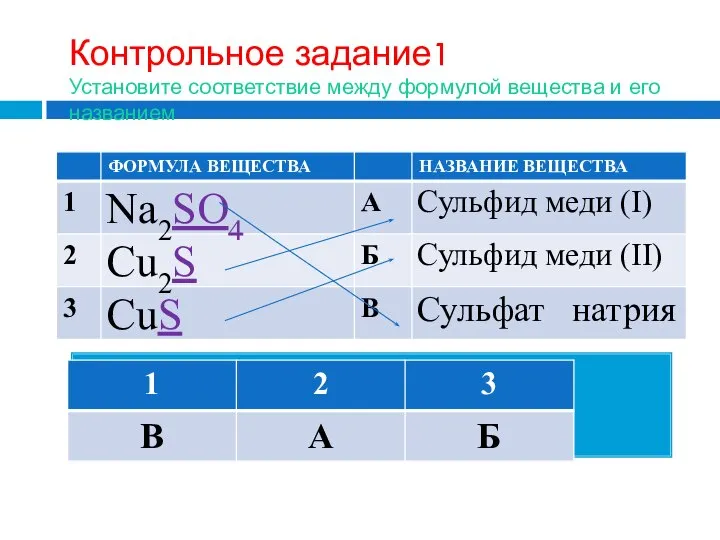
- 21. Контрольное задание1 Установите соответствие между формулой вещества и его названием
- 22. 2. Составление формул солей по их названиям.
- 23. 1. Запиши рядом знаки химических элементов, которые входят в состав вещества. Алгоритм составления формул солей: Составить
- 24. 2. Над знаками химических элементов поставь их степень окисления. Пример: Fe SO4 +3 -2 Второй пункт
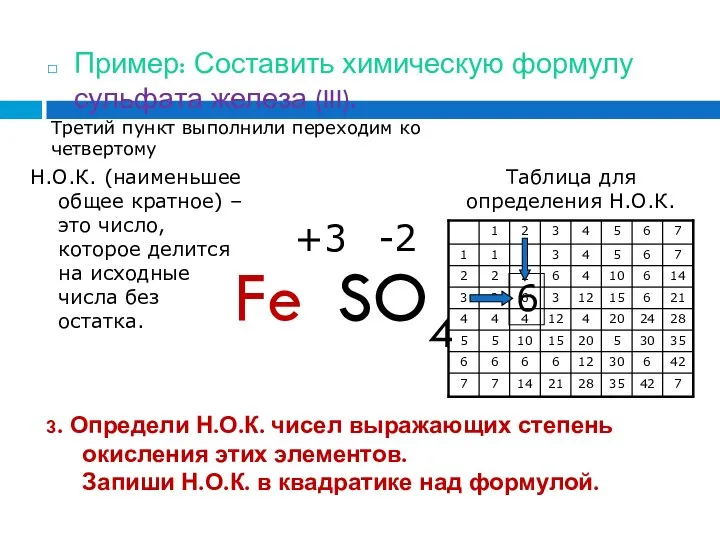
- 25. 3. Определи Н.О.К. чисел выражающих степень окисления этих элементов. Запиши Н.О.К. в квадратике над формулой. Пример:
- 26. 4. Раздели Н.О.К. на степень окисления каждого элемента. Запиши полученный индекс. Пример: Составить химическую формулу сульфата
- 27. Составить формулу сульфата алюминия: (второй способ) Составить формулы: нитрат железа (III), сульфат натрия, карбонат меди (II),
- 28. Составьте формулу хлорида кальция СаCl2 Составьте формулу нитрата натрия NaNO3 Zn(SO4)2 Cu NO3 Составьте формулу сульфата
- 29. 3. Отдельные Представители стр.77 в таблицу хлорид натрия
- 30. NaCl
- 31. "Среди всех природных минеральных солей, самая главная та, которую мы называем просто “соль” А.Е.Ферсман
- 32. За 4 года человек съедает пуд соли (в год человек с пищей потребляет 3-5,5 кг соли)
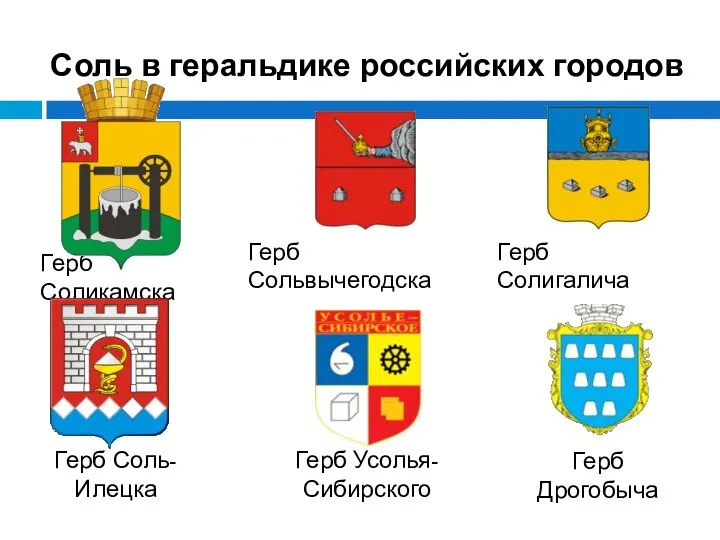
- 33. Соль в геральдике российских городов Герб Соликамска Герб Солигалича Герб Сольвычегодска Герб Соль-Илецка Герб Усолья-Сибирского Герб
- 34. Добыча соли из соляных шахт из соленых озер
- 35. На озере Баскунчак ежегодно добывается около 5 млн. тонн соли
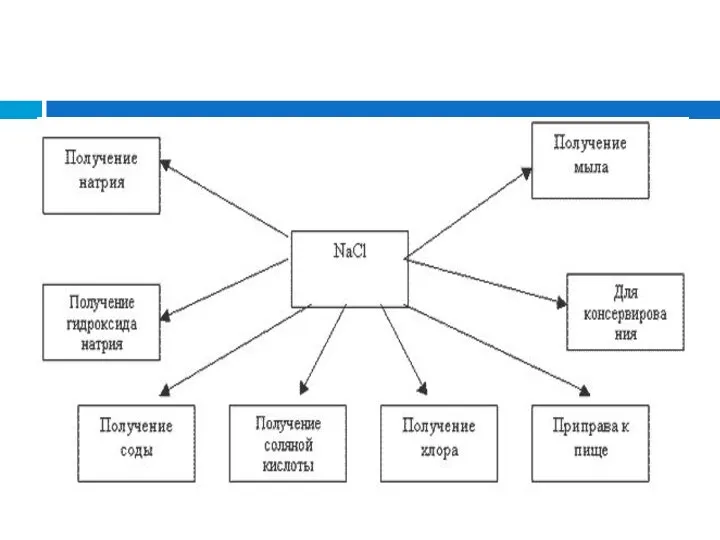
- 36. Применение NaCl
- 37. Д/З: CaCO3
- 38. Моллюски, раки, радиолярии, кораллы – все имеют известковый скелет
- 39. Большой Барьерный риф в Австралии
- 40. Меловые горы
- 41. Минералы карбоната кальция находятся в горных породах: Известняк Мел Мрамор Мрамор Мрамор Мрамор Травертин
- 42. Мрамор – строительный материал Единственное в России здание, полностью построенное из нешлифованного мрамора — железнодорожный вокзал
- 43. Д/З: Фосфат кальция - основа минералов фосфоритов и апатитов
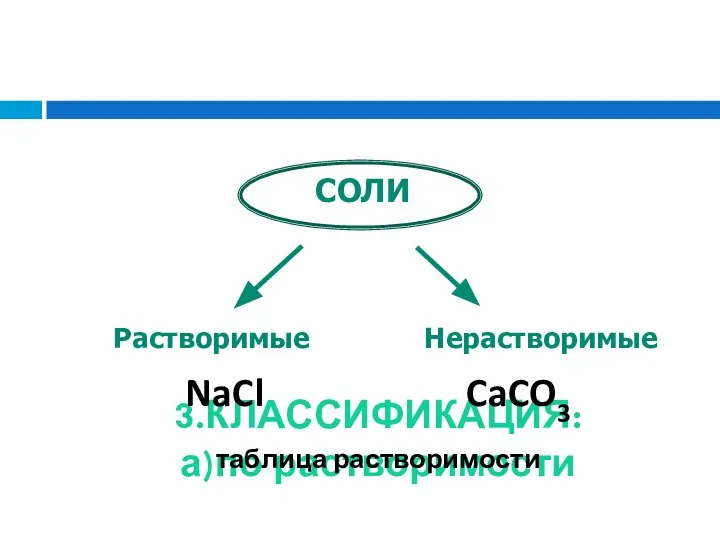
- 44. 3.КЛАССИФИКАЦИЯ: а)по растворимости
- 45. 3.КЛАССИФИКАЦИЯ: а)по растворимости NaCl CaCO3 таблица растворимости
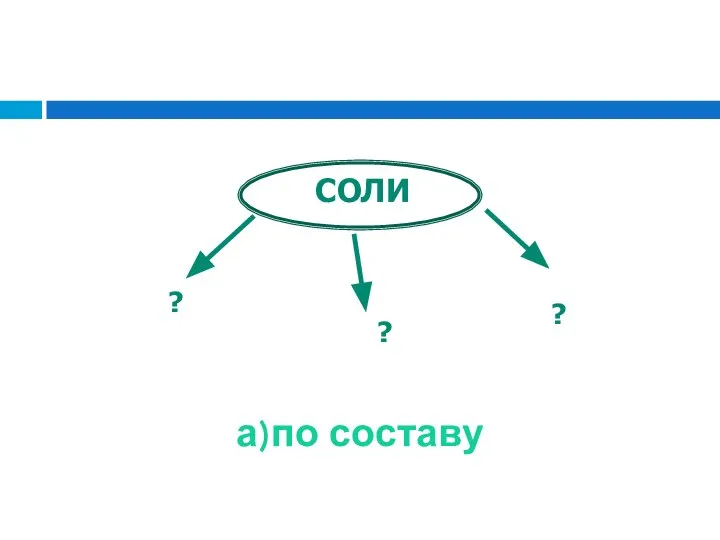
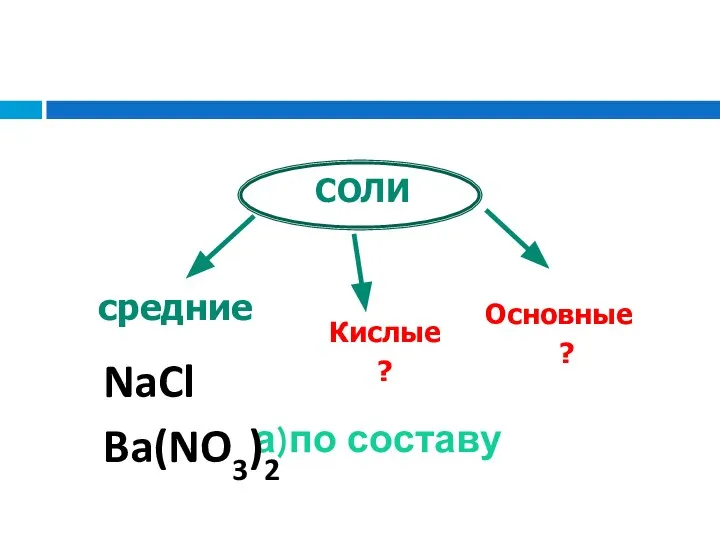
- 46. а)по составу
- 47. а)по составу NaCl Ba(NO3)2
- 48. Контрольное задание - итоговое Часть А (задания с выбором ответа) 1. Соли – это сложные вещества:
- 49. Контрольное задание - итоговое Часть В Выбери лишнее вещество и объясни почему? Игра « Третий лишний»
- 50. Контрольное задание - итоговое Часть А Г А Часть В объясни почему? 1. NaCl. т.к… 2.
- 52. Скачать презентацию






























 Бутлеровтың құрылыс теориясы
Бутлеровтың құрылыс теориясы Спирты. Тема 5
Спирты. Тема 5 Анализ карбоновых кислот и их производных
Анализ карбоновых кислот и их производных Оценка опасности взрыва горючих газов
Оценка опасности взрыва горючих газов Кислоты, их состав и название. Цель урока: 1. Сформировать понятия о кислотах. 2. Рассмотреть состав, название и классификацию кислот. 3. Познакомить учащихся с важнейшими неорганическими кислотами. © Осиевская И.А.
Кислоты, их состав и название. Цель урока: 1. Сформировать понятия о кислотах. 2. Рассмотреть состав, название и классификацию кислот. 3. Познакомить учащихся с важнейшими неорганическими кислотами. © Осиевская И.А.  Фосфор и его соединения
Фосфор и его соединения Физико-химические методы исследования биологически активных веществ
Физико-химические методы исследования биологически активных веществ Презентация по Химии "Предмет органической химии. Органические вещества" - скачать смотреть
Презентация по Химии "Предмет органической химии. Органические вещества" - скачать смотреть  Методика решения части С2 ГИА 9 класс
Методика решения части С2 ГИА 9 класс Фосфаттардағы байланыс теориясы
Фосфаттардағы байланыс теориясы Сульфаты и оксиды металлов
Сульфаты и оксиды металлов Механизм и закономерности кристаллизации металлов
Механизм и закономерности кристаллизации металлов Небезпечні хімічні речовини Підготувала: учениця 8 – А класу Кіровоградського НВК №34 Подколзіна Анна
Небезпечні хімічні речовини Підготувала: учениця 8 – А класу Кіровоградського НВК №34 Подколзіна Анна  Почему протекают химические реакции
Почему протекают химические реакции Презентация по химии Амины
Презентация по химии Амины Химия плутония, америция и трансамерициевых актиноидов
Химия плутония, америция и трансамерициевых актиноидов Неметаллы IVA и IIIA групп Углерод, кремний , бор
Неметаллы IVA и IIIA групп Углерод, кремний , бор Разложение отходов. 11 класс
Разложение отходов. 11 класс 10 класс семинар-написание формул органических веществ
10 класс семинар-написание формул органических веществ Электролиз водных растворов
Электролиз водных растворов Физическая и коллоидная химия
Физическая и коллоидная химия Влияние фтора на организм человека
Влияние фтора на организм человека Почему протекают химические реакции Начала термодинамики Автор: Фельдман Людмила Валентиновна, учитель химии МБОУ СОШ им. А.М.Гор
Почему протекают химические реакции Начала термодинамики Автор: Фельдман Людмила Валентиновна, учитель химии МБОУ СОШ им. А.М.Гор Классификация углеводородов
Классификация углеводородов Материаловедение. Теория сплавов
Материаловедение. Теория сплавов Древесина и её топливные свойства
Древесина и её топливные свойства Підгрупа карбону
Підгрупа карбону Вторичная переработка углеводородов
Вторичная переработка углеводородов