Содержание
- 2. Історія спирту Етиловий спирт, точніше рослинний хмільний напій, що його містить, був відомий людству з глибокої
- 3. Історія спирту Вперше синтез етанолу дією сірчаної кислоти на етилен здійснив у 1854 році французький хімік
- 4. Класифікація спиртів Якщо до складу молекули спирту входить одна гідроксильна група, то такий спирт називають одноатомним,
- 5. Хімічні властивості спиртів Кислотно-основні властивості Дегідратація Естерифікація Реакція окиснення
- 6. Кислотно-основні властивості Характерною хімічною властивістю спиртів є їх здатність Характерною хімічною властивістю спиртів є їх здатність
- 7. Кислотно-основні властивості Гідроксильний атом Гідрогену займає в молекулі особливе положення. На відміну від інших атомів Гідрогену,
- 8. Дегідратація Для спиртів характерним є також реакції дегідратації (відщеплення води). Так, при нагріванні вище 160°С етилового
- 9. Естерифікація Крім того, для спиртів характерні також реакції взаємодії з кислотами, внаслідок чого утворюються складні ефіри.
- 11. Скачать презентацию
Історія спирту
Етиловий спирт, точніше рослинний хмільний напій, що його містить, був
Історія спирту
Етиловий спирт, точніше рослинний хмільний напій, що його містить, був
Вперше спирт з вина отримали в 6-7 століттях арабські хіміки, а першу пляшку міцного алкоголю (прообразу сучасної горілки) виготовив перський алхімік Ар-Рази в 860 році.Структурна формула етанолу
У Європі етиловий спирт був отриманий із продуктів бродіння в 11-12 столітті в Італії.
До Росії спирт вперше потрапив у 1386 році, коли генуезьке посольство привезло його з собою під назвою «аква віта» і презентувала царського двору.
У 1660 році англійський хімік і богослов Роберт Бойль вперше отримав зневоднений етиловий спирт, а також відкрив його деякі фізичні і хімічні властивості, зокрема виявивши здатність етанолу бути високотемпературним пальним для пальників. Абсолютний (безводний) етиловий спирт був отриманий у 1796 році російським хіміком Т.Є. Ловіцем.
У 1842 році німецький хімік Якоб Генріх Вільгельм Шіль (1813-1889) відкрив, що спирти утворюють гомологічний ряд, відрізняючись на деяку постійну величину. Щоправда, він помилився описавши її як C2H2. Через два роки, інший хімік Шарль Жерар встановив правильне гомологічної співвідношення CH2 і передбачив формулу і властивості невідомого в ті роки пропілового спирту.
У 1850 році англійський хімік Олександр Вільямсон, досліджуючи реакцію алкоголятів з етилйодидом, встановив, що етиловий спирт є похідним від води з одним зміщенням Гідрогеном, експериментально підтвердив формулу C2H5OH.
Історія спирту
Вперше синтез етанолу дією сірчаної кислоти на етилен здійснив у
Історія спирту
Вперше синтез етанолу дією сірчаної кислоти на етилен здійснив у
Перше дослідження метилового спирту було проведено в 1834 році французькими хіміками Жаном-Батистом Дюма і Еженом Пеліго; вони назвали його «метиловим або деревним спиртом», так як він був виявлений в продуктах сухої перегонки деревини. Синтез метанолу з метилхлориду здійснив французький хімік Марселен Бертло в 1857 році. Ним же вперше був відкритий в 1855 році ізопропіловий спирт, синтезований дією на пропен водної сірчаної кислоти.
Вперше третинний спирт (трет-бутанол, 2-метил-пропан-2-ол) синтезував в 1863 році відомий російський вчений А. М. Бутлеров, поклавши початок цілої серії експериментів у цьому напрямку.
Молекула етиленгліколю, найпростішого діолу
Представник двоатомних спиртів — етиленгліколь — вперше був синтезований французьким хіміком А. Вюрцом в 1856 році. Триатомний спирт — гліцерин — був виявлений у природних жирах ще в 1783 році шведським хіміком Карлом Шеєле, однак його склад був відкритий тільки в 1836 році, а синтез здійснено з ацетону в 1873 році Шарлем Фріделем.
Класифікація спиртів
Якщо до складу молекули спирту входить одна гідроксильна група, то
Класифікація спиртів
Якщо до складу молекули спирту входить одна гідроксильна група, то
Спирти, як і вуглеводні, утворюють гомологічні ряди. Кожний наступний член цього ряду відрізняється від попереднього на гомологічну різницю -CH2-.
Назви спиртів походять від назв вуглеводневих радикалів, що входять до складу молекули спиртів. Міжнародні їх назви утворюються з назв відповідних вуглеводів з додаванням закінчення ол. Наприклад, CH3—OH — метиловий спирт, або метанол; C2H5—OH — етиловий спирт, або етанол і т. д.
Загальна формула одноатомних насичених спиртів CnH2n+1OH або R—OH, де R — вуглеводневий радикал. В таблиці наведений гомологічний ряд насичених одноатомних спиртів.
Нижчі спирти (з малою кількістю атомів Карбону в молекулі) при звичайній температурі є леткими рідинами, а вищі, починаючи з C15H31—OH, — тверді речовини. Нижчі спирти з водою зміщуються у всіх співвідношеннях. З підвищенням молекулярної маси розчинність спиртів зменшується. Усі спирти легші від води. В міру збільшення молекулярної маси температура кипіння спиртів підвищується.
Хімічні властивості спиртів
Кислотно-основні властивості
Дегідратація
Естерифікація
Реакція окиснення
Хімічні властивості спиртів
Кислотно-основні властивості
Дегідратація
Естерифікація
Реакція окиснення
Кислотно-основні властивості
Характерною хімічною властивістю спиртів є їх здатність Характерною хімічною властивістю
Кислотно-основні властивості
Характерною хімічною властивістю спиртів є їх здатність Характерною хімічною властивістю
2C2H5—OH + 2Na → 2C2H5—ONa + H2 ↑.
Інші атоми Гідрогену, котрі зв'язані безпосередньо з Карбоном, у реакцію не вступають. На прикладі цих реакцій науковці вперше зустрілись з явищем впливу одних атомів на інші в молекулі. Суть цього впливу можна показати на прикладі молекули етилового спирту, електронну будову якої можна зобразити в такому вигляді:будову якої можна зобразити в такому вигляді:
Кислотно-основні властивості
Гідроксильний атом Гідрогену займає в молекулі особливе положення. На відміну
Кислотно-основні властивості
Гідроксильний атом Гідрогену займає в молекулі особливе положення. На відміну
У спиртах можуть заміщатися не лише гідроксильні атоми Гідрогену, а і вся гідроксильна група. Наприклад, при нагріванні етилового спирту з бромоводнем утворюється бромоетан:
Дегідратація
Для спиртів характерним є також реакції дегідратації (відщеплення води). Так, при
Дегідратація
Для спиртів характерним є також реакції дегідратації (відщеплення води). Так, при
Естерифікація
Крім того, для спиртів характерні також реакції взаємодії з кислотами, внаслідок
Естерифікація
Крім того, для спиртів характерні також реакції взаємодії з кислотами, внаслідок








 Введение. Основные понятия химии
Введение. Основные понятия химии I закон термодинамики, его применение для расчёта тепловых эффектов
I закон термодинамики, его применение для расчёта тепловых эффектов Дозиметрия ионизирующих излучений. Влияние радиации на организм человека
Дозиметрия ионизирующих излучений. Влияние радиации на организм человека Камни и Рак
Камни и Рак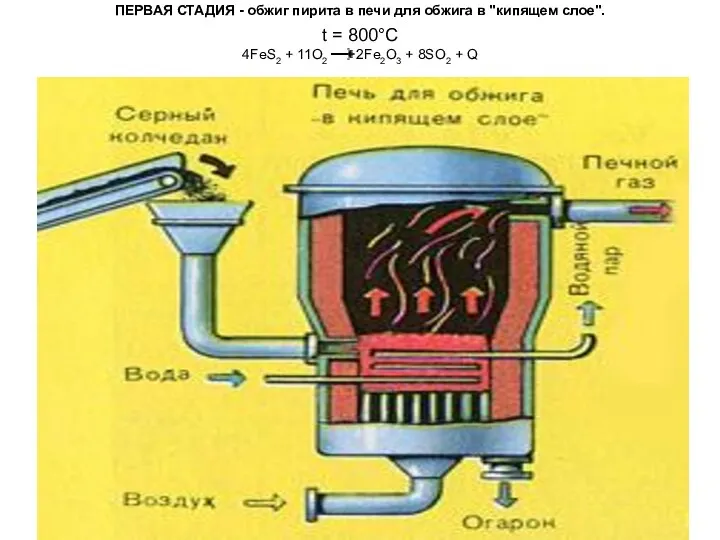 Получение серной кислоты
Получение серной кислоты Презентация Спирты
Презентация Спирты Глицерин Свойства - применение Выполнила учитель химии МОУ «Средняя школа №7» г. Балаково Саратовской области Трибунская Е
Глицерин Свойства - применение Выполнила учитель химии МОУ «Средняя школа №7» г. Балаково Саратовской области Трибунская Е Получение водорода в промышленности и его применение Химия 8 класс
Получение водорода в промышленности и его применение Химия 8 класс  Исследование влияния концентрации наночастиц никеля в водных растворах на генерацию активных форм кислорода при лазерном пробое
Исследование влияния концентрации наночастиц никеля в водных растворах на генерацию активных форм кислорода при лазерном пробое Классификация химических элементтов
Классификация химических элементтов Презентация по Химии "Нитраты - минеральные удобрения" - скачать смотреть
Презентация по Химии "Нитраты - минеральные удобрения" - скачать смотреть  Фізичні та хімічні явища. (7 клас)
Фізичні та хімічні явища. (7 клас) Каучук. История открытия
Каучук. История открытия Материаловедение. Теория термической обработки стали. (Тема 8)
Материаловедение. Теория термической обработки стали. (Тема 8) Органические вещества. Валентность. Теория химического строения
Органические вещества. Валентность. Теория химического строения Основы общей химии
Основы общей химии Важнейшие химические понятия и законы
Важнейшие химические понятия и законы Презентация по химии Неорганические и органические основания.
Презентация по химии Неорганические и органические основания.  Особенности строения, реакционной способности и методы синтеза алкенов
Особенности строения, реакционной способности и методы синтеза алкенов Водород, нахождение в природе. Получение водорода и его физические свойства
Водород, нахождение в природе. Получение водорода и его физические свойства Классификация оснований
Классификация оснований PSKhE
PSKhE Электрофизические свойства GaAs, зонная структура, полупроводящий и полуизолирующий GaAs, способы создания p-n перехода
Электрофизические свойства GaAs, зонная структура, полупроводящий и полуизолирующий GaAs, способы создания p-n перехода Деструкция углеводородов
Деструкция углеводородов Физические, химические свойства предельных и непредельных карбоновых кислот, получение
Физические, химические свойства предельных и непредельных карбоновых кислот, получение Классификация силикатов
Классификация силикатов - Это оружие массового поражения, действие которого основано на токсических свойствах химических веществ. - Это оружие массового
- Это оружие массового поражения, действие которого основано на токсических свойствах химических веществ. - Это оружие массового  Алюминий и его органические производные
Алюминий и его органические производные