Сполуки неметалічних елементів з Гідрогеном. Склад, фізичні властивості, добування в лабораторії аміаку і хлороводню. Взаємод
Содержание
- 2. Мета: . Ознайомити зі складом та особливостями будови молекули аміаку та хлорводню. Розглянути лабораторні способи добування
- 3. Демонстрації: 1. Якісна реакція на хлорид-іон. 2. Добування амоніаку і розчинення його у воді (“фонтан”), випробування
- 4. Сполуки неметалічних елементів з Гідрогеном.
- 5. Склад і назви сполук. Сполуки з Гідрогеном відомі для більшості неметалічних елементів; їх не утворюють лише
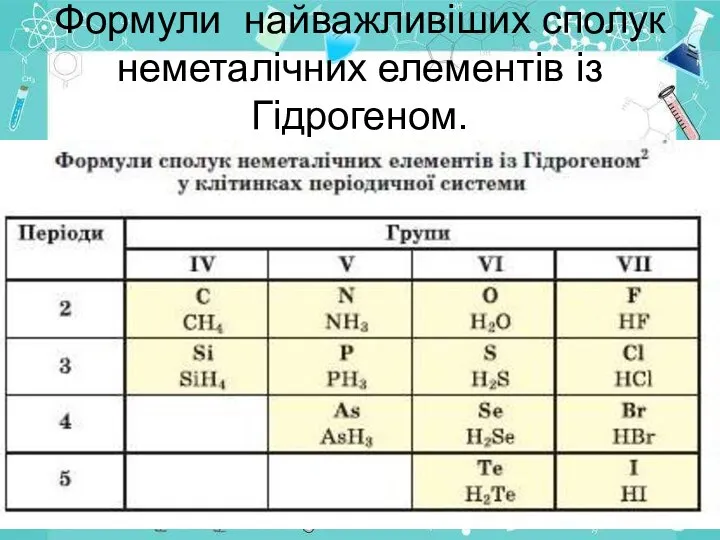
- 6. Формули найважливіших сполук неметалічних елементів із Гідрогеном.
- 7. Загальна формула сполук елементів із Гідрогеном має два варіанти написання — НnЕ і ЕНn. Послідовність запису
- 8. Для сполук неметалічних елементів із Гідрогеном частіше використовують тривіальні назви амоніак, метан, вода, хлороводень, сірководень та
- 9. Будова. Сполуки неметалічних елементів із Гідрогеном складаються з молекул Атоми в них сполучені ковалентними зв'язками. Якщо
- 10. Якщо позитивні й негативні заряди, що виникли на атомах унаслідок зміщення спільних електронних пар, рівномірно розподілені
- 11. Фізичні властивості. Більшість сполук неметалічних елементів із Гідрогеном за звичайних умов є газами, а гідроген фторид
- 12. Найбільшу розчинність у воді мають сполуки галогенів із Гідрогеном та амоніак. Наприклад, в 1 л води
- 13. Метан СН4 інертний щодо води (за звичайних умов). Водний розчин амоніаку NН3, на відміну від розчинів
- 14. Нітроген
- 15. Історія вікриття нітрогену: У 1772 р. Англієць Д. Резерфорд встановив, що повітря, що залишився під дзвоном,
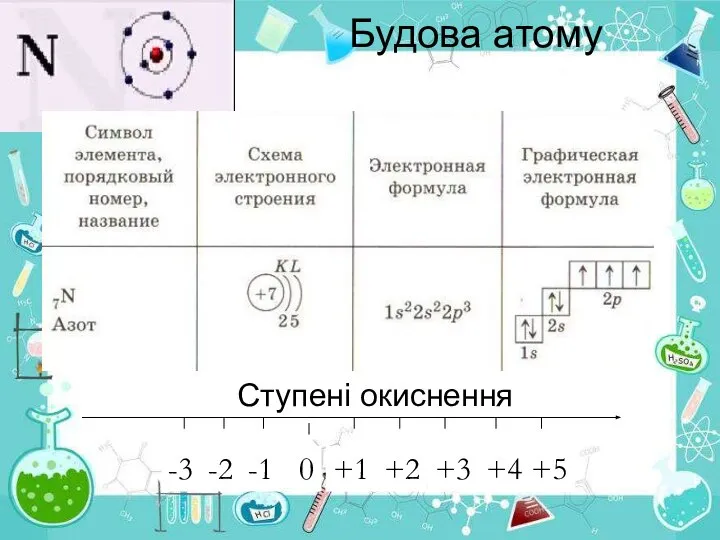
- 16. Будова атому Ступені окиснення -1 0 +1 -2 -3 +2 +3 +4 +5
- 17. Яким чином можна пояснити хімічну інертність молекули азоту? ? 2 атома азоту з'єднані в молекулу потрійний
- 18. Отримання :
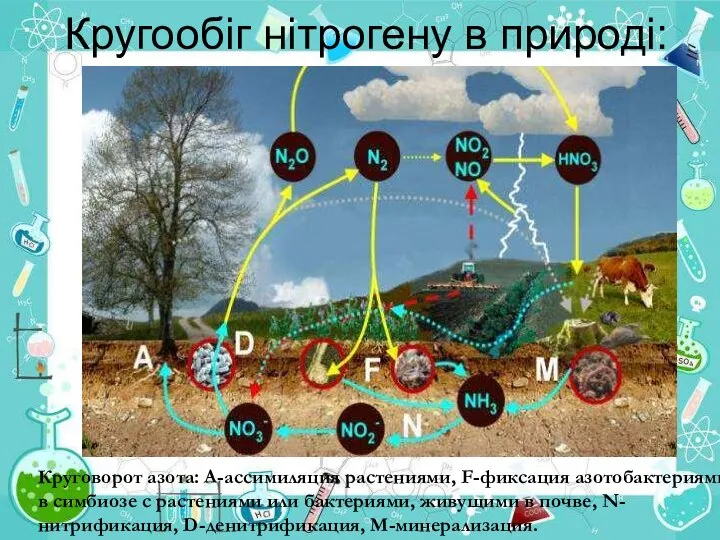
- 19. Кругообіг нітрогену в природі: Круговорот азота: А-ассимиляция растениями, F-фиксация азотобактериями в симбиозе с растениями или бактериями,
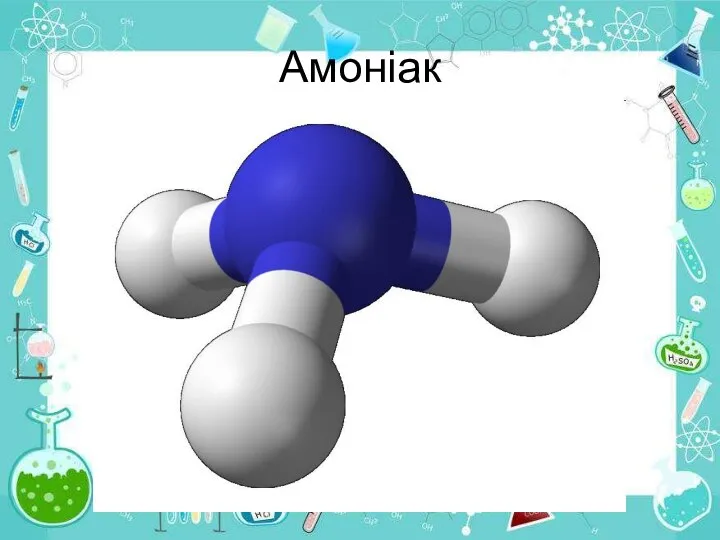
- 20. Амоніак
- 21. Амоніак Будова молекули. Молекула аміаку NH3 являє собою диполь: спільні електронні пари дуже зміщені до атома
- 22. Властивості амоніаку. Амоніак – безбарвний газ з різким запахом. При температурі, нижчій за – 33,4ОС, він
- 23. Для амоніаку характерні реакції приєднання і окислення. 1.Взаємодіє з водою і утворює гідрати NH3.H2O, NH3+H2O=NH4OH. Лужна
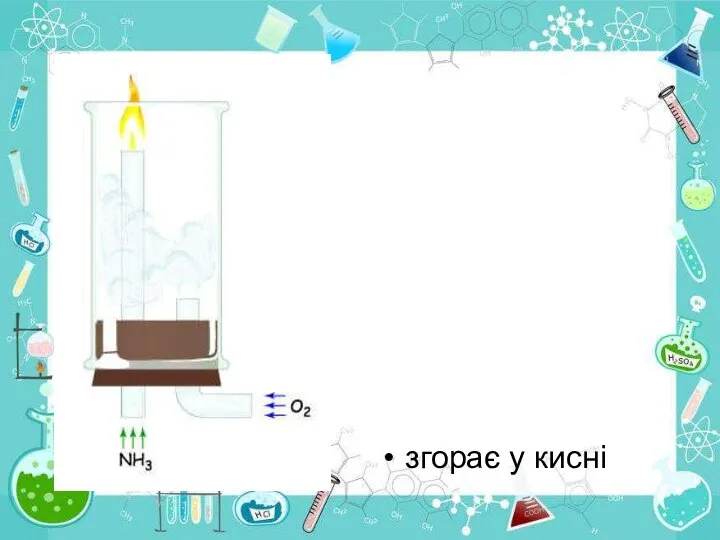
- 24. згорає у кисні
- 25. Якісна реакція на NH 1) взаємодія з лугами: _ + NH ОН =NH3 +H2O Реакцію проводять:
- 26. Добування У лабораторії амоніак добувають, нагріваючи амоній хлорид гашеним вапном. 2NH4Cl+Ca(OH)2=CaCl2+H2O+2NH3 Амоніак, що утворився висушують СаО.
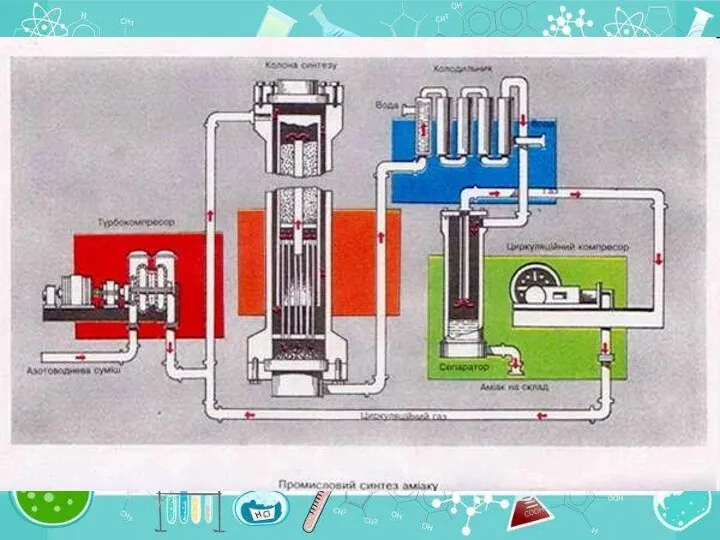
- 28. 1 - компресор; 2 - фільтр; 3 - контактний апарат; 4 - холодильник; 5 - збірник.
- 29. Застосування. Аміак — важливий продукт хімічної промисловості. Його використовують як добриво і для виробництва азотних добрив,
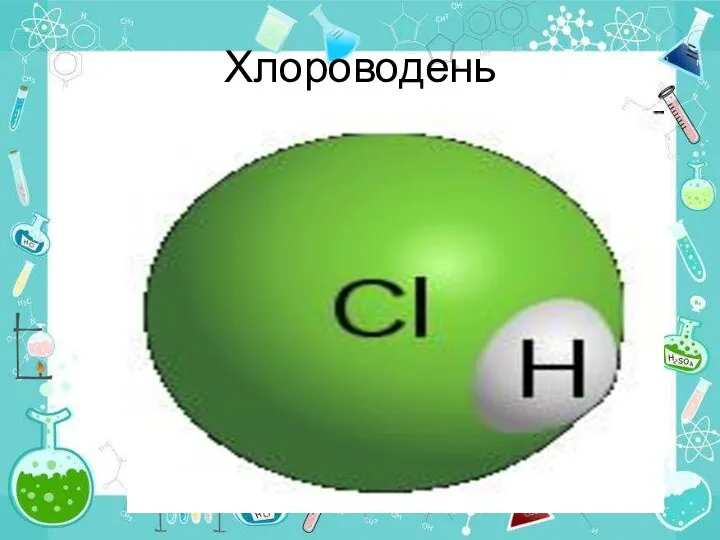
- 30. Хлороводень
- 31. Електронна і графічна формули молекули хлороводню:
- 32. Хлороводень (HCl) — безбарвний задушливий газ з різким запахом. Температура розплавлення: −115 °C (158 K), температура
- 33. Розчин хлороводню у воді називають хлоридною, або соляною, кислотою. Поява кислотних властивостей хлороводню в розчині обумовлюється
- 34. Хімічні властивості. Хлоридна кислота реагує: • з металами з виділенням водню • з основними й амфотерними
- 35. Добування гідроген хлориду і хлоридної кислоти. У промисловості гідроген хлорид добувають спалюванням водню в атмосфері хлору
- 36. Н2 + С12 = 2НС1, а в лабораторії — за реакцією обміну між твердою сіллю (натрій
- 37. ВЗАЄМОДІЯ АМОНІАКУ ТА ХЛОРОВОДНЮ З ВОДОЮ. Аміак добре розчиняється у воді утворюючи аміачну воду (за нормальних
- 38. Солі амонію.
- 39. СОЛІ АМОНІЮ — це кристалічні речовини з йонним типом зв'язку. До складу солей амонію входять один
- 40. Нітрат амонію
- 41. Солі амонію добувають при взаємодії амоніаку або амоній гідроксид з кислотами: NH3+NHО3=NH4NО3; 2NH3+H2SO4=(NH4)2SO4; NH4OH+HNO3=NH4NO3+H2O. У катіоні
- 42. Хімічні властивості солей Сіль і метал Сіль і основа Сіль Сіль і кислота Сіль і сіль
- 43. Солі амонію виявляють загальні властивості солей: 1) взаємодіють з лугами: NH4Cl+NaOH=NaCl+NH4OH (NH3 +H2O) 2) взаємодіють з
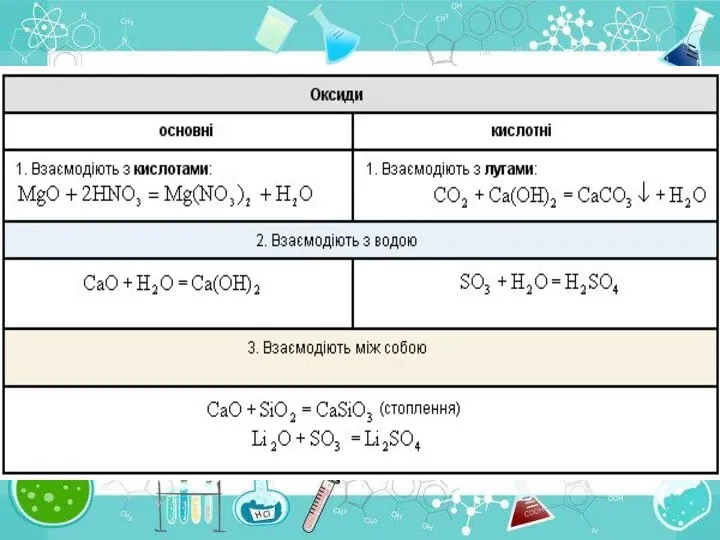
- 44. Оксиди неметалічних елементів. Мають кислотний характер
- 46. СУЛЬФУР утворює два кислотні оксиди: оксид сульфуру (ІV) S02 і оксид сульфуру(VI) S03
- 47. Оксид сульфуру(IV) SO2 (діоксид сульфуру, сірчистий газ) — це безбарвний важкий газ (у 2,2 раза важчий
- 48. НІТРОГЕН З ОКСИГЕНОМ утворює п'ять оксидів, в яких він виявляє ступінь окиснення від +1 до +5:
- 49. Оксид нітрогену (І) N20 — безбарвний газ із приємним запахом, залежить до несолетвірних оксидів. Під назвою
- 50. З оксидів фосфору Р205 і Р203 найбільше значення має оксид фосфору(V).
- 51. Оксид фосфору (V) Р205 — білий дрібнокристалічний порошок, дуже гігроскопічний, тому застосовується для осушування газів. Типовий
- 52. ЕЛЕМЕНТ КАРБОН З ЕЛЕМЕНТОМ ОКСИГЕНОМ утворює два оксиди — С02 і СО. С02 — оксид карбону(IV),
- 53. Оксид карбону(IV), або вуглекислий газ, С02 за звичайних умов — безбарвний газ, без запаху, важчий за
- 54. Взаємодія з водою. Якщо у пробірку з водою (1 — 2 мл) додати 1—2 краплі розчину
- 55. Добування оксиду карбону(ІУ). У лабораторних умовах С02 добувають дією хлоридної кислоти на мармур: СаС03 + 2НСl
- 56. Для елемента Силіцію характерним є SiO2 —оксид силіцію(IV), діоксид силіцію, кремнезем.
- 57. Оксид силіцію(ІV) SiO2, або діоксид силіцію, — тверда речовина, кристалічна, безбарвна, тугоплавка (tпл. 1728 °С), у
- 59. Скачать презентацию
















































 Сера и ее важнейшие соединения 16S 1s22s22p63s23p4 (р- элемент) S8 – ромбическая сера (наиболее устойчивая аллотропная модификация серы;
Сера и ее важнейшие соединения 16S 1s22s22p63s23p4 (р- элемент) S8 – ромбическая сера (наиболее устойчивая аллотропная модификация серы; Медь и ее сплавы
Медь и ее сплавы Нестандартные методы активации химических реакций
Нестандартные методы активации химических реакций Чистые вещества и смеси. Способы разделения смесей
Чистые вещества и смеси. Способы разделения смесей Щелочно-земельные металлы
Щелочно-земельные металлы Реакционная способность углеводородов
Реакционная способность углеводородов НЕМЕТАЛЛЫ Все, что я познаю, я знаю, для чего это мне надо и где и как я могу эти знания применить. Найти разумный баланс между
НЕМЕТАЛЛЫ Все, что я познаю, я знаю, для чего это мне надо и где и как я могу эти знания применить. Найти разумный баланс между  Анилин. Физические свойства
Анилин. Физические свойства Физическая химия дисперсных систем. Коллоидные растворы
Физическая химия дисперсных систем. Коллоидные растворы Гелий. История открытия
Гелий. История открытия Магматичні родовища
Магматичні родовища Проект. Создание производства гранулированных биоорганических удобрений
Проект. Создание производства гранулированных биоорганических удобрений Презентация по Химии "Железо" - скачать смотреть
Презентация по Химии "Железо" - скачать смотреть  Роль хімічних знань у пізнанні природи
Роль хімічних знань у пізнанні природи Презентация по Химии "«Химические волокна»" - скачать смотреть
Презентация по Химии "«Химические волокна»" - скачать смотреть  Дисперсные системы
Дисперсные системы Неорганическая химия
Неорганическая химия Формування ВМ з заданою структурою
Формування ВМ з заданою структурою Карбоновые кислоты
Карбоновые кислоты Материаловедение. Виды и свойства материалов
Материаловедение. Виды и свойства материалов Диаграммы состояния двухкомпонентных сплавов
Диаграммы состояния двухкомпонентных сплавов Органическая химия
Органическая химия Кремний (Silicium). Химические свойства
Кремний (Silicium). Химические свойства Химическая кинетика
Химическая кинетика Методы получения основных классов неорганических соединений
Методы получения основных классов неорганических соединений Свойства растворов
Свойства растворов Алкины — углеводороды, содержащие тройную связь между атомами углерода
Алкины — углеводороды, содержащие тройную связь между атомами углерода Презентация по Химии "Аммиак" - скачать смотреть
Презентация по Химии "Аммиак" - скачать смотреть