Содержание
- 2. Определите тип химической связи для веществ: Na NaCl Cl2 HCl металлическая ионная Ковалентная неполярная Ковалентная полярная
- 3. У каких веществ будут наблюдаться заряды атомов в соединениях Na NaCl Cl2 HCl 0 атом электронейтрален
- 4. Степень окисления – это условный заряд атомов химического элемента в соединении, вычисленный на основе предположения, что
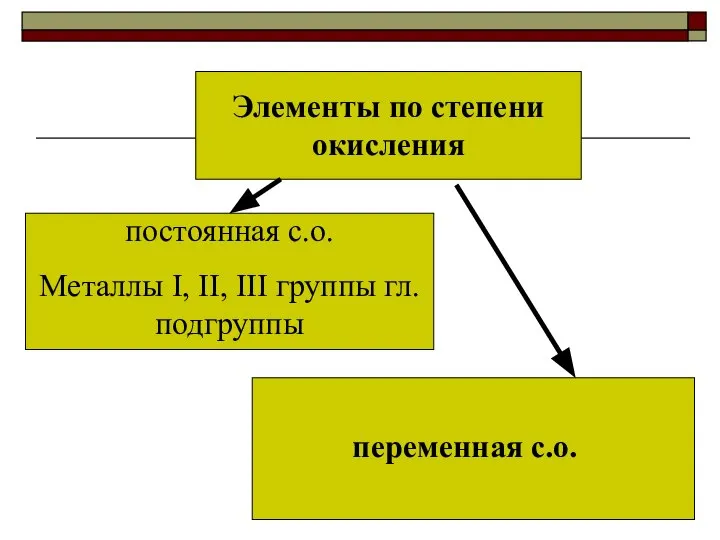
- 5. Элементы по степени окисления постоянная с.о. Металлы I, II, III группы гл. подгруппы переменная с.о.
- 6. У атомов кислорода с.о. всегда -2. У атомов водорода с.о. +1, с металлами -1. У металлов
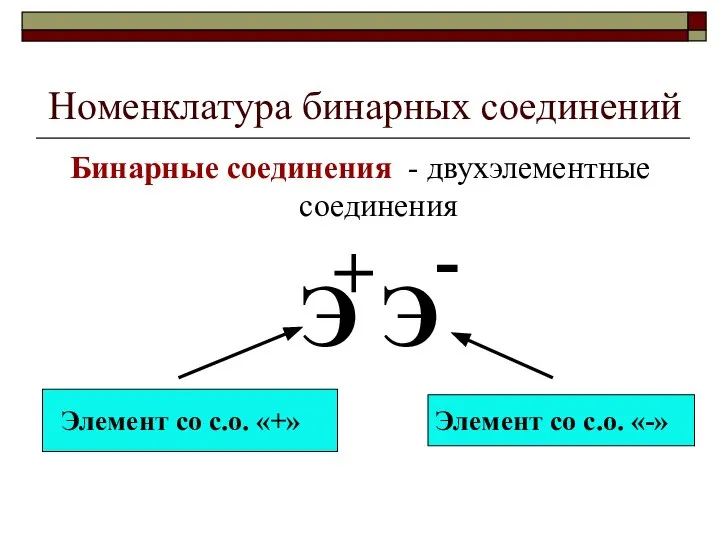
- 7. Номенклатура бинарных соединений Бинарные соединения - двухэлементные соединения Э Э - + Элемент со с.о. «+»
- 8. Название бинарных соедиенений– латинское с суффиксом «ид» Хлорид – соединения хлора Карбид – соединения углерода Сульфид
- 9. Определение степени окисления по формуле
- 10. Выполните задание 1 Определите с.о. у оксидов азота. NO N2O N2O3 NO2 N2O5 2 Определите с.о.
- 11. Составление формул по с.о. 1 если с.о. одинаковы, то индексы не ставят. 2 если с.о. разные
- 12. Составление формул по степени окисления
- 13. Выполните задание 1 Составьте формулы по степени окисления А) Оксидов: марганца II, IV, VI, VII. Б)
- 14. Домашнее задание Параграф 17 упр. №1,2,4,5. Р.Т. стр 54-57
- 15. Оксиды
- 16. Расставьте степени окисления и составьте формулы веществ СuO PO KO FeO SO +2 +3 СuO P2O5
- 17. Оксиды – сложные вещества, состоящие из двух химических элементов, один из которых кислород в с.о. -2.
- 18. Запишите формулы веществ и расставьте с.о. H2SO4 SO2 K2SO4 OF2 H2O H2O2 WO3 SO2 H2O WO3
- 19. Оксиды в природе Запишите формулы оксидов встречающихся в природе Руды железа Оксид железа III красный железняк
- 20. Запишите формулы оксидов встречающихся в природе Оксид кремния песок, кварц Оксид алюминия глина, боксит Оксид водорода
- 21. Запишите формулы оксидов встречающихся в природе Оксид азота IV бурый газ Оксид серы IV сернистый газ
- 22. Решите задачу Какой объем займут 88 г углекислого газа? Сколько атомов каждого элемента содержится в этом
- 24. Скачать презентацию



















 Интеллектуальная разминка HCl, H2SO4, H2CO3, H3PO4, HNO3. Al2O3 , CaO, Na2O, CO2, CuO. KOH, Ba(OH)2, Al(OH)3, Cu(OH)2, Fe(OH)3. BaСl2, ZnSO4, MgS, Ca(NO3)2.
Интеллектуальная разминка HCl, H2SO4, H2CO3, H3PO4, HNO3. Al2O3 , CaO, Na2O, CO2, CuO. KOH, Ba(OH)2, Al(OH)3, Cu(OH)2, Fe(OH)3. BaСl2, ZnSO4, MgS, Ca(NO3)2.  Веселый химический КВН
Веселый химический КВН Изомерия алкенов. Цель урока: закрепить понятие изомеры, познакомить с геометрической изомерией
Изомерия алкенов. Цель урока: закрепить понятие изомеры, познакомить с геометрической изомерией  Медицинская химия, введение. (Лекция 1)
Медицинская химия, введение. (Лекция 1) Производство геля для душа и его состав
Производство геля для душа и его состав Основания, их классификация и свойства в свете ТЭД
Основания, их классификация и свойства в свете ТЭД Получение галогенов. Биологическое значение и применение галогенов и их соединений
Получение галогенов. Биологическое значение и применение галогенов и их соединений Химические элементы O, S, Se, Te_Feb
Химические элементы O, S, Se, Te_Feb Методы экстрагирования ЛРС и оборудование
Методы экстрагирования ЛРС и оборудование Химия и стирка
Химия и стирка  Нуклеиновые кислоты
Нуклеиновые кислоты Презентация по Химии "Гетероциклические соединения" - скачать смотреть
Презентация по Химии "Гетероциклические соединения" - скачать смотреть  Способы переработки нефти
Способы переработки нефти Free Radical Polymerization
Free Radical Polymerization Презентация по Химии "ГАЛЕРЕЯ РУССКИХ ХИМИКОВ" - скачать смотреть бесплатно
Презентация по Химии "ГАЛЕРЕЯ РУССКИХ ХИМИКОВ" - скачать смотреть бесплатно Токсическое действие неорганических веществ
Токсическое действие неорганических веществ Углеводный обмен
Углеводный обмен Гетероциклические соединения. Шестичленные гетероциклы с одним гетероатомом
Гетероциклические соединения. Шестичленные гетероциклы с одним гетероатомом Белки, или протеины
Белки, или протеины Оксосоединения. Основные понятия
Оксосоединения. Основные понятия Превращение веществ
Превращение веществ Электронная оболочка. Строение электронных оболочек атомов химических элементов
Электронная оболочка. Строение электронных оболочек атомов химических элементов Хлор (лат. Chlorum, Cl)
Хлор (лат. Chlorum, Cl) «Нұрбанк» Акционерлік қоғамы
«Нұрбанк» Акционерлік қоғамы Дизельное топливо
Дизельное топливо Основные классы неорганических соединений
Основные классы неорганических соединений Основы МКТ
Основы МКТ Стиральные порошки и средства для стирки 2016
Стиральные порошки и средства для стирки 2016