Содержание
- 2. «Нет ничего кроме атомов и пустоты. Все прочее - впечатления» Демокрит (460-370 гг. до н. э.)
- 3. Существует предел деления - атом Демокрит (460-370 гг. до н.э.) Аристотель (384-322 гг. до н. э.)
- 4. Только в XVIII веке трудами А. Лавуазье, М. В. Ломоносова и других ученых Лавуазье Антуан Лоран
- 5. В 1897 году Джозеф Джон Томсон открыл электрон. Опыты Томсона подтвердили, что электроны входят в состав
- 6. Атом – это шар, по всему объёму которого равномерно распределён положительный заряд. Внутри шара находятся электроны.
- 7. Модель строения атома, предложенная Томсоном, нуждалась в экспериментальной проверке. В 1911 г. Эрнест Резерфорд совместно со
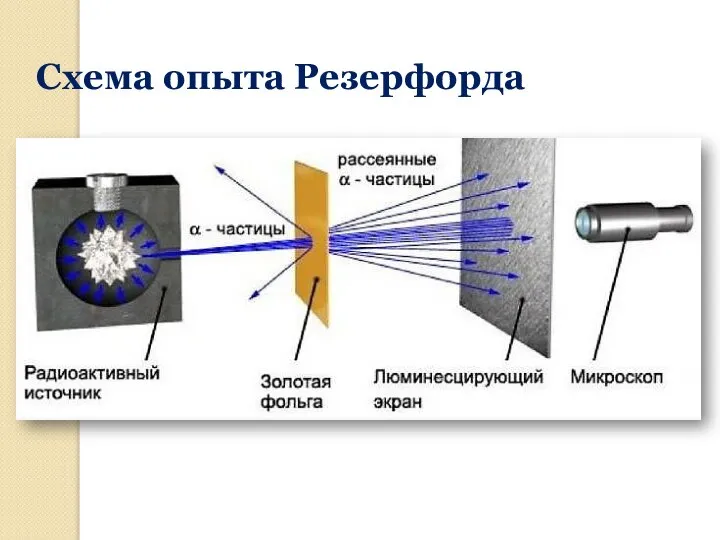
- 8. Схема опыта Резерфорда
- 9. Сцинтилляции на экране в отсутствие фольги Сцинтилляции на экране, когда на пути пучка помещена фольга
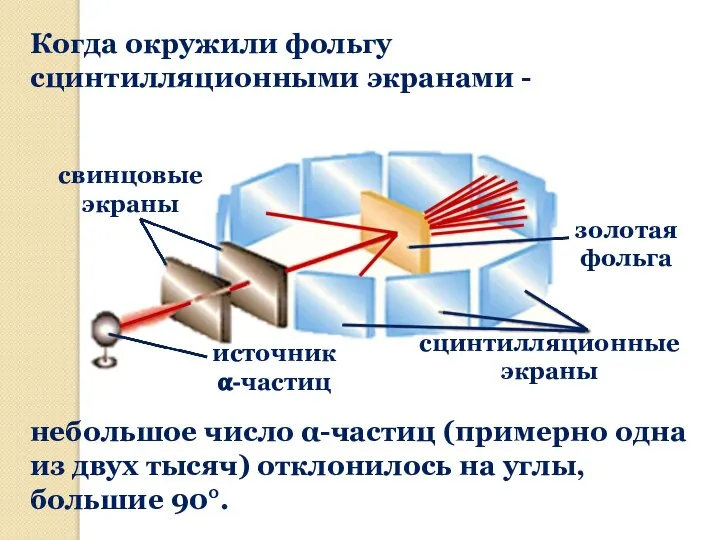
- 10. источник ?-частиц свинцовые экраны сцинтилляционные экраны золотая фольга Когда окружили фольгу сцинтилляционными экранами - небольшое число
- 11. Резерфорд о рассеянии α-частиц на большие углы: «Это почти столь же невероятно, как если бы вы
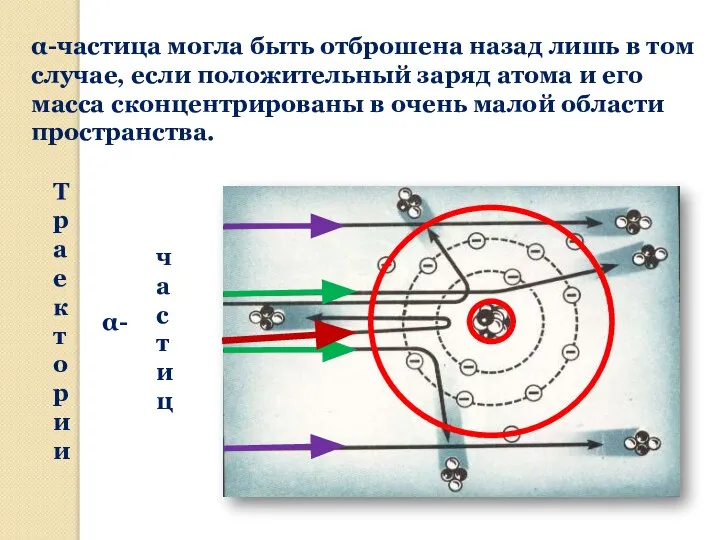
- 12. α-частица могла быть отброшена назад лишь в том случае, если положительный заряд атома и его масса
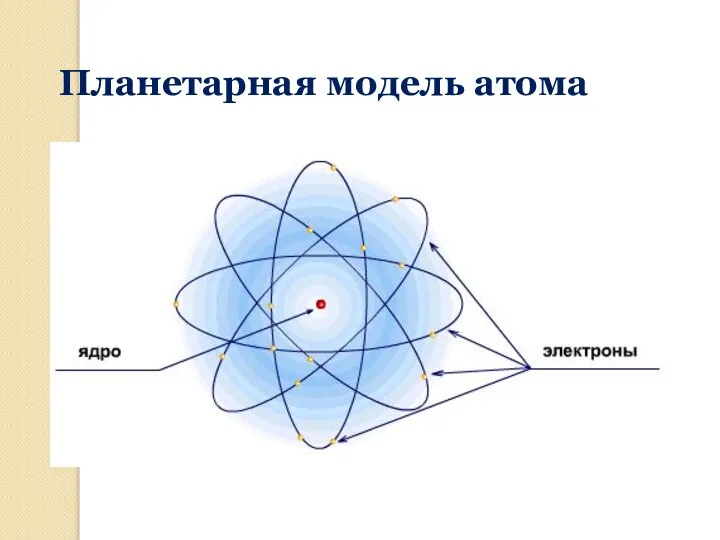
- 13. Планетарная модель атома
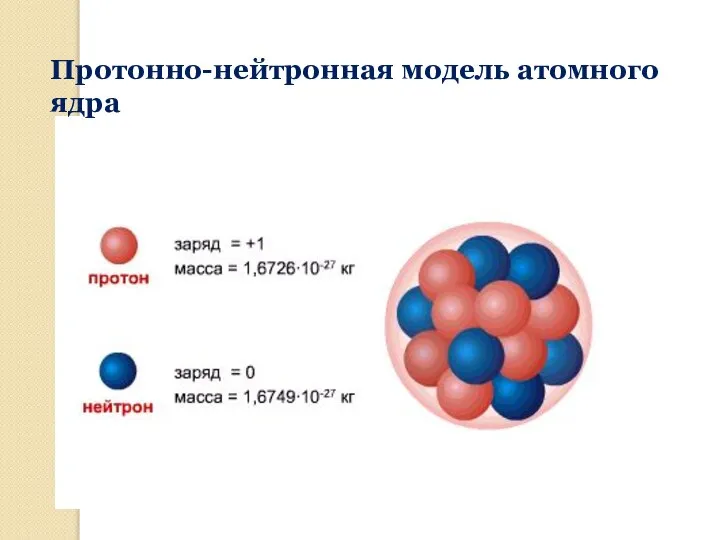
- 14. Протонно-нейтронная модель атомного ядра
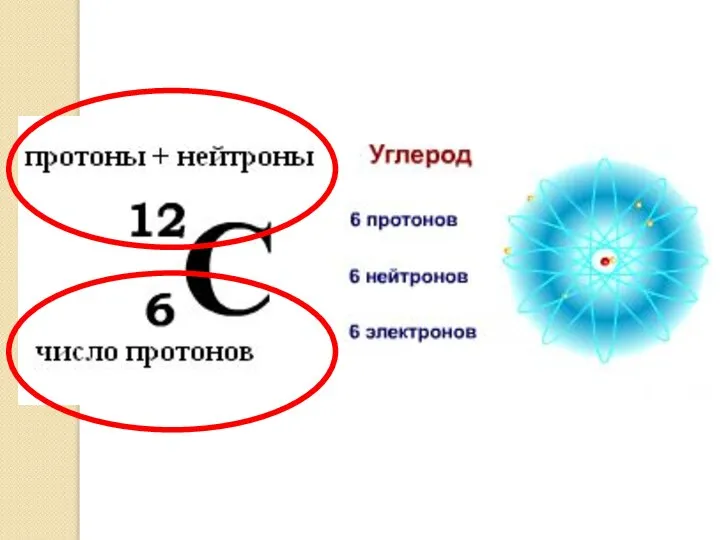
- 15. Порядковый номер Z элемента в периодической таблице Д.И. Менделеева – это число электронов в атоме, число
- 17. Но эта модель не объясняет устойчивость атома. Атом должен прекратить свое существование. Электрон излучает и теряет
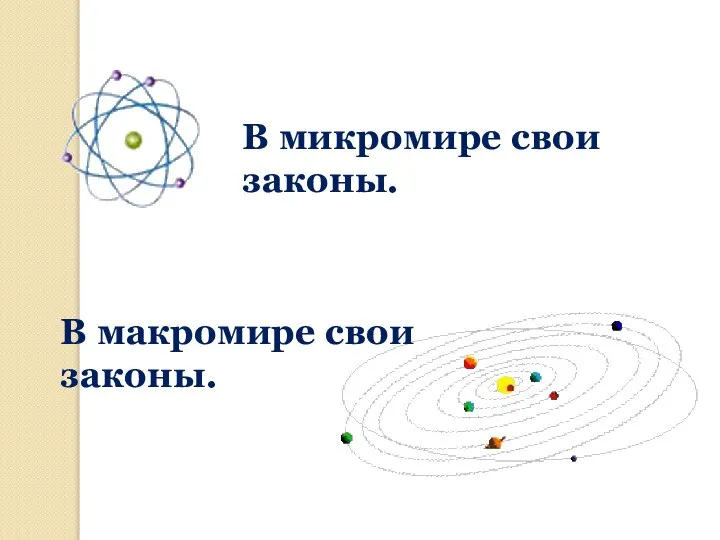
- 18. В микромире свои законы. В макромире свои законы.
- 20. Скачать презентацию










 Химическая термодинамика и кинетика
Химическая термодинамика и кинетика Основні класи неорганічних речовин
Основні класи неорганічних речовин Паровые зоны в гидротермальных системах
Паровые зоны в гидротермальных системах Учебно - исследовательский проект «Выращивание кристаллов в домашних условиях»
Учебно - исследовательский проект «Выращивание кристаллов в домашних условиях» Презентация по Химии "Изотопы" - скачать смотреть
Презентация по Химии "Изотопы" - скачать смотреть  Конструкционные функциональные волокнистые композиты
Конструкционные функциональные волокнистые композиты Уравнения химических реакций
Уравнения химических реакций Крем
Крем  Коррозия металла
Коррозия металла Нафта, вугілля, природний газ як вуглеводнева сировина. Основні види палива та їх значення в енергетиці країни.
Нафта, вугілля, природний газ як вуглеводнева сировина. Основні види палива та їх значення в енергетиці країни.  Методы нахождения коэффициентов в уравнениях химических реакций
Методы нахождения коэффициентов в уравнениях химических реакций Производные карбиновой, тио- и дитиокарбаминовой кислот (карбаматы)
Производные карбиновой, тио- и дитиокарбаминовой кислот (карбаматы) Презентация по Химии "Проблема вмісту нітратів у харчових продуктах" - скачать смотреть бесплатно
Презентация по Химии "Проблема вмісту нітратів у харчових продуктах" - скачать смотреть бесплатно Алюминий и его соединения
Алюминий и его соединения Алмазы, искусственный и естественный рост
Алмазы, искусственный и естественный рост Хлор 11 класс - Презентация
Хлор 11 класс - Презентация Кристаллохимия. Тығыз шарлар теориясы
Кристаллохимия. Тығыз шарлар теориясы Основания и соли
Основания и соли ФКХ-Л2 2016
ФКХ-Л2 2016 Тотығу түрлері.Липидтердің пероксидті тотығуы (ЛПТ), антиоксиданттар
Тотығу түрлері.Липидтердің пероксидті тотығуы (ЛПТ), антиоксиданттар Побутові хімікати
Побутові хімікати Пластмассы
Пластмассы Производство метанола и этанола
Производство метанола и этанола Хром және оның қосылыстары
Хром және оның қосылыстары Основные классы неорганических соединений
Основные классы неорганических соединений Д. И. Менделеев в высказываниях
Д. И. Менделеев в высказываниях Учение о растворах
Учение о растворах Реакции координированных лигандов
Реакции координированных лигандов