Содержание
- 3. Количество электронов в оболочке атома соответствует числу протонов в ядре атома.
- 5. Орбиталь — пространство вокруг ядра атома, где наиболее вероятно нахождение данного электрона
- 6. Орбитали составляют энергетические уровни.
- 8. Электронная оболочка атомов первого периода содержит один энергетический уровень.
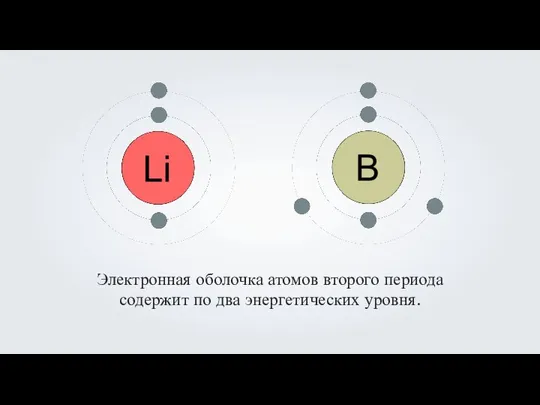
- 9. Электронная оболочка атомов второго периода содержит по два энергетических уровня.
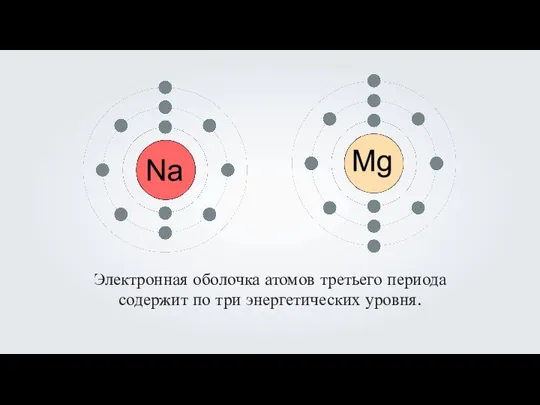
- 10. Электронная оболочка атомов третьего периода содержит по три энергетических уровня.
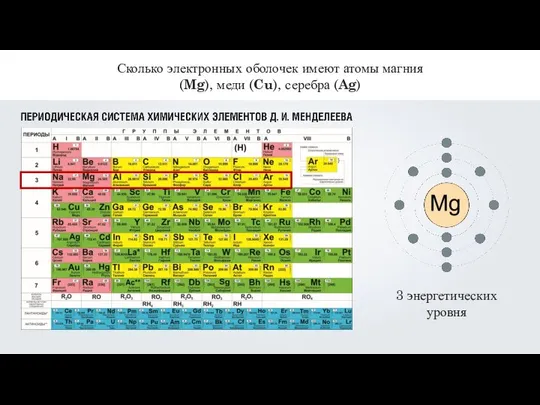
- 11. Сколько электронных оболочек имеют атомы магния (Mg), меди (Cu), серебра (Ag)
- 12. Сколько электронных оболочек имеют атомы магния (Mg), меди (Cu), серебра (Ag)
- 13. Сколько электронных оболочек имеют атомы магния (Mg), меди (Cu), серебра (Ag) 5 энергетических уровней
- 14. Максимальное число электронов, находящихся на энергетическом уровне можно определить по следующей формуле: 2n2
- 15. Максимальное количество электронов на первом уровне: 2⋅12= 2 Максимальное количество электронов на втором уровне: 2⋅22= 8
- 22. Построение схемы строения электронных оболочек на примере гелия (Не), бора (B), кислорода (O), фтора (F) 1.
- 23. Построение схемы строения электронных оболочек на примере гелия (Не), бора (B), кислорода (O), фтора (F) Определим
- 24. Построение схемы строения электронных оболочек на примере гелия (Не), бора (B), кислорода (O), фтора (F) А
- 25. Построение схемы строения электронных оболочек на примере гелия (Не), бора (B), кислорода (O), фтора (F) Бор
- 26. Построение схемы строения электронных оболочек на примере гелия (Не), бора (B), кислорода (O), фтора (F) Кислород
- 27. Построение схемы строения электронных оболочек на примере гелия (Не), бора (B), кислорода (O), фтора (F) Фтор
- 28. s-, p-, d- и f-орбитали
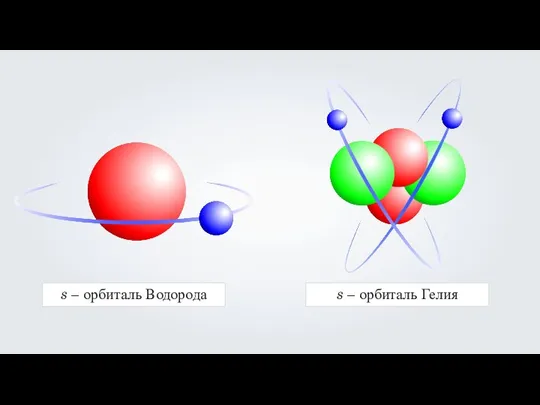
- 29. s - орбиталь
- 30. s – орбиталь Водорода s – орбиталь Гелия
- 31. Н – 1S1 He – 1S2 Li – 1S22S1 Mg – 1S22S22p63S2 B – 1S22S22p1 Электронные
- 32. Электронные формулы химических элементов первых трёх периодов Н – 1S1 He – 1S2 Li – 1S22S1
- 34. Скачать презентацию


























 Stereochemistry.Isomers are different compounds
Stereochemistry.Isomers are different compounds ПЕРВОНАЧАЛЬНЫЕ ХИМИЧЕСКИЕ ПОНЯТИЯ ОБОБЩАЮЩИЙ УРОК
ПЕРВОНАЧАЛЬНЫЕ ХИМИЧЕСКИЕ ПОНЯТИЯ ОБОБЩАЮЩИЙ УРОК  Сера
Сера Металлы. Кроссворд
Металлы. Кроссворд Урок - лекция с контролем в 10 классе
Урок - лекция с контролем в 10 классе  Определение массовой концентрации общего железа с сульфосалициловой кислотой. (Лабораторная работа 2)
Определение массовой концентрации общего железа с сульфосалициловой кислотой. (Лабораторная работа 2) Особенности КИМ ЕГЭ 2015 года по химии Составитель: Снастина М. Г. Москва 2014 г.
Особенности КИМ ЕГЭ 2015 года по химии Составитель: Снастина М. Г. Москва 2014 г.  Презентация Соли
Презентация Соли Вуглеводи
Вуглеводи Понятие о качественных реакциях. 9 класс
Понятие о качественных реакциях. 9 класс Адам мен жануар организміне бордың әсері
Адам мен жануар организміне бордың әсері Жиры. Классификация жиров
Жиры. Классификация жиров Азокрасители. Цвет, классификация
Азокрасители. Цвет, классификация Химические аспекты выбора полимеров-предшественников для получения углеродных волокон
Химические аспекты выбора полимеров-предшественников для получения углеродных волокон Реакции замещения
Реакции замещения Химическая термодинамика. Лекция 2
Химическая термодинамика. Лекция 2 Химический источник электрического тока
Химический источник электрического тока Выполнила ученица 9б класса Коробатова Алена Учитель: Дьяченко Людмила Александровна
Выполнила ученица 9б класса Коробатова Алена Учитель: Дьяченко Людмила Александровна Фосфор красный, белый и черный
Фосфор красный, белый и черный Общая характеристика элементов IIIA-группы. Бор. Алюминий
Общая характеристика элементов IIIA-группы. Бор. Алюминий Индиго-краситель
Индиго-краситель Сера, ее физические и химические свойства
Сера, ее физические и химические свойства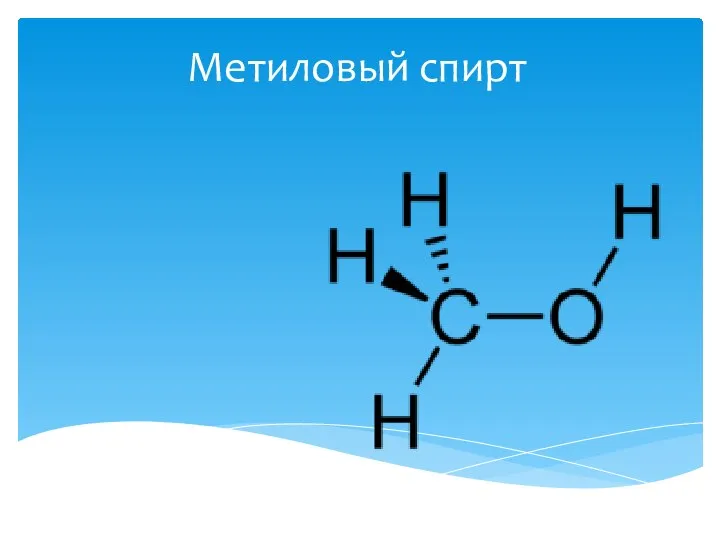 Метиловый спирт
Метиловый спирт Требование к оформлению отчета лабораторной работы
Требование к оформлению отчета лабораторной работы Значение окислительно-восстановительных реакций в жизни человека
Значение окислительно-восстановительных реакций в жизни человека Координационные соединения и их применение в медицине, фармакологии
Координационные соединения и их применение в медицине, фармакологии Нефть Общие сведения
Нефть Общие сведения Сульфаттар және эфирсульфаттар
Сульфаттар және эфирсульфаттар