Содержание
- 2. Документы, которые определяют структуру и содержание экзаменационной работы ЕГЭ 2015 года: Кодификатор элементов содержания и требований
- 3. Предназначение кодификатора определяет общий объём содержания курса химии, проверяемого на экзамене
- 4. Структура кодификатора состоит из двух частей: Часть 1 «Перечень элементов содержания, проверяемых на едином государственном экзамене
- 5. Часть 1 «Перечень элементов содержания, проверяемых на едином государственном экзамене по химии» перечислены те понятия, законы,
- 6. Часть 2 «Перечень требований к уровню подготовки, проверяемых на едином государственном экзамене по химии» содержит перечень
- 7. «Спецификация контрольных измерительных материалов для проведения в 2015 году единого государственного экзамена по химии» наиболее полно
- 8. В спецификации подробно описаны структура и план экзаменационной работы ЕГЭ по химии этого года; дана характеристика
- 9. Изменения в КИМ ЕГЭ 2015 года по сравнению с 2014 годом 1. Изменена структура варианта КИМ:
- 10. Система оценивания заданий Верное выполнение каждого из заданий с порядковыми номерами 1 – 26 базового уровня
- 11. Система оценивания заданий Верное выполнение каждого из заданий с порядковыми номерами 27 – 35 повышенного уровня
- 12. Система оценивания заданий За верное выполнение всех заданий экзаменационной работы можно максимально получить 64 первичных баллов
- 13. Дополнительные справочные материалы: Периодическая система химических элементов Д.И. Менделеева; таблица растворимости солей, кислот и оснований в
- 14. Демонстрационный вариант представляет собой образец экзаменационной работы, составленный в соответствии со спецификацией на его примере можно
- 15. Обобщённый план экзаменационной работы Всего заданий в экзаменационной работе 40 Для каждой позиции в плане указаны:
- 16. Задание 1 Строение электронных оболочек атомов элементов первых четырех периодов: s-, p- и d-элементы. Электронная конфигурация
- 17. Примеры задания 1 Два неспаренных электрона на внешнем уровне в основном состоянии имеет атом 1)магния 2)углерода
- 18. Задание 2 Закономерности изменения химических свойств элементов и их соединений по периодам и группам Общая характеристика
- 19. Примеры задания 2 В каком ряду химические элементы расположены в порядке уменьшения их электроотрицательности? 1) Sb
- 20. Задание 3 Ковалентная химическая связь, ее разновидности и механизмы образования. Характеристики ковалентной связи (полярность и энергия
- 21. Примеры задания 3 Соединение с ионной связью образуется при взаимодействии 1) P и O2 2) Na
- 22. Задание 4 Электроотрицательность. Степень окисления и валентность химических элементов.
- 23. Пример задания 4 Хлор проявляет положительную степень окисления в соединениях с 1) фосфором 2) кислородом 3)
- 24. Задание 5 Вещества молекулярного и немолекулярного строения. Тип кристаллической решетки. Зависимость свойств веществ от их состава
- 25. Пример задания 5 Вещество с высокой температурой плавления, очень малой электропроводностью расплава, нерастворимое в воде, имеет
- 26. Задание 6 Классификация неорганических веществ. Номенклатура неорганических веществ (тривиальная и международная).
- 27. Пример задания 6 Среди перечисленных веществ: А) Ba(NO3)2 Б) Ca(HS)2 В) (NH4)2SО4 Г) MgHPO4 Д) CaBr2
- 28. Задание 7 Характерные химические свойства простых веществ-металлов: щелочных, щелочноземельных, алюминия; переходных металлов: меди, цинка, хрома, железа.
- 29. Задание 8 Характерные химические свойства оксидов: оснóвных, амфотерных, кислотных.
- 30. Задание 9 Характерные химические свойства оснований и амфотерных гидроксидов. Характерные химические свойства кислот.
- 31. Задание 10 Характерные химические свойства солей: средних, кислых, оснóвных, комплексных (на примере соединений алюминия и цинка).
- 32. Задание 11 Взаимосвязь неорганических веществ
- 33. Примеры заданий 7 - 11 При термическом разложении какой соли не образуется твёрдый остаток? 1) NH4NO3
- 34. Задание 12 Теория строения органических соединений: гомология и изомерия (структурная и пространственная). Типы связей в молекулах
- 35. Пример задания 12 Изомером этанола является 1) СН3СООН 2) CH3–O–CH3 3) СН3СНО 4) C3H7OH
- 36. Задания 13 - 15 Характерные химические свойства углеводородов: алканов, циклоалканов, алкенов, диенов, алкинов, ароматических углеводородов (бензола
- 37. Пример задания И бутан, и бутен реагируют с 1) аммиачным раствором Ag2O 2) раствором KMnO4 3)
- 38. Задание 16 Основные способы получения углеводородов кислородсодержащих соединений
- 39. Пример задания 16 При взаимодействии какого вещества с водой можно получить уксусный альдегид? 1) C2H2 2)
- 40. Задание 17 Взаимосвязь углеводородов и кислородсодержащих органических соединений
- 41. Пример задания 17 В схеме превращений веществом Х является 1) этаналь 2) этанол 3) этан 4)
- 42. Задания 18 – 21 Ориентированы на проверку знаний о химической реакции: классификация химических реакций в неорганической
- 43. Пример задания Изменение давления не влияет на скорость реакции между 1) N2 и H2 2) Al
- 44. Задание 22 Правила работы в лаборатории. Правила безопасности при работе с едкими, горючими и токсичными веществами,
- 45. Пример задания 22 Верны ли следующие суждения о свойствах указанных веществ, которые необходимо учитывать при работе
- 46. Задание 23 Понятие о металлургии: общие способы получения металлов. Общие научные принципы химического производства (на примере
- 47. Пример задания 23 Верны ли следующие суждения о производстве метанола? А. Для осуществления реакции СО +
- 48. На позициях 24, 25 и 26 присутствуют три расчетные задачи Выполнение этих заданий предполагает применение умений
- 49. Пример задания Согласно термохимическому уравнению реакции окисления глюкозы C6H12O6(тв) + 6O2(г) = 6CO2(г) + 6H2O(г) +
- 50. Задания 27 - 32 Представляют собой задания повышенного уровня сложности. По форме предъявления условия – задания
- 51. Задания 27 - 32 Проверяют усвоение следующих элементов содержания: Классификация и номенклатура органических соединений (27). Степень
- 52. Пример задания 31 Установите соответствие между формулой вещества и реагентами, с каждым из которых это вещество
- 53. Пример задания 32 Установите соответствие между формулами веществ и реагентом, с помощью которого их можно различить.
- 54. Задания 33 - 35 Представляют собой задания повышенного уровня сложности. По форме предъявления условия – задания
- 55. Задания 33 - 35 Проверяют усвоение следующих элементов содержания: Характерные химические свойства углеводородов: алканов, циклоалканов, алкенов,
- 56. Пример задания 35 И диметиламин, и анилин взаимодействуют с 1) хлоридом кальция 2) гидроксидом натрия 3)
- 57. Задания с развёрнутым ответом (36 - 40) Проверяют усвоение следующих элементов содержания: Реакции окислительно-восстановительные (36). Реакции,
- 58. Пример задания 36 Используя метод электронного баланса, составьте уравнение реакции: H2S + K2Cr2O7 + … …
- 59. Пример задания 37 Смесь оксида азота(IV) и кислорода пропустили через раствор гидроксида калия. Полученную при этом
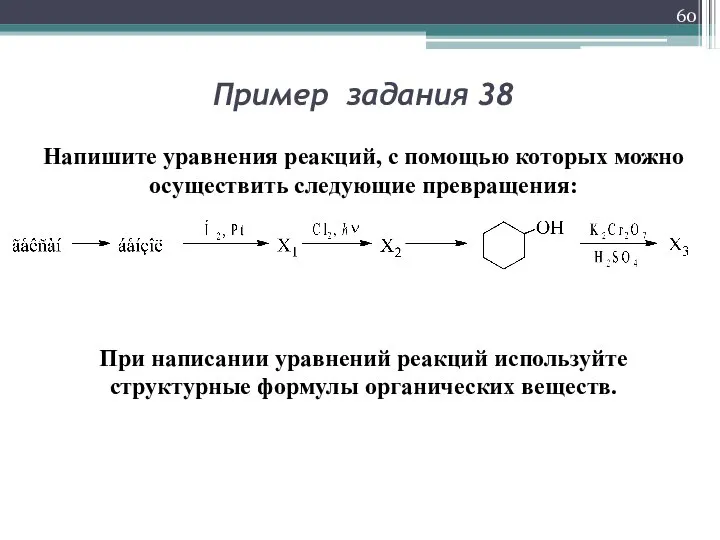
- 60. Пример задания 38 Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения: При написании уравнений
- 61. Пример задания 39 Фосфор массой 12,42 г прореагировал при нагревании с избытком хлора. Полученный хлорид растворили
- 62. Пример задания 40 При сжигании образца некоторого органического соединения массой 14,8 г получено 35,2 г углекислого
- 63. Элементы ответа: 1) Найдено количество вещества продуктов сгорания: Общая формула вещества CxHyOz n(CO2) = 35,2/44 =
- 64. Элементы ответа (продолжение) 3) Составлена структурная формула вещества: 4) Записано уравнение реакции вещества с оксидом меди(II):
- 66. Скачать презентацию






























































 «ШАРИКИ СЧАСТЬЯ» Неустроева Светлана Габдульхатовна, учитель I категории, МБОУ «СОШ №31», г.Нижнекамск
«ШАРИКИ СЧАСТЬЯ» Неустроева Светлана Габдульхатовна, учитель I категории, МБОУ «СОШ №31», г.Нижнекамск Презентация по Химии "Белки." - скачать смотреть бесплатно
Презентация по Химии "Белки." - скачать смотреть бесплатно Электролиз веществ
Электролиз веществ Сердечные гликозиды. Общая характеристика, методы выделения, анализ. (Тема 7)
Сердечные гликозиды. Общая характеристика, методы выделения, анализ. (Тема 7) Physics and chemistry of surface phenomena
Physics and chemistry of surface phenomena Д.И. Менделеевтің өмірі мен қызметі. Периодтық заңның маңызы
Д.И. Менделеевтің өмірі мен қызметі. Периодтық заңның маңызы Оцтова кислота
Оцтова кислота Математика и химия
Математика и химия Гидролиз солей
Гидролиз солей Электролит және бейэлектролит ерітінділердің коллигативті қасие
Электролит және бейэлектролит ерітінділердің коллигативті қасие Фосфор
Фосфор Спирты. Состав и строение спиртов
Спирты. Состав и строение спиртов Ionization Energy
Ionization Energy Сера и ее соединения
Сера и ее соединения Нафта Хімічна природа і утворення
Нафта Хімічна природа і утворення  Химия в сельском хозяйстве
Химия в сельском хозяйстве Презентация по Химии "Ліки" - скачать смотреть бесплатно
Презентация по Химии "Ліки" - скачать смотреть бесплатно Чистые вещества. Смеси
Чистые вещества. Смеси Оксиды. Классификация и химические свойства
Оксиды. Классификация и химические свойства Виды присадок к моторным топливам
Виды присадок к моторным топливам ТИПЫ ХИМИЧЕСКОЙ СВЯЗИ Цели: Дать понятия ионной, ковалентной, металлической, водородной хим.связям; Научить определять и запис
ТИПЫ ХИМИЧЕСКОЙ СВЯЗИ Цели: Дать понятия ионной, ковалентной, металлической, водородной хим.связям; Научить определять и запис Примеры реакций в жизни и в быту. Реакции по направлению процесса
Примеры реакций в жизни и в быту. Реакции по направлению процесса Термодинамика поверхностных явлений. (Часть 2)
Термодинамика поверхностных явлений. (Часть 2) Пластмаси
Пластмаси  Использование QR-кода в обучении химии
Использование QR-кода в обучении химии Природные каменные материалы. (Лекция 3)
Природные каменные материалы. (Лекция 3) Электрические поля в фотосинтетических мембранах
Электрические поля в фотосинтетических мембранах Амины, анилин
Амины, анилин