Содержание
- 2. Итог проверки пробника 5/60 первичных. По 1 б за номера 3, 7, 12. 2 б за
- 3. Содержание ЕГЭ Вторая часть 30 – ОВР 31- РИО (знание свойств солей, кислот и оснований) 32-
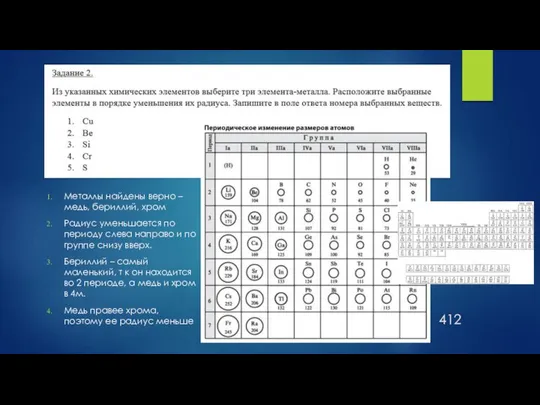
- 4. 412 Металлы найдены верно – медь, бериллий, хром Радиус уменьшается по периоду слева направо и по
- 5. Задание 5. Аммиачная селитра – NH4NO3 В1 «Селитры» – соли азотной кислоты HNO3 Индийская селитра –
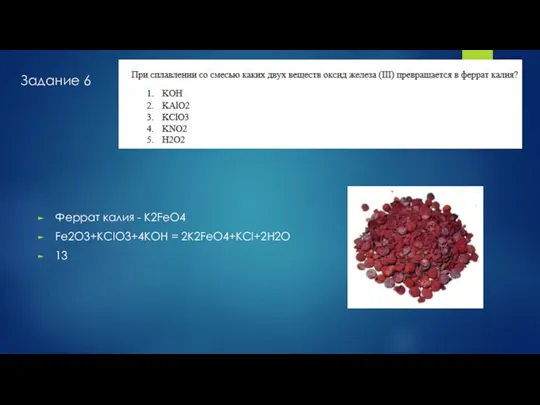
- 6. Задание 6 Феррат калия - K2FeO4 Fe2O3+KClO3+4KOH = 2K2FeO4+KCl+2H2O 13
- 7. Задание 7 Х – 1
- 8. 1123 SO2+2H2S=3S+2H2O S(+4)-?S(0) S(-2)-?S(0) Реакция сопропорционирования (функции окислителя и восстановителя выполняет один и тот же элемент
- 9. 2 1 ZnCl2+K2S=ZnS(осадок)+2KCl H2S – слабая кислота, диссоциирует обратимо 2ZnS+3O2=2ZnO+2SO2
- 10. Задание 11 Молекулярная формула стирола – С8Н8 Общая формула алканов – CnH2n+2. Алкан, содержащий 8 атомов
- 12. Стеарат кальция Ca(C₁₇H₃₅COO)₂ Соль стеариновой кислоты
- 13. Задание 21. Ответ: 231 PH3 – фосфин. СО: -3 Низшая. Может только отдавать электроны, только восстановитель
- 14. Задание 32 2KH2PO4 + 3Ca(OH)2 → Ca3(PO4)2 + 2KOH + 4H2O Ca3(PO4)2 + 5C + 3SiO2
- 15. Электролиз (задание 22) + (32, 34) Электролиз – окислительно-восстановительные реакции, протекающие на электродах при пропускании эл.
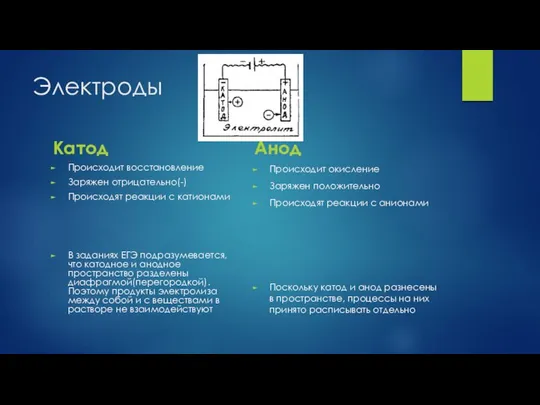
- 16. Электроды Катод Происходит восстановление Заряжен отрицательно(-) Происходят реакции с катионами В заданиях ЕГЭ подразумевается, что катодное
- 17. Электролиз расплавов Встречается электролиз расплавов галогенидов металлов, щелочей, оксида алюминия(Al2O3) 1. Диссоциация на ионы 2. Восстановление
- 18. Пример 2. Электролиз расплава гидроксида натрия
- 19. Электролиз расплава Al2O3 Важный промышленный процесс(служит для получения алюминия) Для снижения температуры плавления к расплаву добавляют
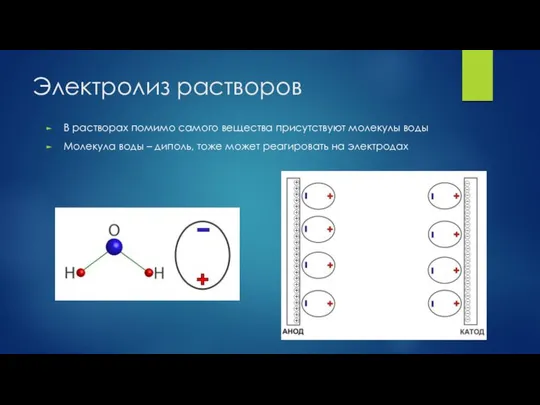
- 20. Электролиз растворов В растворах помимо самого вещества присутствуют молекулы воды Молекула воды – диполь, тоже может
- 21. Процессы на катоде
- 22. Процессы на аноде
- 23. Электролиз раствора нитрата цинка
- 24. Электролиз раствора фторида меди(||)
- 25. Электролиз раствора нитрата серебра
- 26. Электролиз раствора ацетата натрия
- 27. Задание: написать уравнение электролиза раствора бромида калия
- 28. Ответ:
- 29. Практика (№1) Установите соответствие между формулой соли и продуктом, образующимся на катоде при электролизе её водного
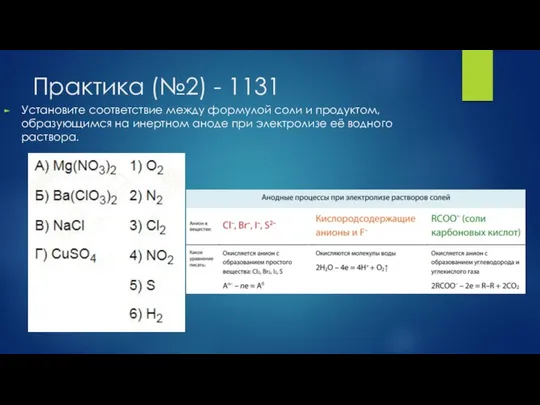
- 30. Практика (№2) - 1131 Установите соответствие между формулой соли и продуктом, образующимся на инертном аноде при
- 31. Практика (№3) - 4314 Установите соответствие между формулой вещества и газообразными продуктами электролиза его водного раствора:
- 32. Практика (№4) - 3441 Установите соответствие между формулой соли и продуктом электролиза водного раствора этой соли,
- 33. Практика (№5) - 2442 Установите соответствие между формулой соли и продуктом, образующимся на инертном аноде при
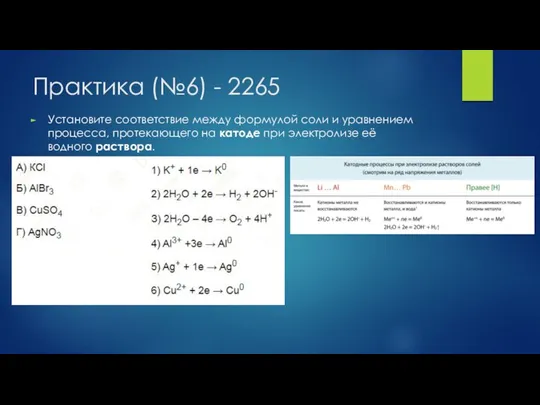
- 34. Практика (№6) - 2265 Установите соответствие между формулой соли и уравнением процесса, протекающего на катоде при
- 35. Практика (№7) - 3552 Установите соответствие между формулой вещества и электролитом, использующимся для его электрохимического получения:
- 36. Практика (№8) - 2421 Установите соответствие между формулой соли и продуктом, образующимся на инертном аноде при
- 37. Практика (№9) - 1543 Установите соответствие между формулой вещества и газообразными продуктами электролиза его водного раствора
- 38. Практика (№10) - 3646 Установите соответствие между формулой вещества и продуктами электролиза водного раствора этого вещества,
- 39. Задачи на электролиз 1. Сначала на электродах реагируют катионы и анионы, которые могут на них реагировать
- 41. Скачать презентацию
































 Степень окисления. Бинарные соединения металлов и не металлов: оксиды, хлориды, сульфиды и др.
Степень окисления. Бинарные соединения металлов и не металлов: оксиды, хлориды, сульфиды и др.  Презентация по Химии "Металлы – простые вещества" - скачать смотреть
Презентация по Химии "Металлы – простые вещества" - скачать смотреть  ПОДГОТОВКА К КОНТРОЛЬНОЙ РАБОТЕ ПО ТЕМЕ « Углеводороды» 10 класс. Автор: Ким Н.В. Учитель химии МБОУ «СОШ № 6» г.Нягань ХМАО-Югры
ПОДГОТОВКА К КОНТРОЛЬНОЙ РАБОТЕ ПО ТЕМЕ « Углеводороды» 10 класс. Автор: Ким Н.В. Учитель химии МБОУ «СОШ № 6» г.Нягань ХМАО-Югры Слайд-шоу
Слайд-шоу Аміни. Метиламін
Аміни. Метиламін Тема урока: Обобщение и систематизация знаний по теме: «Строение атома, химическая связь»
Тема урока: Обобщение и систематизация знаний по теме: «Строение атома, химическая связь» Гидролиз. Граф структуры
Гидролиз. Граф структуры Основные характеристики химического равновесия:
Основные характеристики химического равновесия: Композиты. Полимерные композиционные материалы
Композиты. Полимерные композиционные материалы Общая характеристика углерода
Общая характеристика углерода Голубое золото
Голубое золото Неорганическое композиционное антикоррозионное покрытие для защиты стальных деталей и особенности его формирования
Неорганическое композиционное антикоррозионное покрытие для защиты стальных деталей и особенности его формирования Химическая игра Своя игра
Химическая игра Своя игра Органика.
Органика. Адам ағзасында кездесетін химиялық элементтер
Адам ағзасында кездесетін химиялық элементтер Презентация "Гидролиз солей"
Презентация "Гидролиз солей" Виды состояния вещества
Виды состояния вещества Электронные конфигурации атомов химических элементов. Графическое изображение электронных конфигураций атомов
Электронные конфигурации атомов химических элементов. Графическое изображение электронных конфигураций атомов Призентація на тему: Способи виведення іржі
Призентація на тему: Способи виведення іржі  Альдегиды. Получение и применение
Альдегиды. Получение и применение Дисперсные системы. Свойства коллоидных растворов
Дисперсные системы. Свойства коллоидных растворов Галогены VII группы. Биологическая роль и применение в медицине
Галогены VII группы. Биологическая роль и применение в медицине Соединения галогенов
Соединения галогенов Аминокилоты. Получение и применение
Аминокилоты. Получение и применение Соли Mg SO4 – сульфат магния
Соли Mg SO4 – сульфат магния Галогены. Химические свойства
Галогены. Химические свойства Ионообменная хроматография и ее применение
Ионообменная хроматография и ее применение Оксосоединения: альдегиды и кетоны
Оксосоединения: альдегиды и кетоны