Содержание
- 2. Оксосоединения характеризуются присутствием в молекулах группы С=О, называемой карбонилом или карбонильной группой Она придает данным соединениям
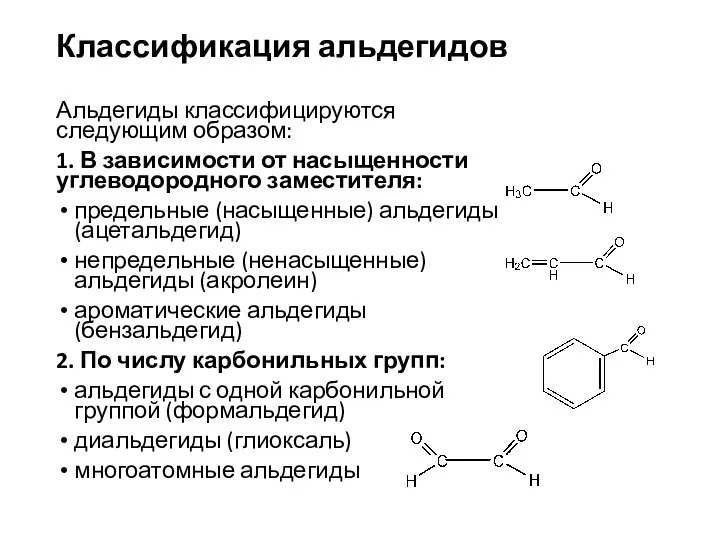
- 3. Классификация альдегидов Альдегиды классифицируются следующим образом: 1. В зависимости от насыщенности углеводородного заместителя: предельные (насыщенные) альдегиды
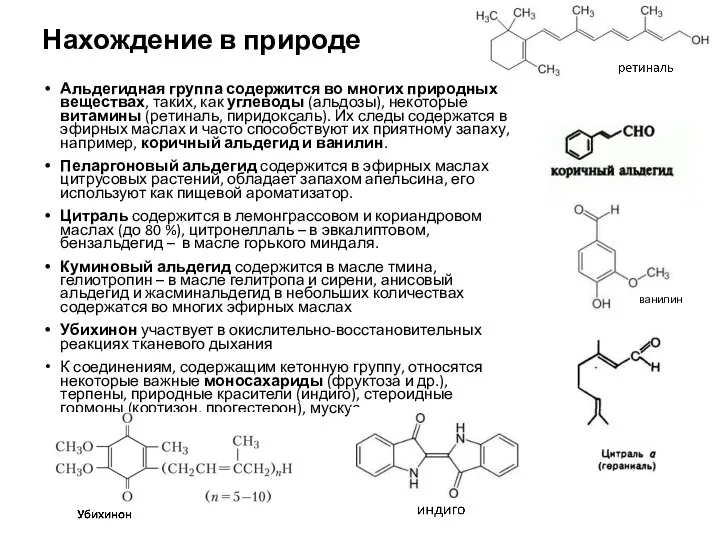
- 4. Нахождение в природе Альдегидная группа содержится во многих природных веществах, таких, как углеводы (альдозы), некоторые витамины
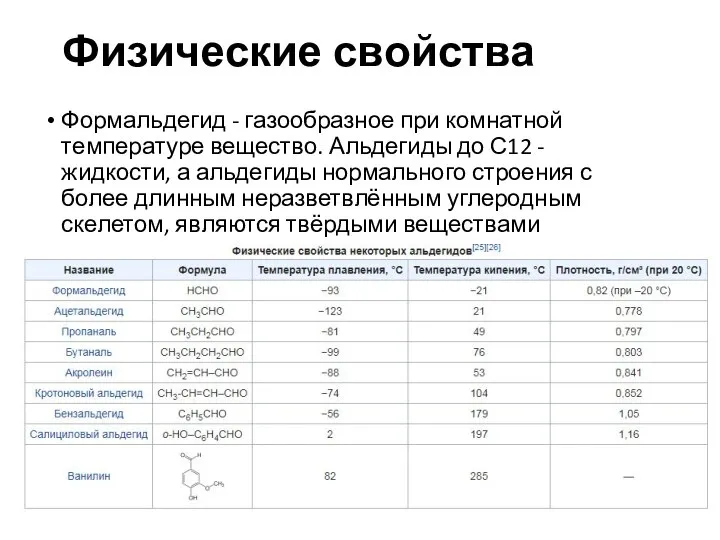
- 5. Физические свойства Формальдегид - газообразное при комнатной температуре вещество. Альдегиды до С12 - жидкости, а альдегиды
- 6. Температуры кипения альдегидов с неразветвлённым строением углеродной цепи выше, чем у их изомеров. Они кипят при
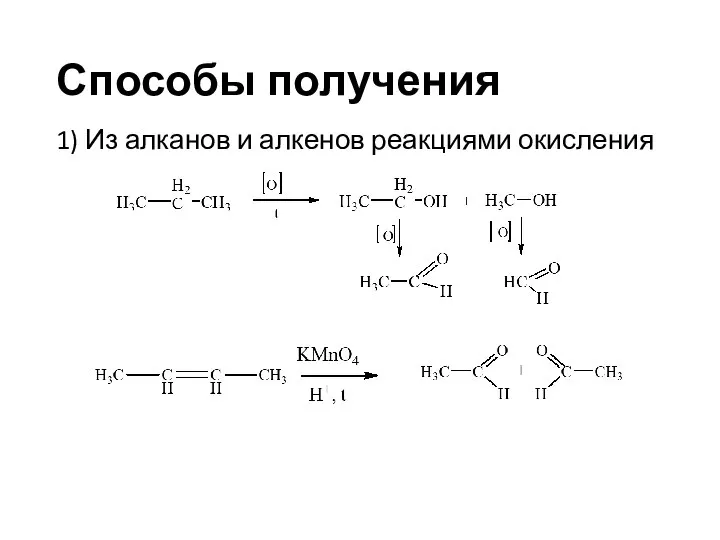
- 7. Способы получения 1) Из алканов и алкенов реакциями окисления
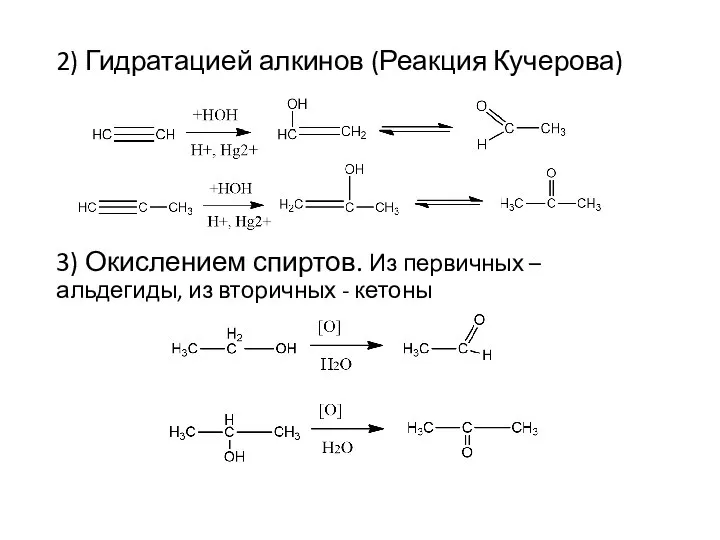
- 8. 2) Гидратацией алкинов (Реакция Кучерова) 3) Окислением спиртов. Из первичных – альдегиды, из вторичных - кетоны
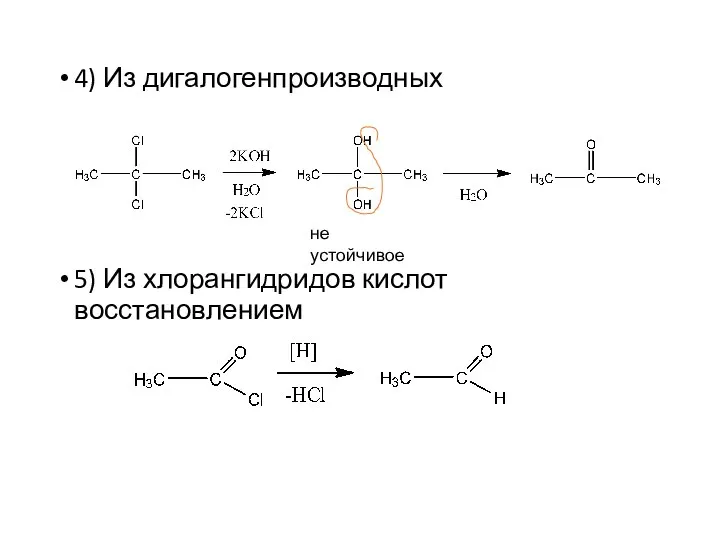
- 9. 4) Из дигалогенпроизводных 5) Из хлорангидридов кислот восстановлением не устойчивое
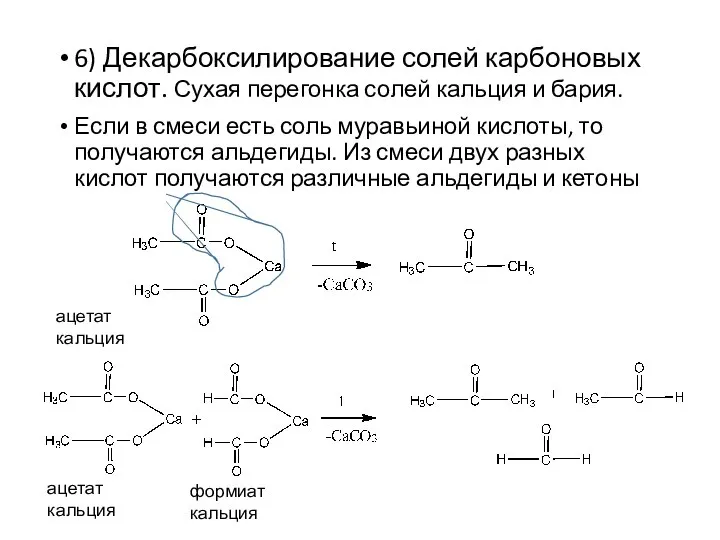
- 10. 6) Декарбоксилирование солей карбоновых кислот. Сухая перегонка солей кальция и бария. Если в смеси есть соль
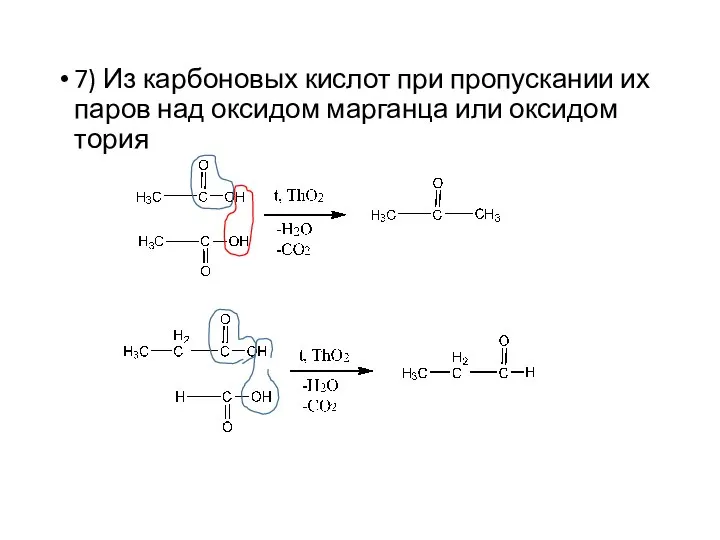
- 11. 7) Из карбоновых кислот при пропускании их паров над оксидом марганца или оксидом тория
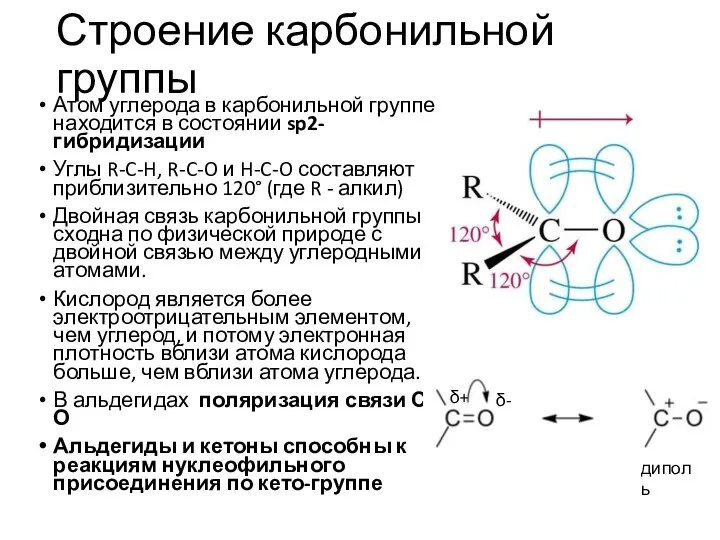
- 12. Строение карбонильной группы Атом углерода в карбонильной группе находится в состоянии sp2-гибридизации Углы R-C-H, R-C-O и
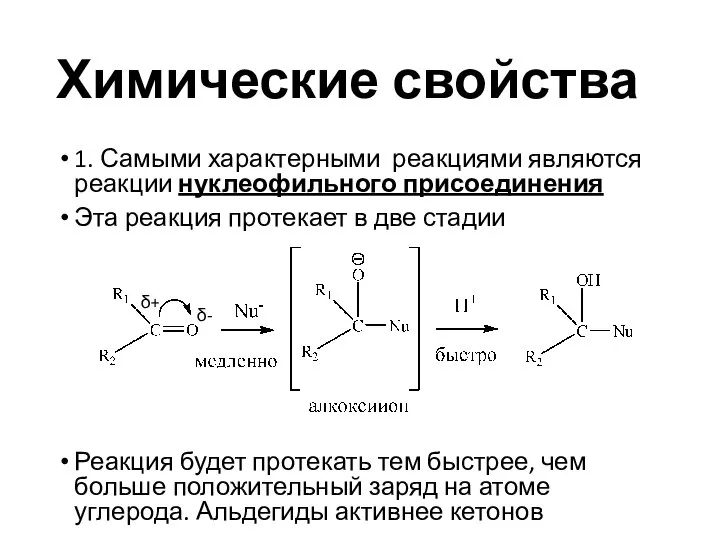
- 13. Химические свойства 1. Самыми характерными реакциями являются реакции нуклеофильного присоединения Эта реакция протекает в две стадии
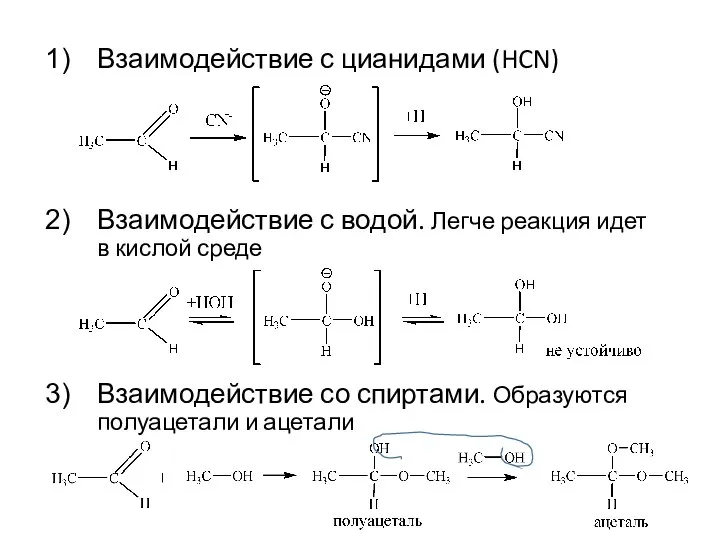
- 14. Взаимодействие с цианидами (HCN) Взаимодействие с водой. Легче реакция идет в кислой среде Взаимодействие со спиртами.
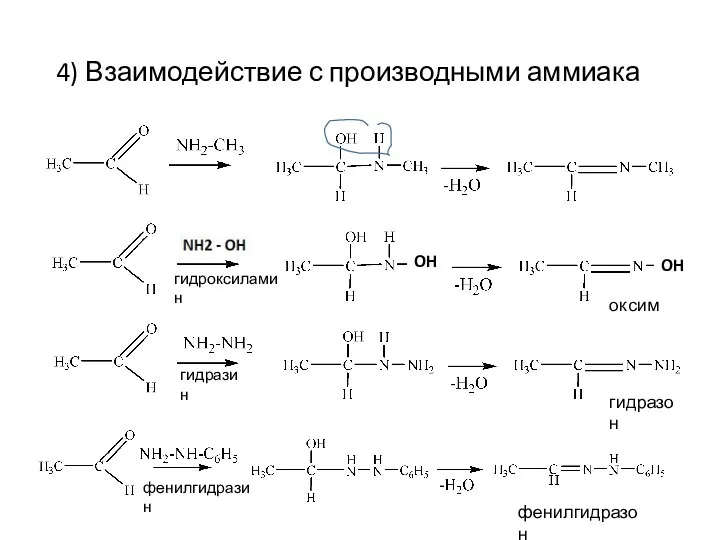
- 15. 4) Взаимодействие с производными аммиака оксим гидразон фенилгидразон OH OH гидроксиламин гидразин фенилгидразин
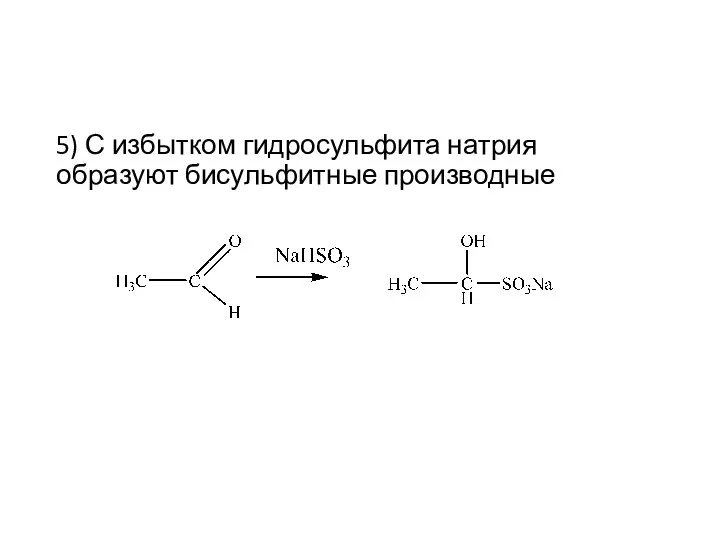
- 16. 5) С избытком гидросульфита натрия образуют бисульфитные производные
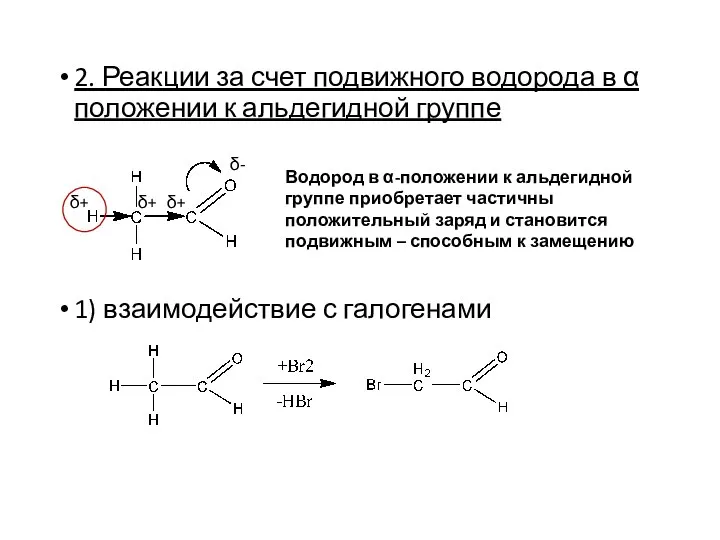
- 17. 2. Реакции за счет подвижного водорода в α положении к альдегидной группе 1) взаимодействие с галогенами
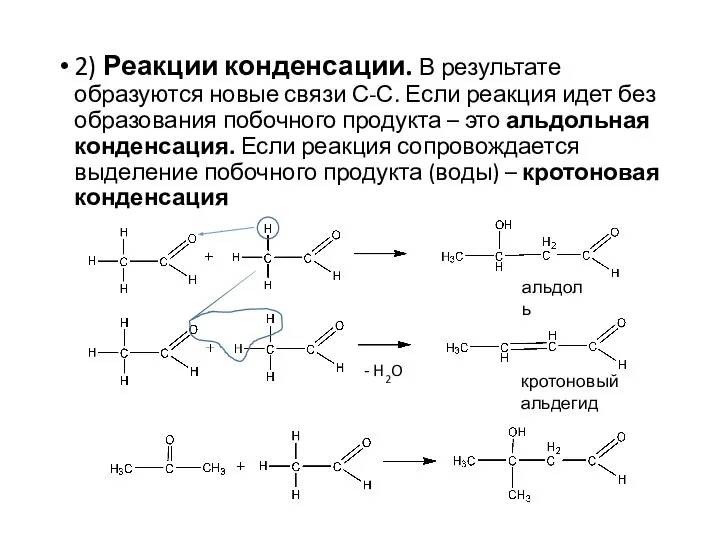
- 18. 2) Реакции конденсации. В результате образуются новые связи С-С. Если реакция идет без образования побочного продукта
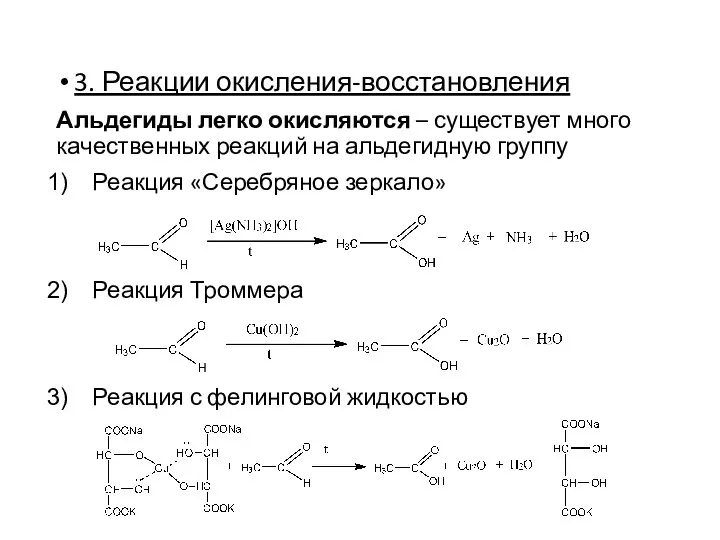
- 19. 3. Реакции окисления-восстановления Альдегиды легко окисляются – существует много качественных реакций на альдегидную группу Реакция «Серебряное
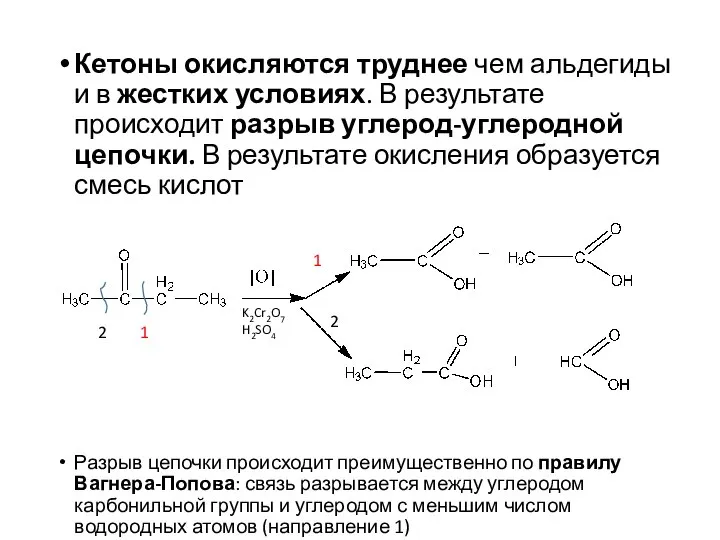
- 20. Кетоны окисляются труднее чем альдегиды и в жестких условиях. В результате происходит разрыв углерод-углеродной цепочки. В
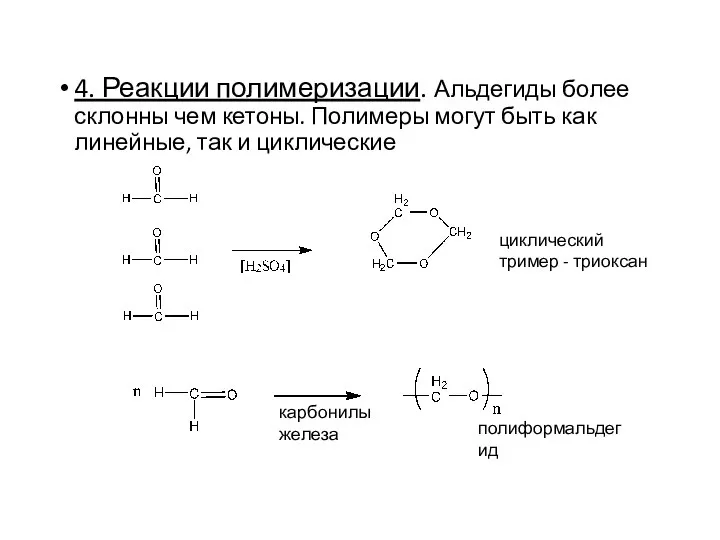
- 21. 4. Реакции полимеризации. Альдегиды более склонны чем кетоны. Полимеры могут быть как линейные, так и циклические
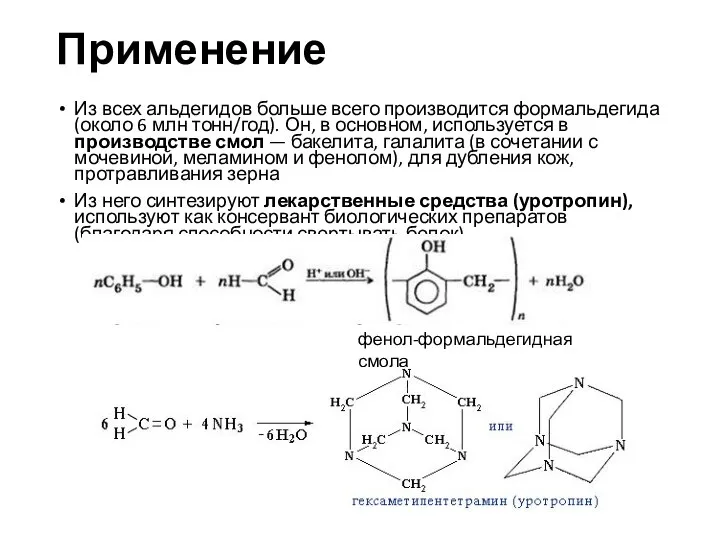
- 22. Применение Из всех альдегидов больше всего производится формальдегида (около 6 млн тонн/год). Он, в основном, используется
- 23. Некоторые альдегиды синтезируют только в небольших масштабах (менее 1000 тонн / год) и используют в качестве
- 25. Скачать презентацию



 Скорость реакции и температура. (Лекция 10)
Скорость реакции и температура. (Лекция 10) Презентация по Химии "Неорганические кислоты" - скачать смотреть
Презентация по Химии "Неорганические кислоты" - скачать смотреть  АЛОТРОПНІ ФОРМИ КАРБОНУ АВТОР: НАЗАРЕНКО МАКСИМ ВОЛОДИМИРОВИЧ 9-А КЛАС,ГІМНАЗІЯ №32 ПЕЧЕРСЬКИЙ РАЙОН, М. КИЇВ ПЕДАГОГІЧНИЙ КЕ
АЛОТРОПНІ ФОРМИ КАРБОНУ АВТОР: НАЗАРЕНКО МАКСИМ ВОЛОДИМИРОВИЧ 9-А КЛАС,ГІМНАЗІЯ №32 ПЕЧЕРСЬКИЙ РАЙОН, М. КИЇВ ПЕДАГОГІЧНИЙ КЕ Металлический водород
Металлический водород Аминокислоты «Единственный путь, ведущий к знанию – это деятельность» Б. Шоу
Аминокислоты «Единственный путь, ведущий к знанию – это деятельность» Б. Шоу Горные породы: гранит, базальт
Горные породы: гранит, базальт Ниобий. Физиологическое действие
Ниобий. Физиологическое действие Обмен холестерола
Обмен холестерола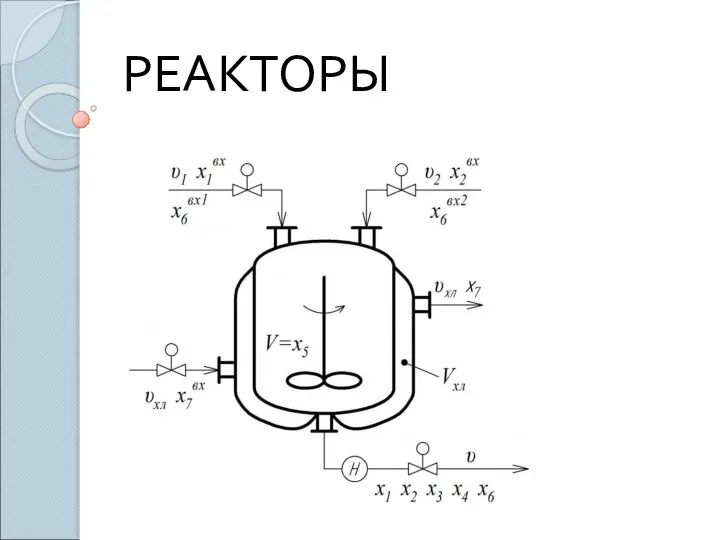 Реакторы. Основные требования к промышленным реакторам
Реакторы. Основные требования к промышленным реакторам Полімери
Полімери Спектроскопія ямр на ядрах 13с
Спектроскопія ямр на ядрах 13с Ауыр металдар
Ауыр металдар Основные способы получения солей. Отдельные представители солей
Основные способы получения солей. Отдельные представители солей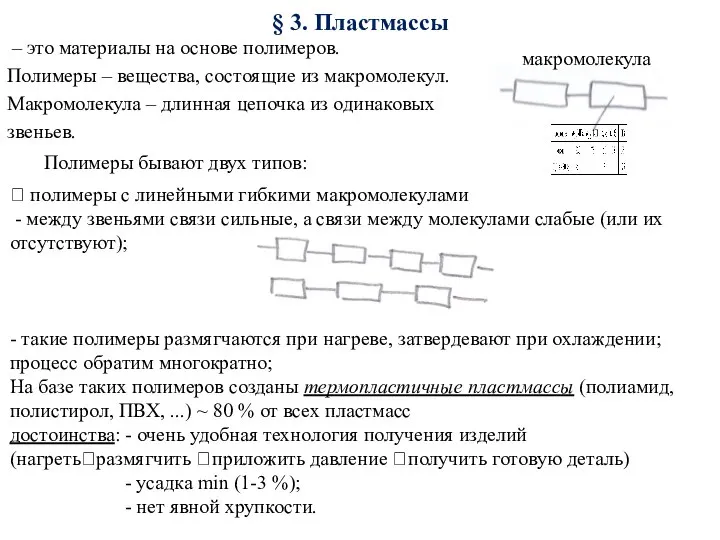 Пластмассы. Материалы, устойчивые против агрессивой среды
Пластмассы. Материалы, устойчивые против агрессивой среды Алкендер – қаныпаған көмірсутектер. Алынуы, химиялық қасиеттері және қолданылуы
Алкендер – қаныпаған көмірсутектер. Алынуы, химиялық қасиеттері және қолданылуы Полисахариды. Крахмал. Целлюлоза
Полисахариды. Крахмал. Целлюлоза Щелочноземельные металлы
Щелочноземельные металлы Сероводород в природе. Получение сероводорода синтетическим способом
Сероводород в природе. Получение сероводорода синтетическим способом Периодическая система химических элементов. Простые и сложные вещества
Периодическая система химических элементов. Простые и сложные вещества Аналитическая химия стойких органических загрязнителей
Аналитическая химия стойких органических загрязнителей Презентация по химии Аналитическая химия
Презентация по химии Аналитическая химия Химия элементов. Комплексные соединения. Основные понятия координационной теории. Номенклатура. Поведение в растворе
Химия элементов. Комплексные соединения. Основные понятия координационной теории. Номенклатура. Поведение в растворе Презентация по Химии "Амфотерные свойства воды" - скачать смотреть
Презентация по Химии "Амфотерные свойства воды" - скачать смотреть  История развития контролируемой радикальной полимеризации. Управление ростом полимерной цепи нитроксильными радикалами
История развития контролируемой радикальной полимеризации. Управление ростом полимерной цепи нитроксильными радикалами Интеррактивный кроссворд на тему: Химическая посуда и лабораторное оборудование
Интеррактивный кроссворд на тему: Химическая посуда и лабораторное оборудование Алюминий
Алюминий Основы коррозии и защиты металлов
Основы коррозии и защиты металлов Презентация по Химии "РАДИОИЗОТОПНЫЙ КОМПЛЕКС РИЦ-80. РАЗРАБОТКА НОВЫХ МЕТОДОВ ПОЛУЧЕНИЯ ГЕНЕРАТОРНОГО ИЗОТОПА Sr-82 И ДРУГИХ МЕДИ
Презентация по Химии "РАДИОИЗОТОПНЫЙ КОМПЛЕКС РИЦ-80. РАЗРАБОТКА НОВЫХ МЕТОДОВ ПОЛУЧЕНИЯ ГЕНЕРАТОРНОГО ИЗОТОПА Sr-82 И ДРУГИХ МЕДИ